Clear Sky Science · sv
Uppreglering av MGMT medierar temozolomidresistens som beror på USP5
Varför vissa hjärntumörer slutar svara på ett viktigt läkemedel
För personer med den aggressiva hjärntumören glioblastom är ett av de huvudsakliga läkemedlen som läkare förlitar sig på temozolomid. Inledningsvis kan denna kemoterapi bromsa sjukdomen, men tumörer lär sig ofta att stå emot den. Denna studie ställer en praktisk fråga med liv‑eller‑död‑konsekvenser: vad är det som exakt tillåter dessa cancerceller att undkomma läkemedlet, och kan vi hitta nya svaga punkter att angripa så att behandlingen börjar fungera igen?
Ett läkemedel som hjälper först, sedan försvagas effekten
Temozolomid fungerar genom att skada DNA i snabbt delande tumörceller och tvinga dem att dö. Många glioblastom producerar dock ett reparationsprotein kallat MGMT som kan ångra denna skada. Patienter vars tumörer slår på MGMT tenderar att få sämre utfall eftersom läkemedlets effekt neutraliseras. Läkare kan delvis förutsäga svar genom att kontrollera om MGMT‑genen är kemiskt avstängd (metylerad) eller aktiv (ometylerad), men detta förklarar inte fullt ut varför resistens utvecklas eller hur MGMT‑nivåerna förblir höga inne i tumörceller över tid.
Dolda hjälpande faktorer som skyddar reparationsproteinet
Författarna undersökte ett annat kontrollskikt: de molekylära ”städpatrullerna” som bestämmer vilka proteiner som ska förstöras och vilka som ska sparas. Celler taggar normalt utslitna proteiner för nedbrytning, medan en grupp enzymer kallade deubikvitinerande enzymer (DUBs) kan rädda proteiner från detta öde. Genom att gräva i stora offentliga cancer-databaser och studera läkemedelsresistenta glioblastomcellinjer odlade i labbet fokuserade teamet in sig på två sådana enzymer, USP5 och USP8. I tumörprover från hundratals patienter tenderade högre USP5‑nivåer att förekomma tillsammans med högre MGMT‑nivåer, och patienter vars tumörer hade båda generna uppreglerade dog i allmänhet tidigare.
Att bygga upp resistens i labbet
För att efterlikna vad som händer hos patienter utsatte forskarna två vanliga glioblastomcellinjer gradvis för ökande doser av temozolomid tills cellerna blev resistenta. I dessa härdade celler steg flera DUBs, men USP5, USP8, USP10 och reparationsproteinet MGMT var särskilt förhöjda. När teamet använde små RNA‑molekyler för att tysta USP5 eller USP8 blev de resistenta cellerna plötsligt sårbara: de aktiverade självdestruktionsprogram, inklusive apoptos och en form av stressdriven själv‑nedbrytning känd som autofagi. Samtidigt sjönk MGMT‑nivåerna kraftigt, och ett annat resistens‑kopplat protein, USP10, minskade också, vilket antyder att dessa enzymer sitter nära toppen av ett överlevnadsnätverk.
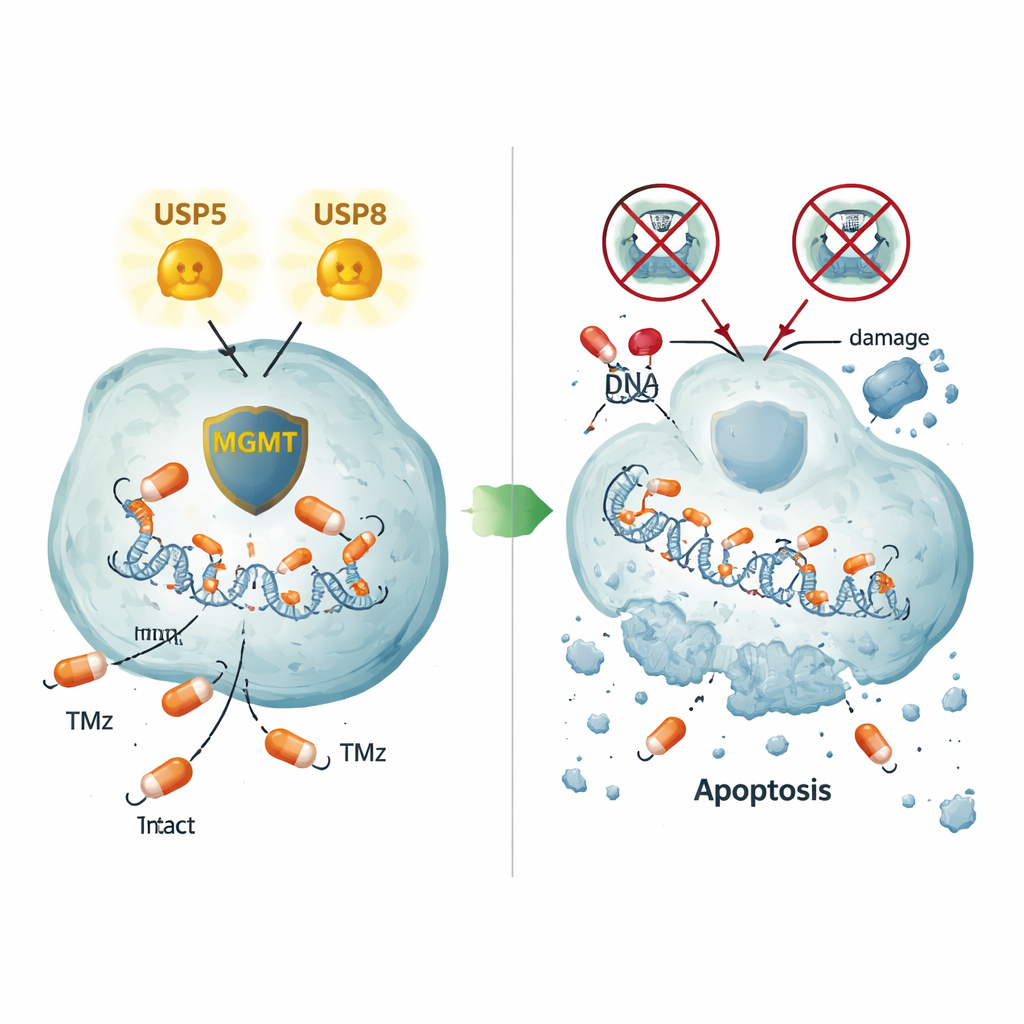
Två olika sätt att hålla MGMT vid liv
Noga avbildning av tumörceller och mänsklig tumörvävnad visade att USP5 och MGMT ofta lokaliserades tillsammans i samma regioner av cellen, särskilt i cytoplasman. Blockerad USP5 sänkte inte bara MGMT utan gjorde också att MGMT bröts ner av cellens protein‑kvarn, en process som kunde återställas med läkemedlet bortezomib, som blockerar proteasomen. Överuttryck av USP5 i celler som annars saknade MGMT var tillräckligt för att höja MGMT‑proteinnivåerna, även i en icke‑hjärncellinje, vilket bekräftar en direkt stabiliserande effekt. USP8 visade sig verka annorlunda: nedreglering av USP8 minskade också MGMT, men utan att förändra USP5 självt, vilket avslöjar en andra, USP5‑oberoende väg som hjälper till att behålla MGMT. Även i en resistent cellinje som inte alls producerade MGMT ledde avstängning av USP5 eller USP8 fortfarande till omfattande celldöd, vilket pekar på ytterligare resistensvägar som kontrolleras av dessa enzymer.
Kopplingar till immunsystemet och nya behandlingsidéer
Bortom läkemedelsresistens kopplar studien USP5 till hur glioblastom interagerar med immunsystemet. Analys av genomiska data föreslog att förändringar i USP5‑nivåer och genkopietal påverkar balansen av olika immunceller runt tumören, inklusive cytotoxiska T‑celler och regulatoriska T‑celler. Tidigare arbete har också visat att USP5 kan stabilisera PD‑L1, ett protein tumörer använder för att stänga av angripande T‑celler. Tillsammans tyder fynden på att USP5 kan hjälpa tumörer både att överleva kemoterapi och undfly immunsvar, vilket gör det till ett särskilt attraktivt läkemedelsmål.
Vad detta betyder för framtida hjärntumörbehandling
Enkelt uttryckt identifierar detta arbete USP5 och USP8 som nyckelväktare som skyddar reparationsproteinet MGMT och hjälper glioblastomceller att motstå temozolomid. Genom att avväpna dessa väktare kunde författarna döda läkemedelsresistenta celler i labbet och sänka MGMT‑nivåerna, även i vissa fall där MGMT‑baserad resistens inte var det enda problemet. Det väcker hopp om att framtida läkemedel riktade mot USP5 eller USP8, möjligen i kombination med befintlig kemoterapi och immunterapier, skulle kunna göra envisa hjärntumörer känsliga igen och ge patienter mer tid.
Citering: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
Nyckelord: glioblastom, resistens mot temozolomid, MGMT, USP5, deubikvitinerande enzymer