Clear Sky Science · sv
MNX1-medierade histonmodifieringar och PBX-genfamiljens roll i MNX1‑inducerad leukemogenes
Varför en liten genetisk miss spelar roll för sjuka barn
De flesta barndomsleukemier går numera att behandla, men en sällsynt form — spädbarnsakut myeloisk leukemi (AML) — är fortfarande särskilt dödlig. Många av dessa spädbarn delar samma genetiska olycka: två kromosomer byter bitar, vilket förvandlar en normalt tyst utvecklingsgen, MNX1, till en överaktiv drivkraft. Denna studie ställer en enkel men avgörande fråga: när MNX1 väl blir uppreglerad, vad gör den egentligen inne i unga blodceller för att driva dem mot cancer — och kan den processen avbrytas?
Från normala blodceller hos nyfödda till okontrollerad tillväxt
Leukemi uppstår när omogna blodceller slutar mogna och börjar dela sig okontrollerat. Hos spädbarn med t(7;12)-kromosombytet blir MNX1 onormalt aktiv i mycket tidiga blodbildande celler i fosterlever och benmärg. Forskarna byggde en musmodell som efterliknar denna situation: de slog på human MNX1 i fostrets blodstamceller, transplanterade dem till möss och följde hur djuren gick från ett pre-leukemiskt stadium till fullskalig leukemi. Genom att jämföra celler i dessa olika stadier med friska kontroller kunde de spåra hur MNX1 omprogrammerar cellens interna kontrollsystem över tid.
Hur MNX1 skriver om cellens instruktionsbok
MNX1 är en transkriptionsfaktor — ett protein som binder DNA och styr vilka gener som slås på eller av. Teamet kombinerade flera kraftfulla metoder — masspektrometri, RNA‑sekvensering och kromatinprofilering — för att se vilka partner MNX1 samarbetar med och vilka gener den påverkar. De fann att MNX1 samarbetar med enzymer som lägger till kemiska markörer på histonproteiner, de spolliknande strukturer som DNA är virat kring. Särskilt ökar MNX1 en "PÅ"-markör kallad H3K4me3 och minskar en "AV"-markör kallad H3K27me3 på vissa platser i genomet. Dessa förändringar luckrar upp den lokala DNA-strukturen och gör det lättare för viktiga tillväxtrelaterade gener att aktiveras.
En "hit-and-run"‑påverkan på en kritisk kontrollgen
Bland många påverkade gener framträdde en särskilt tydligt: Pbx1, som tillhör PBX-familjen av DNA‑bindande proteiner och länge kopplats till leukemi. Studien visar att MNX1 binder direkt till Pbx1-genens kontrollregion, ökar PÅ‑markören där och tar bort AV‑markören. Detta startar Pbx1‑uttrycket tidigt, när cellerna fortfarande bara är pre‑leukemiska. Överraskande nog — senare, när leukemin etablerats — sitter MNX1 inte längre starkt kvar vid den platsen, men Pbx1 förblir aktivt och dess histonmarkeringar ligger kvar i en pro‑tillväxtkonfiguration. Det tyder på en "hit-and-run"‑mekanism: MNX1 besöker kortvarigt viktiga kromatinregioner, lämnar beständiga epigenetiska markörer efter sig och kan sedan avlägsna sig medan det förändrade tillståndet fortsätter att driva sjukdomen.
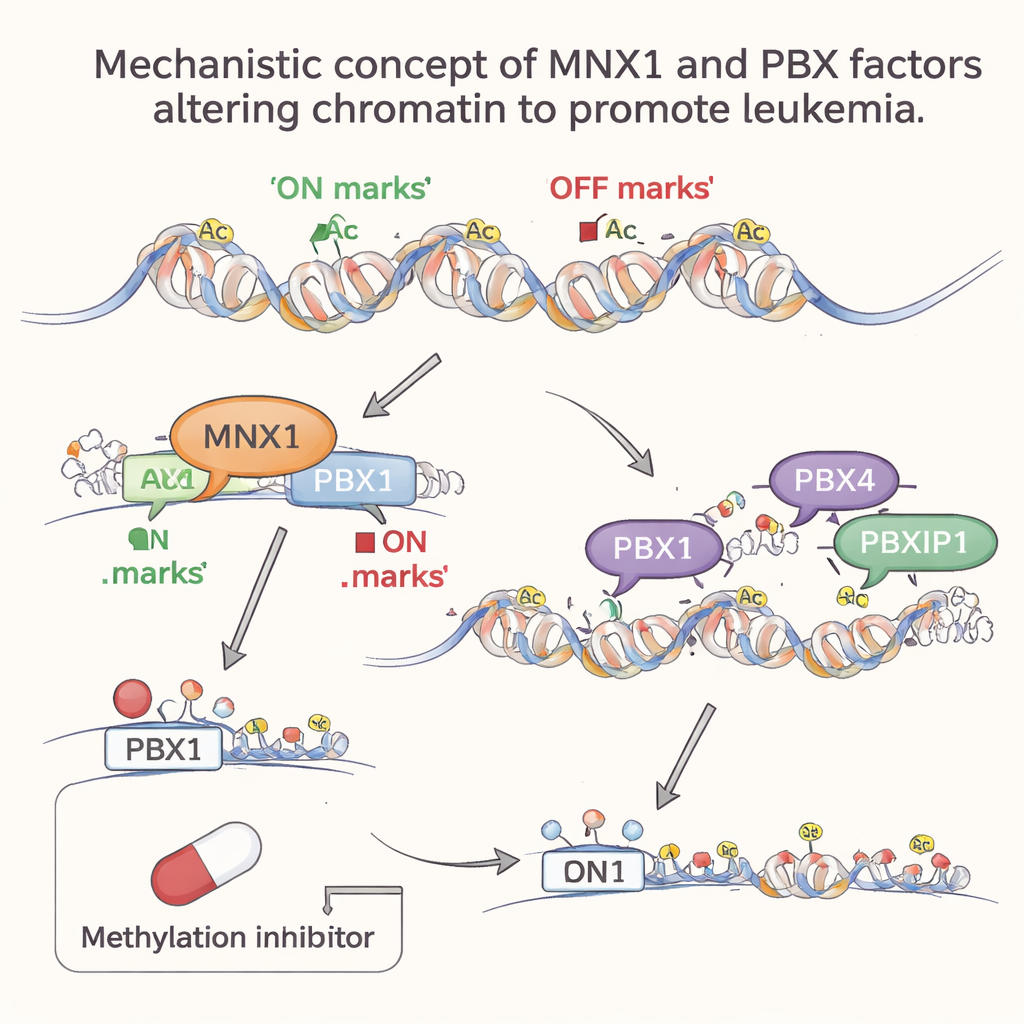
Senare medhjälpare går in för att låsa fast cancers tillstånd
När leukemin fortskrider blir andra PBX‑familjemedlemmar, PBX4 och PBXIP1, mer aktiva — men först i ett senare skede. Genom genome-wide analyser visade forskarna att deras föredragna DNA‑motiv är starkt berikade i regioner av öppet, aktivt kromatin som omformats efter MNX1‑aktiviteten. Med andra ord formar MNX1 först om kromatinlandskapet och sätter igång Pbx1; därefter flyttar PBX4 och PBXIP1 in i dessa nyåtkomliga regioner för att förstärka de onormala genprogram som främjar celldelning, blockerar normal blodutveckling och försämrar DNA‑reparation. Detta stegvisa deltagande antyder en arbetsdelning: PBX1 fungerar som en MNX1‑beroende tidig brytare, medan PBX4 och PBXIP1 hjälper till att upprätthålla det leukemiska programmet.
Blockera de kemiska markörer som driver leukemi
Eftersom MNX1 verkar via enzymer som lägger metylgrupper på histoner testade teamet om en bred metyltransferas‑inhibitor, Sinefungin, kunde störa denna kedja. I pre‑leukemiska fostrets blodceller som uttrycker MNX1 minskade Sinefungin kraftigt Pbx1‑nivåerna, vilket är förenligt med att blockera den promotor‑specifika metylering som MNX1 förlitar sig på. Däremot ändrades PBX4‑ och PBXIP1‑nivåerna knappt, vilket stämmer med deras senare, indirekta aktivering under sjukdomens utveckling. Tillsammans ger dessa resultat ett övertygande stöd för att spädbarns‑AML med t(7;12) drivs inte bara av en trasig gen utan av en kaskad av beständiga epigenetiska förändringar som MNX1 sätter igång.
Vad detta betyder för framtida behandlingar
För icke‑specialister är huvudbudskapet att studien kartlägger en kedjereaktion: en överaktiv MNX1‑gen omprogrammerar kemiska markörer på DNA‑packande proteiner, slår på PBX1 tidigt och banar väg för PBX4 och PBXIP1 att låsa cellerna i ett leukemiskt tillstånd. Eftersom dessa steg beror på specifika histonmetyleringsmönster erbjuder de tydliga, testbara mål för läkemedel som stör dessa markörer. I längden skulle terapier riktade mot MNX1–PBX‑axeln eller de enzymer som placerar dessa epigenetiska taggar kunna hjälpa till att stänga av de felaktiga instruktioner som driver denna aggressiva leukemi hos spädbarn och öka chansen till bestående bot.
Citering: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Nyckelord: spädbarnsakut myeloisk leukemi, MNX1, PBX1 PBX4 PBXIP1, epigenetisk histonmetylering, t(7;12)-kromosomtranslokation