Clear Sky Science · sv
Nedreglering av CDC25C hämmar levercancer (HCC)-tillväxt via mitokondriell stress‑inducerad autofagi och apoptos
Varför denna studie om levercancer är viktig
Levercancer är en av de dödligaste cancerformerna globalt, och många patienter upptäcks för sent för att kirurgi eller standardbehandlingar ska ge goda resultat. Denna studie undersöker en enskild cellulär “omkopplare”, ett protein kallat CDC25C, som tycks driva levercancertillväxt samtidigt som det är mindre avgörande för friska leverceller. Genom att dämpa denna omkopplare fann forskarna att de kunde stressa och slutligen döda cancerceller genom cellernas egna städunderhålls- och självförstörande system, vilket pekar mot en lovande och mer selektiv behandlingsstrategi.
En tillväxtomkopplare inne i levertumörer
Varje cell måste avgöra när den ska dela sig och när den ska sluta. CDC25C är ett av de nyckelproteiner som driver celler genom delningscykeln. I levercancer sitter denna omkopplare ofta fast i “på”-läge, vilket hjälper tumörer att växa och sprida sig. Forskarna använde muslevercancerceller och normala musleverceller, samt tumörbärande möss, för att artificiellt sänka CDC25C-nivåerna. De bekräftade, med standard genetiska och proteinanalyser, att CDC25C var kraftigt reducerat i experimentgruppen jämfört med kontroll, vilket etablerade en robust modell för att studera vad som händer när denna tillväxtomkopplare skruvas ner.
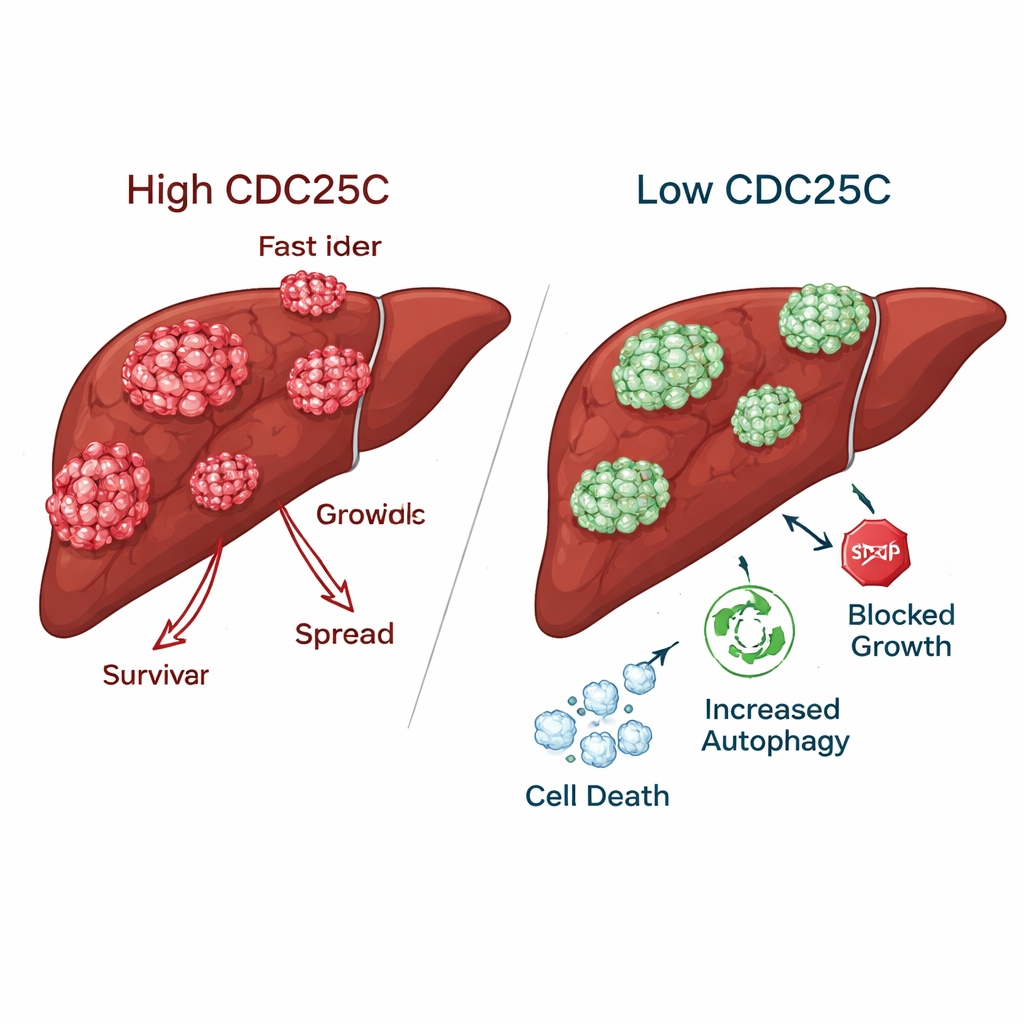
Hämmad cancer samtidigt som friska leverceller skonas
När CDC25C minskades i levercancerceller förlorade tumörerna många av sina aggressiva egenskaper. Cancerceller bildade betydligt färre kolonier, migrerade långsammare över artificiella “sår” och hade sämre förmåga att röra sig genom och invadera barriärer i laboratorietester. I kontrast visade normala leverceller faktiskt bättre tillväxt och rörlighet när CDC25C sänktes, vilket tyder på att frisk vävnad kan tolerera eller till och med dra nytta av CDC25C‑hämning. I möss visade tumörer som konstruerats med reducerad CDC25C lägre nivåer av detta protein både i gen- och proteinmätningar, vilket bekräftar att samma effekt uppstod i levande djur.
Mitokondriell stress och cellens städbesättning
Genom elektronenmikroskopi såg forskarna att cancerceller med låg CDC25C innehöll svullna, skadade mitokondrier — cellens små kraftverk — tillsammans med bubbel‑liknande strukturer kallade autofagosomer som indikerar aktivering av cellens interna återvinningssystem, autofagi. De mätte sedan viktiga tecken på mitokondriell stress: kalciumnivåer och reaktiva syreföreningar (ROS), som båda var förhöjda i cancerceller efter CDC25C‑sänkning. Markörer för mitokondriellt stressvar, inklusive hjälpproteiner som HSP60 och två mitokondriella ”kvalitetskontroll”‑enzymer, ökade också, liksom CHOP, en stressrelaterad faktor som länkar mitokondriella problem till bredare cellulära svar. Slående nog gick dessa stressignaler i motsatt riktning i normala leverceller, vilket förstärker idén att cancer‑ och friska celler reagerar mycket olika på förlusten av CDC25C.
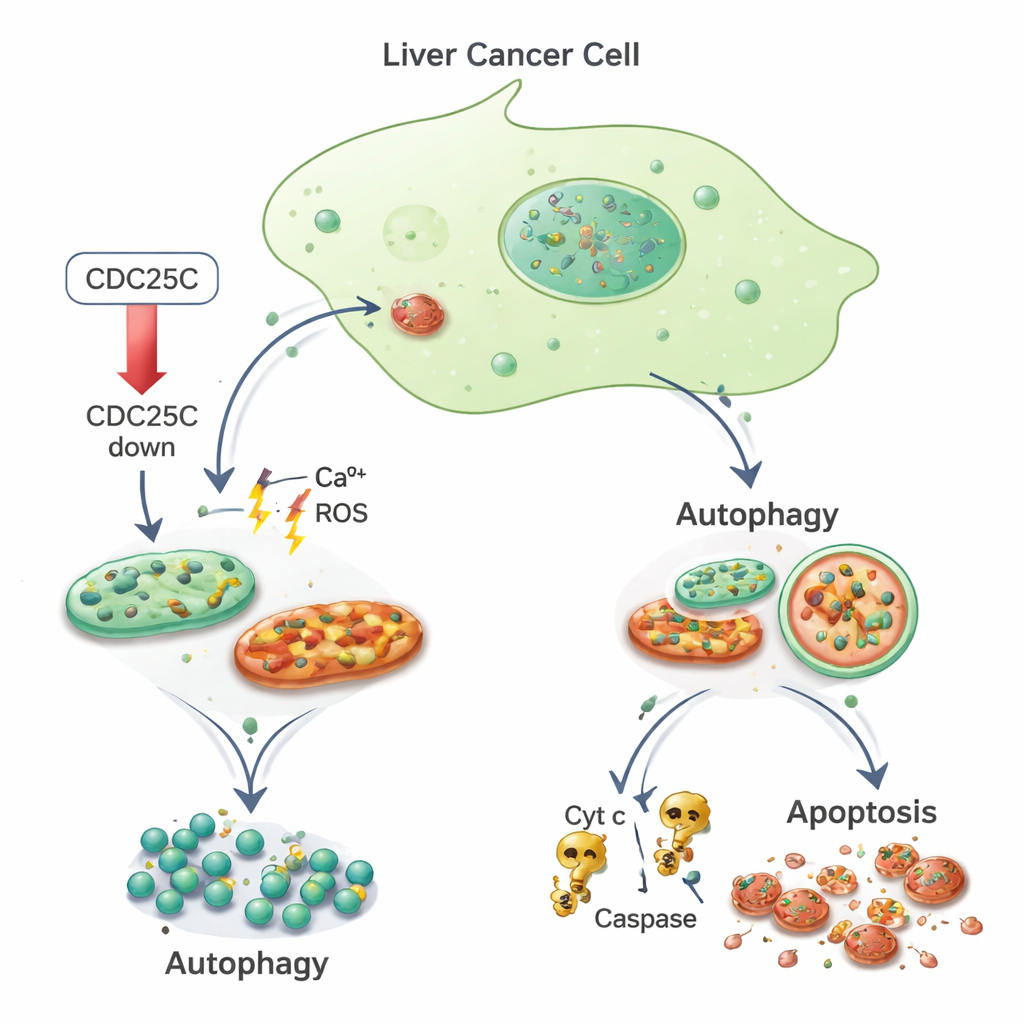
Från stress till självnedbrytning och celldöd
Forskarna undersökte sedan hur dessa stressade cancerceller hanterade situationen. De fann att markörer för autofagi ökade i både cancer‑ och normala leverceller när CDC25C minskades. Proteiner såsom LC3 och p62, som speglar bildandet och aktiviteten hos autofagosomer, steg i nivå och indikerade att cellerna ökade sin städmaskineri. Samtidigt, endast i cancerceller, tycks mitokondriell skada driva cellerna förbi reparerbarhet och in i programmerad celldöd. Med hjälp av fluorescerande färgningar och flödescytometri såg forskarna fler cancerceller med fragmenterade, starkt färgade kärnor — ett kännetecken för apoptos — och reducerad mitokondriemembranpotential. De fann också ökade nivåer av cytokrom c och enzymerna Caspase‑3 och Caspase‑9, klassiska komponenter i den mitokondriedrivna dödsvägen. Normala leverceller visade däremot mindre apoptos under samma CDC25C‑sänkande förhållanden.
Vad detta kan betyda för framtida behandlingar
För en lekmannaläsare är huvudbudskapet att nedreglering av CDC25C tycks träffa levercancerceller där de är som sårbarast: överbelasta deras kraftverk, driva deras återvinningssystem till överdrift och slutligen utlösa ren självförstörelse — samtidigt som friska leverceller i stor utsträckning skonas. Författarna drar slutsatsen att CDC25C är mer än en enkel tillväxtomkopplare; det formar också hur celler hanterar stress, städning och död. Eftersom cancerceller i hög grad är beroende av CDC25C och reagerar på dess förlust med dödlig mitokondriell stress och apoptos, kan läkemedel som riktar sig mot detta protein, eller dess nedströms stressvägar, en dag erbjuda ett mer selektivt sätt att behandla levercancer med färre skador på frisk levervävnad.
Citering: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Nyckelord: hepatocellulärt karcinom, CDC25C, mitokondriell stress, autofagi, apoptos