Clear Sky Science · sv
Faecal mikrobiom förutspår behandlingssvar efter påbörjad semaglutid- eller empagliflozinbehandling
Varför dina tarmbakterier kan påverka diabetesbehandling
Personer med typ 2‑diabetes får i allt större utsträckning nyare läkemedel såsom semaglutid (känd från viktminskningsannonser) och empagliflozin, som hjälper till att sänka blodsocker och kroppsvikt. Men inte alla svarar lika bra. Denna studie ställer en enkel men kraftfull fråga: kan de biljoner bakterier som lever i vår tarm förklara vem som gynnas mest av dessa läkemedel, och skulle de en dag kunna vägleda mer personanpassad diabetesvård?
Studien i korthet och vad som mättes
Forskare följde 20 vuxna med typ 2‑diabetes som redan tog standardläkemedlet metformin och hade fetma. Deras läkare lade till antingen semaglutid eller empagliflozin utifrån medicinskt behov. Under ett helt år lämnade deltagarna avföringsprov fyra gånger och blod‑ och urinprov tre gånger. Avföringsproven användes för att kartlägga tarmbakterierna, medan blod‑ och urintester följde viktiga hälsomarkörer såsom långtidsblodsocker (HbA1c), kroppsvikt, njurfunktion och tecken på inflammation. Denna design gjorde det möjligt för teamet att både se hur läkemedlen påverkade hälsan och om det initiala tarmmikrobiomet kunde förutse dessa förändringar. 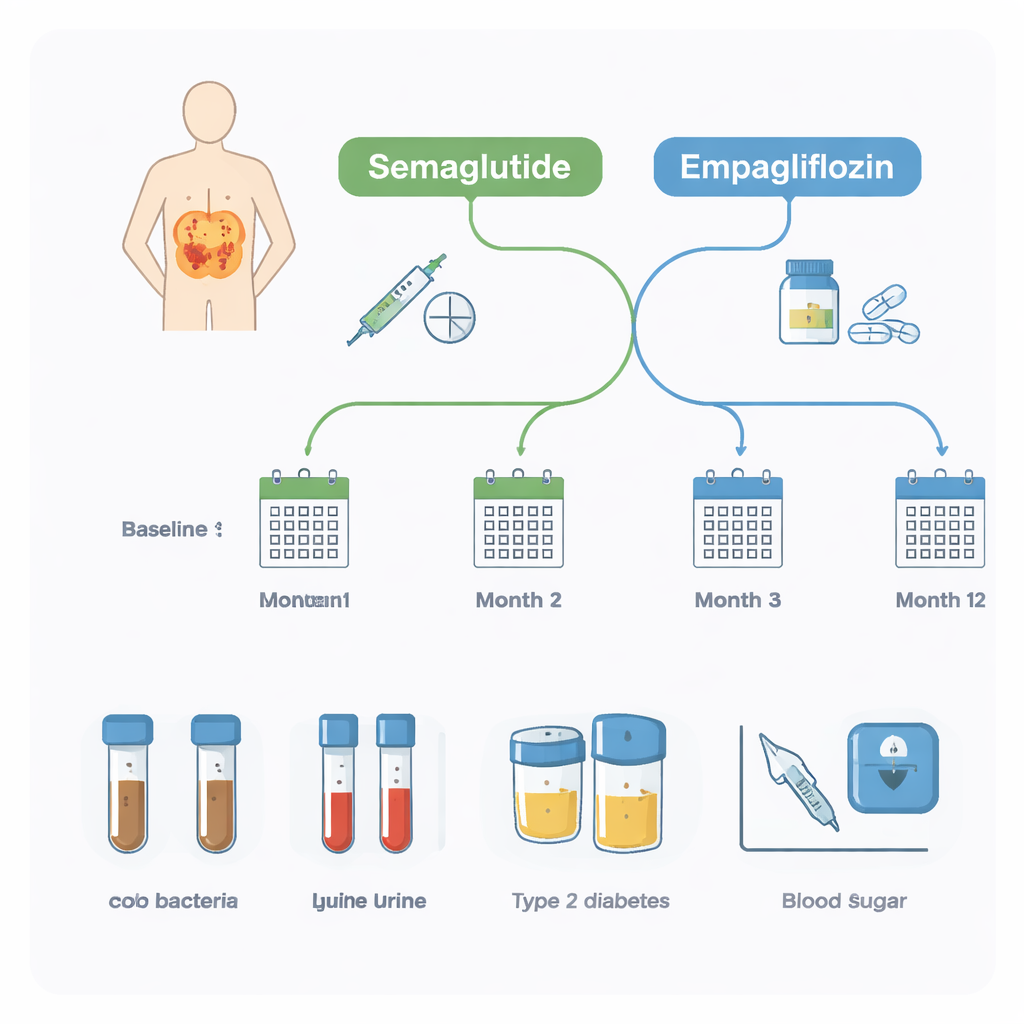
Hur läkemedlen påverkade hälsa och tarmflora
Kliniskt förbättrade båda läkemedlen blodsockerkontrollen vid tredje månaden av behandling, och särskilt semaglutid gav tydlig och bestående viktminskning under 12 månader. När teamet undersökte tarmbakteriell mångfald – hur många olika typer som fanns och hur jämnt de var fördelade – såg de ingen tydlig övergripande förändring efter start av något av läkemedlen. På samma sätt, när de tittade på bredare mönster i vilka bakteriegrupper som var närvarande, kvarstod de flesta uppenbara förändringar inte som statistiskt säkra när strikta korrigeringar för multipla tester tillämpades. Några bakteriegrupper och förutspådda metaboliska vägar verkade ändras mellan månad 3 och 12, men dessa mönster var modest och speglade troligen indirekta effekter av förbättrad metabolism eller förändrad livsstil snarare än en direkt verkan av läkemedlen själva.
Tarmbakterier som potentiella prediktorer för framgång
De mest intressanta fynden kom från att undersöka mikrobiomet före behandling och fråga om det kunde förutsäga vem som skulle förbättras mest. För personer som tog semaglutid visade hundratals mikrobiella startegenskaper nominella samband med senare förändringar i kliniska markörer, särskilt vita blodkroppar och ett mått på inflammation känt som neutrofil‑till‑lymfocyt‑kvoten. Efter strikt statistisk filtrering kvarstod en bakteriegrupp kallad Alistipes som signifikant associerad: individer med mer av denna bakterie vid baseline tenderade att få en större minskning av inflammatoriska celler. Flera bakteriegenera och mikrobiella vägar vid baseline korrelerade också med hur mycket HbA1c sjönk vid tredje månaden, vilket antyder att den initiala tarmcommunityn kan påverka hur kraftfullt semaglutid sänker blodsockret. I empagliflozingruppen kopplades också många bakterier och vägar till förändringar i HbA1c och mått på njurfunktion, men inget överlevde de mest konservativa statistiska testerna, delvis eftersom studien var liten.
Vad fynden betyder – och vad de inte betyder
Viktigt är att detta arbete inte påstår att semaglutid eller empagliflozin dramatiskt ombyggt tarmmikrobiomet på egen hand, eller att någon specifik bakterie garanterar framgång eller misslyckande. Snarare tyder det på att subtila egenskaper hos en persons befintliga tarmcommunity kan vara kopplade till hur kroppen svarar – inte bara vad gäller blodsocker utan också inflammation och andra hälsomarkörer. Eftersom alla deltagare redan tog metformin, vilket i sig påverkar tarmbakterier, kan den tillagda påverkan av de nyare läkemedlen ha varit svårare att upptäcka. Den begränsade provstorleken och vissa saknade prover minskar dessutom hur säkert enskilda bakteriegrupper kan pekas ut som verkliga drivkrafter för läkemedelssvar.
Framåtblick mot skräddarsydd diabetesvård
För en lekmannaläsare är slutsatsen att dina tarmbakterier en dag kan hjälpa läkare välja det diabetesläkemedel som fungerar bäst för dig. I denna tidiga studie kopplades sammansättningen av mikrober i avföringsprover tagna före behandling till hur starkt semaglutid och empagliflozin förbättrade blodsocker och inflammation, medan läkemedlen själva gav endast subtila, långsamma förändringar i tarmcommunities. Större och längre studier kommer att behövas för att bekräfta vilka mikrober som verkligen betyder något och om att förändra dem kan förstärka behandlingseffekter. Om dessa ansträngningar lyckas kan ett enkelt avföringstest bli en del av personlig diabetesvård och hjälpa matcha rätt läkemedel till rätt mikrobiom. 
Citering: Klemets, A., Reppo, I., Krigul, K.L. et al. Fecal microbiome predicts treatment response after the initiation of semaglutide or empagliflozin uptake. Sci Rep 16, 6126 (2026). https://doi.org/10.1038/s41598-026-36318-3
Nyckelord: tarmmikrobiom, typ 2-diabetes, semaglutid, empagliflozin, personlig medicin