Clear Sky Science · sv
Omdisposition av dapagliflozin via polymera nanogeler för kolorektalcancerterapi
Varför ett diabetesläkemedel kan hjälpa till att bekämpa tjocktarmscancer
Kolorektalcancer är en av de främsta orsakerna till cancerrelaterade dödsfall globalt, och många patienter drabbas av återfall trots operation och cytostatika. Denna studie utforskar en oväntad allierad mot sjukdomen: dapagliflozin, en vanlig tablett för typ 2‑diabetes. Genom att paketera läkemedlet i mycket små mjuka partiklar som bildar en mild gel i magen, vill forskarna leverera mer av substansen till tjocktarmen — där kolontumörer växer — samtidigt som den orala dosen hålls liknande befintliga tabletter.
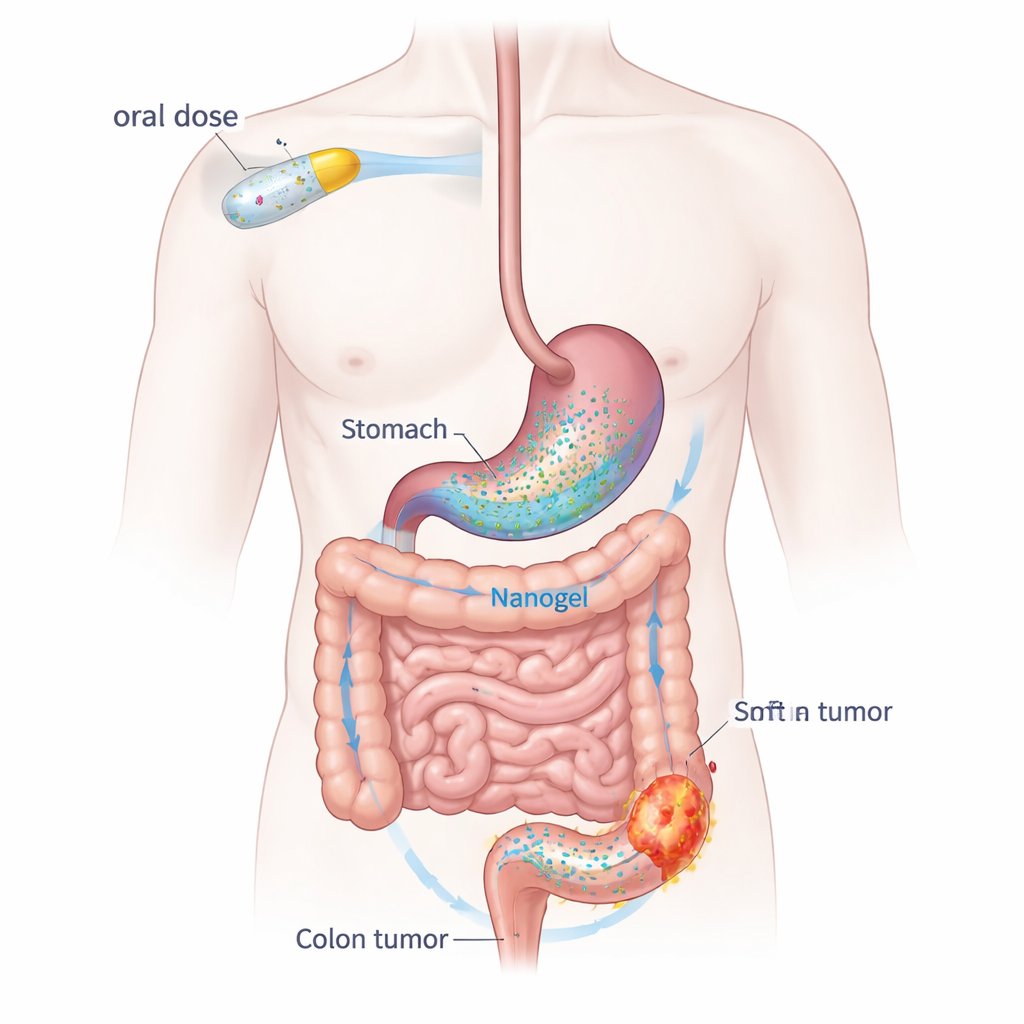
Att förvandla en vardaglig tablett till en cancerinriktad last
Dapagliflozin verkar normalt i njurarna för att sänka blodsockret, men det dämpar också inflammation och bromsar celltillväxt — två processer som cancer är beroende av. Läkemedlet löser sig dock dåligt i vatten och rensas snabbt från kroppen. För att övervinna detta byggde teamet ett ”nanogel”-leveranssystem med två livsmedelslika polymerer: natriumalginat, utvunnet från alger, och polyvinylalkohol, en allmänt använd biokompatibel förtjockningsmedel. Läkemedlet fångas in i nanopartiklar ungefär en tiotusendel av en millimeter i bredd. När dessa partiklar möter magsyra, sjunker de ihop och binds samman till en mjuk hydrogelmassa som ligger kvar och gradvis frisätter läkemedlet när det färdas mot tjocktarmen.
Göra läkemedlet mer lösligt och långsammare att skölja ut
Forskarna optimerade först hur partiklarna framställdes och finjusterade förhållandet mellan de två polymererna så att nanopartiklarna förblev små, jämnt storleksfördelade och stabila i vätska. De bekräftade att läkemedlet var väl inbäddat i polymernätverket och delvis omvandlats från en kristallin till en mer amorf form, vilket generellt löser sig bättre. I testvätskor som efterliknar magsäckens och tarmens miljö ökade nanogelformuleringen dapagliflozins upplevda löslighet med ungefär 1,7–1,8 gånger jämfört med råsubstansen. När de övervakade hur snabbt läkemedlet läckte ut visade nanogelen en mild ”långsamt frisättande” profil över flera timmar, istället för det snabba utbrott som sågs med det rena läkemedlet. Ett särskilt recept, kallat F2, bildade en kompakt, hållbar gel som höll ihop i minst två timmar i sura förhållanden samtidigt som medicinen frigjordes jämnt.
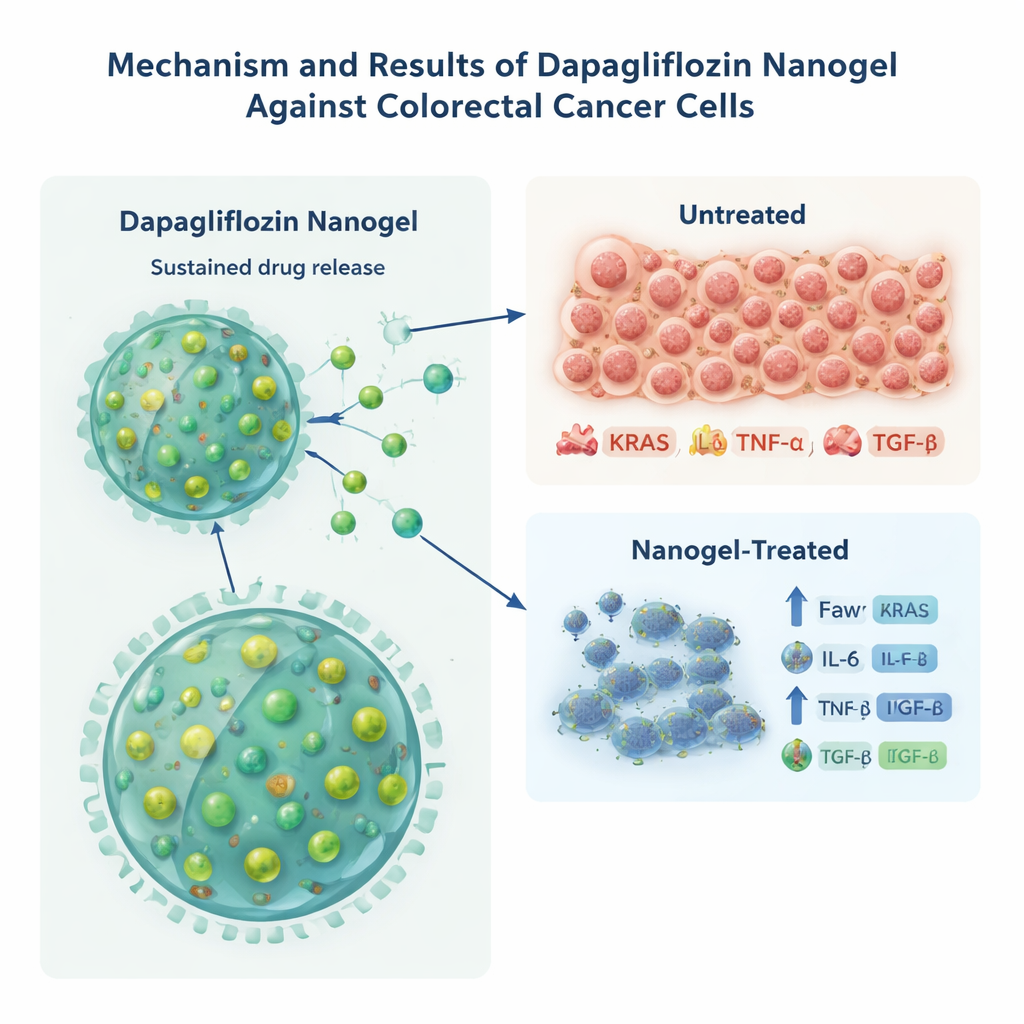
Sätta cancerceller under stress i laboratoriet
För att se om denna nya form av dapagliflozin faktiskt kunde skada cancerceller testade teamet den på HCT‑116 kolorektala cancerceller odlade i petriskålar. Jämfört med samma mängd fritt läkemedel dödade nanogelvarianten cancerceller vid lägre koncentrationer och minskade dosen som krävdes för att halvera celltillväxten med omkring en tredjedel. Forskarna undersökte sedan molekyler kopplade till aggressivt tumörbeteende och kronisk inflammation, inklusive KRAS (ett nyckelprotein som driver cancer) och signalproteinerna IL‑6, TNF‑α och TGF‑β. Celler behandlade med läkemedelsladdad nanogel visade mycket lägre nivåer av alla dessa markörer än celler behandlade med fritt läkemedel eller med tomma partiklar, vilket tyder på att den förlängda exponeringen från nanopartiklarna effektivare dämpade cancer‑ och inflammationsrelaterade signaler. Eftersom cellinjen redan bär en fast KRAS‑mutation varnar författarna att denna minskning av KRAS‑protein kan spegla stressreaktioner snarare än direkt genetisk korrigering, men det stöder ändå en stark biologisk påverkan.
Förändringar i hur kroppen hanterar läkemedlet
Teamet gick sedan vidare till djurstudier och gav råttor antingen en enkel suspension av dapagliflozinpulver eller den optimerade nanogelen, båda peroralt i samma dos. I nanogelgruppen uppträdde toppnivåerna av läkemedlet i blodet senare och lägre, men läkemedlet fanns kvar i cirkulationen längre. Den totala exponeringen (mätt som area under kurvan) ökade måttligt med ungefär 7 %, och den upplevda halveringstiden fördubblades ungefär. Dessa förändringar innebär att kroppen ser en jämnare, mer förlängd dos över tid istället för en skarp topp och snabb nedgång. Det beteendet stämmer överens med vad forskarna designade gelen för: hålla läkemedlet i tarmen, frigöra det långsamt och potentiellt bibehålla högre nivåer som sköljer över nedre tarmen och tjocktarmen där tumörer uppstår.
Vad detta kan innebära för framtida cancerbehandling
I vardagliga termer tar denna studie ett välkänt diabetesläkemedel och utrustar det med en ny ”leveransdräkt” så att det bättre når och dröjer kvar vid kolontumörer. Nanogelen gör läkemedlet lättare att lösa, bromsar dess utflöde från tarmen och verkar göra det mer toxiskt för kolorektala cancerceller samtidigt som viktiga inflammations‑ och tillväxtsignaler dämpas. Hos råttor förlänger den försiktigt läkemedlets närvaro i blodet utan att dramatiskt öka den totala dosen. Arbetet är fortfarande i ett tidigt skede — begränsat till en cellinje och kortsiktiga djurförsök — och har ännu inte visat direkt tumörminskning i levande djur eller människor. Ändå lägger det en detaljerad grund för att omdisponera dapagliflozin som en del av framtida behandlingar mot kolorektalcancer, genom att använda smarta orala nanogeler för att förvandla en välkänd tablett till ett mer målinriktat anticancerverktyg.
Citering: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Nyckelord: kolorektalcancer, Läkemedelsomdisposition, nanopartiklar, oral läkemedelsleverans, dapagliflozin