Clear Sky Science · sv
Nationomfattande genomisk övervakning av karbapenem- och kolistinresistenta Klebsiella pneumoniae-isolat från blodet i Thailand (2020–2024)
Dödliga blodinfektioner ökar
Sjukhus världen över brottas med en oroande trend: vanliga bakterier som tidigare gav efter för våra starkaste antibiotika blir nästan omöjliga att behandla. Den här studien fokuserar på Klebsiella pneumoniae, en mikroorganism som kan invadera blodomloppet och orsaka livshotande infektioner, och följer hur den har utvecklats i hela Thailand för att motstå även reservläkemedel. Att förstå var dessa superbakterier sprids och hur de undviker läkemedel är avgörande för att skydda patienter, vägleda läkarnas val och utforma folkhälsopolitik.
Spåra en sjukhussuperbakterie över ett helt land
Forskarna analyserade 227 Klebsiella pneumoniae-prover tagna från patienters blod på sjukhus runt om i Thailand mellan 2020 och 2024. Dessa prover kom från ett nationellt övervakningsnätverk som rutinmässigt samlar in data om läkemedelsresistenta infektioner. Laboratorietester visade att över 93 % av dessa blodisolat var resistenta mot karbapenemer, en kraftfull klass av antibiotika som ofta används när andra läkemedel misslyckas. Oroväckande nog var nästan en tredjedel av de karbapenemresistenta stammarna också resistenta mot kolistin, ett av de sista alternativen läkare tar till när inget annat hjälper. Genom att kombinera standardkänslighetstester med helgenomsekvensering kunde teamet se inte bara vilka läkemedel som misslyckades, utan också vilka genetiska knep bakterierna använde för att överleva.
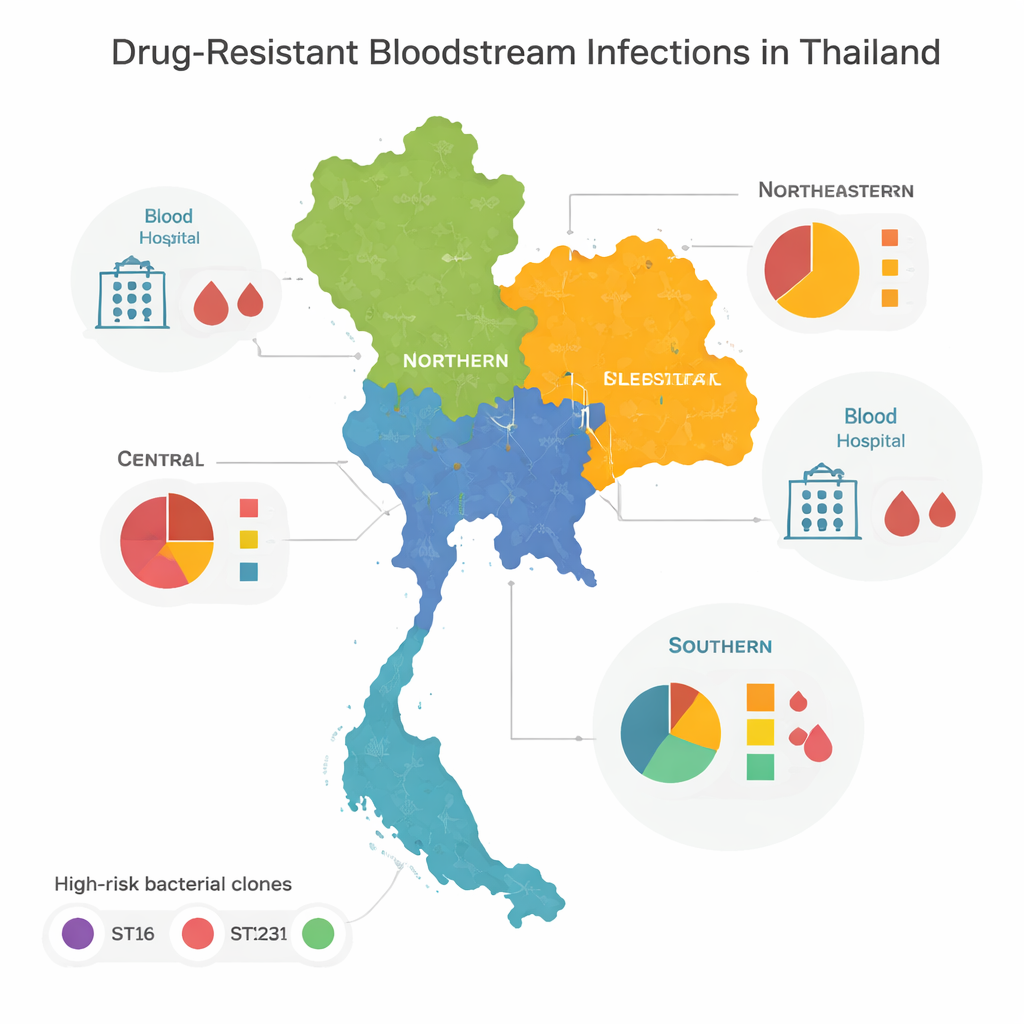
Hög-riskkloner och regionala mönster
När teamet jämförde genomerna fann de att majoriteten av de resistenta bakterierna tillhörde några få ”hög-risk”-familjer, eller kloner, som globalt är kända för att orsaka sjukhusutbrott. Tre särskilt—benämnda ST16, ST147 och ST231—dominerade i centrala, norra respektive nordöstra Thailand. Dessa kloner hade spridit sig stort över regionerna, vilket tyder på frekvent förflyttning av patienter, personal eller bakterier mellan sjukhusen. Den södra delen av landet såg annorlunda ut: istället för att domineras av ett fåtal typer rymde den ett brett spektrum av bakterielinjer, många som sågs bara en gång. Denna mångfald antyder en mer komplex blandning av lokala utbrott, miljökällor och rörelser över gränser snarare än en eller två dominerande kloner.
Hur bakterierna överlistar antibiotika
Studien visade hur dessa bakterier staplar flera resistensmekanismer på varandra. Många ST16- och ST231-stammar bar på gener kända som blaNDM och blaOXA, som producerar enzymer som bryter ner karbapenemantibiotika innan de kan verka. Vissa hade också förändringar i sitt yttre membran som minskar läkemedelsinträde, i kombination vilket skapar mycket hög nivå av resistens. ST231-stammar bar ofta ytterligare en gen, rmtF1, som blockerar en viktig grupp läkemedel kallade aminoglykosider och därigenom ytterligare begränsar behandlingsalternativen. ST147 utmärkte sig för sin genetiska flexibilitet: den kombinerade olika resistensgener och plasmider — små, mobila DNA–ringar — vilket gör den till en potentiell nav för spridning av resistensegenskaper till andra bakterier.
Sista linjens misslyckanden och dolda faror
Det mest oroande fyndet rörde resistens mot kolistin, ett läkemedel som läkare reserverar för desperata situationer. Några sällsynta bakteriefamiljer bar mcr-gener, som kan hoppa mellan arter på plasmider och direkt orsaka kolistinresistens. Andra, särskilt inom ST16-klonen, var resistenta mot kolistin även om de saknade kända resistensgener eller mutationer. Detta tyder på att forskarna ännu inte helt kartlagt alla sätt bakterier kan neutralisera detta sista försvarsläkemedel. Teamet identifierade också hypervirulenta stammar — bakterier som är särskilt bra på att orsaka allvarlig sjukdom — inklusive en linje som kombinerade hög virulens med resistens mot alla testade karbapenemer, en särskilt farlig kombination.
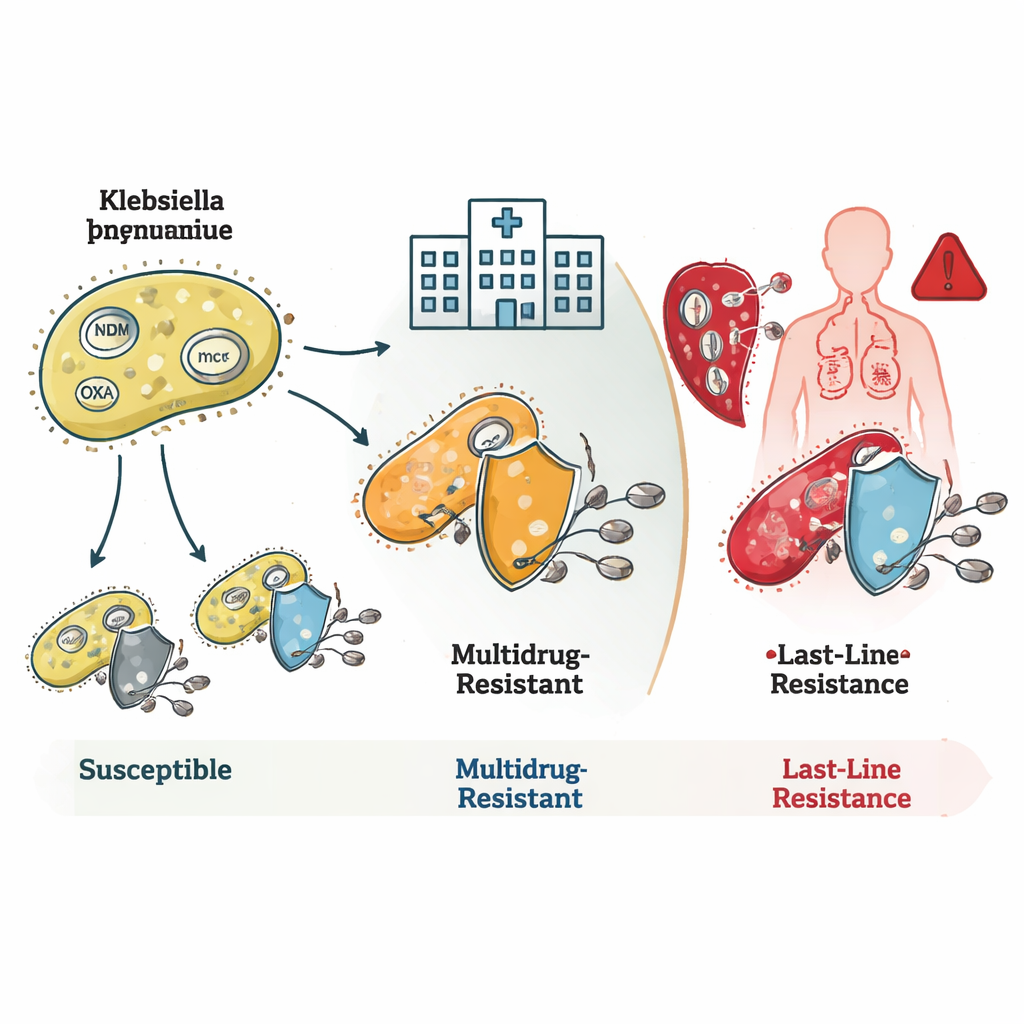
Varför genomisk övervakning spelar roll
För att förstå hur genetiska förändringar översattes till verkliga behandlingsmisslyckanden använde forskarna statistiska modeller för att koppla specifika resistensgener till faktiska labbtestresultat. Gener såsom blaNDM-1 och dess nära släktingar visade extremt starka samband med karbapenemresistens, vilket bekräftar deras centrala roll i att driva behandlingssvikt. För kolistin hade dock de flesta resistenta bakterier inga erkända resistensmarkörer, vilket pekar på dolda mekanismer som fortfarande måste upptäckas. Författarna argumenterar för att rutinmässig användning av helgenomsekvensering i sjukhusövervakning kan fungera som en tidig varningsradar—upptäcka framväxande hög-risk-kloner, spåra deras rörelse över regioner och gränser och vägleda snabba åtgärder för infektionskontroll.
Vad detta betyder för patienter och politik
För en lekmannaläsare är budskapet tydligt men allvarligt: vissa blodinfektioner i Thailand orsakas nu av bakterier som är motståndskraftiga mot nästan alla läkemedel som läkare kan använda, och några få farliga familjer av dessa mikrober sprider sig i stor skala. Samtidigt visar studien att med rätt verktyg — nationell provtagning, genetisk analys och snabb datadelning — kan vårdsystem upptäcka dessa hot i förväg och anpassa sig. Att utöka genomisk övervakning, utveckla snabba molekylära tester och skärpa infektionskontrollen kan hjälpa till att bromsa framfarten av dessa superbakterier och vinna tid för utveckling av nya behandlingar och vaccin.
Citering: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Nyckelord: antimikrobiell resistens, Klebsiella pneumoniae, blodströmsinfektion, genomisk övervakning, Thailands sjukvård