Clear Sky Science · sv
FcIgG-GE11-Melittin som en ny EGFR-riktad peptibody med potent cytotoxisk aktivitet mot cancerceller
Binngift möter precisionsbehandling mot cancer
Många lovande cancerläkemedel är helt enkelt för hårda mot resten av kroppen för att kunna användas säkert. Ett slående exempel är melittin, huvudtoxinet i binngift: det kan slita sönder cancerceller, men det kan också skada röda blodkroppar och frisk vävnad. Denna studie undersöker en smart lösning — att bygga ett ”styrt missil”-system som för melittin direkt till tumörceller som uttrycker en specifik ytmolekyl, samtidigt som normala celler i stor utsträckning besparas.
Varför rikta in sig på en vanlig cancerregulator
En viktig aktör i många tumörer är epidermal tillväxtfaktorreceptorn, eller EGFR. Denna receptor sitter på cellers yta och hjälper till att kontrollera tillväxt och överlevnad. I flera cancerformer — inklusive lung-, kolorektal-, prostatacancer samt vissa huvud‑hals‑ och njurcancerformer — överproduceras EGFR och driver okontrollerad celldelning. På grund av detta har läkemedel som binder EGFR blivit en viktig klass av riktade terapier. Existerande EGFR-läkemedel blockerar dock främst signalering; de skapar inte aktivt hål i cancercellerna. Forskarna frågade sig om de kunde utnyttja melittins kraftfulla celllyserande förmåga och leverera det selektivt till EGFR‑rika tumörceller.
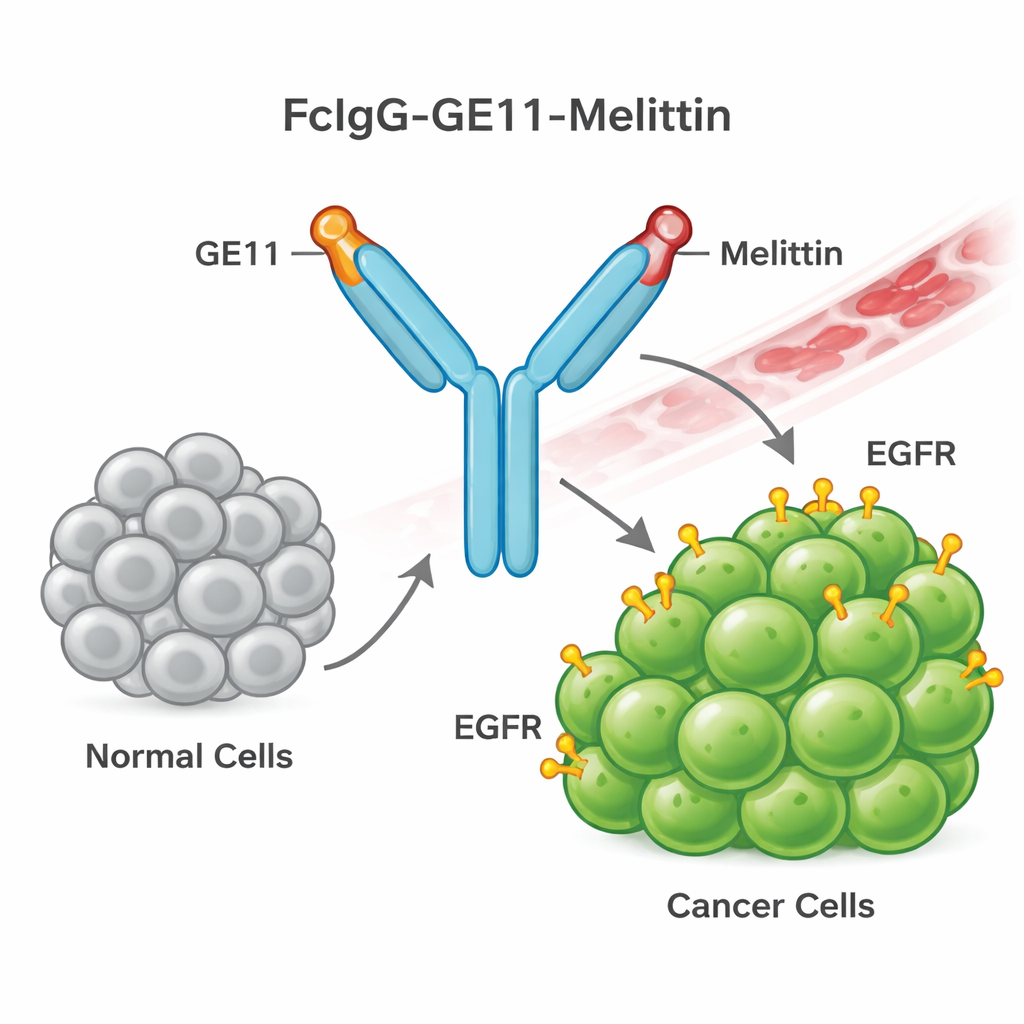
Att bygga ett riktat binngiftsvapen
För detta designade teamet ett nytt fusionsprotein som de kallar FcIgG-GE11-Melittin. Det kombinerar tre delar: en antikropps"svans" (Fc‑regionen av human IgG) som förbättrar stabiliteten i blodomloppet och förenklar rening; en kort styrpeptid kallad GE11 som känner igen och binder EGFR på cancerceller; och melittin, binngiftets peptid som kan rupturera cellmembran. Bakterier konstruerades för att producera detta fusionsprotein i stora mängder. Proteinet fick sedan genomgå refolding och rening, och laboratorietester bekräftade att det bildade den förväntade dimeriska formen och bar den humana antikroppsflaggan, vilket visar att konstruktionen byggts korrekt.
Fäster vid tumörceller, inte bara vilken cell som helst
Nästa fråga var om denna designade molekyl verkligen hittar och fäster vid EGFR‑rika cancerceller. Med hjälp av flödescytometri testade författarna bindning på A549‑lungcancerceller, som är kända för att överuttrycka EGFR. Celler behandlade med FcIgG-GE11-Melittin visade en kraftig ökning i fluorescens, vilket indikerar att många fusionsmolekyler hade fäst vid deras yta. En orelaterad peptibody, Romiplostim, visade nästan ingen bindning och fungerade som negativ kontroll. Den nya konstruktens bindningsprofil överensstämde väl med Cetuximab, en välkänd EGFR‑antikropp, vilket stödjer idén att GE11‑komponenten korrekt styr fusionsproteinet till dess mål.
Dödar cancerceller samtidigt som blodceller skonas
Teamet testade sedan hur väl fusionsproteinet kunde döda olika cancercellinjer i kultur. Fritt melittin var extremt potent men oskiljaktigt, och minskade cellsurvival kraftigt redan vid låga doser i lung‑ (A549), prostata‑ (DU145) och kolorektal‑ (SW480) cancerceller. I kontrast visade FcIgG-GE11-Melittin dosberoende dödlighet som var starkast i EGFR‑positiva celler, medan en EGFR‑fattig bröstcancerlinje (MDA‑MB‑453) var relativt resistent. Detta mönster tyder på att fusionskonstruktets angrepp beror på EGFR‑riktning snarare än slumpmässig membranskada. Viktigast av allt, i experiment med mänskliga röda blodkroppar orsakade fritt melittin nästan fullständig hemolys vid måttliga doser, medan fusionsproteinet gav mindre än 5 % hemolys även vid mycket höga koncentrationer. Med andra ord reducerade kopplingen av melittin till den EGFR‑sökande bärare dramatiskt dess benägenhet att spränga röda blodkroppar.
Vad detta kan innebära för framtidens cancervård
Sammanfattningsvis visar arbetet att koppling av ett potent membranstörande toxin som melittin till ett precist riktingssystem kan förvandla det från ett brett toxiskt ämne till ett mer tumörselektivt vapen. FcIgG-GE11-Melittin binder starkt till EGFR‑överuttryckande cancerceller, dödar dem på ett kontrollerat, dosberoende sätt och visar minimal skada på röda blodkroppar i laboratoriet. Även om ytterligare djurstudier och säkerhetstester krävs innan någon användning hos patienter är möjlig, illustrerar denna strategi hur omformning av naturliga toxiner till styrda terapier skulle kunna öppna nya vägar för att behandla EGFR‑positiva cancerformer mer effektivt och med färre biverkningar.
Citering: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Nyckelord: riktad cancerbehandling, EGFR, bivensmelittin, peptibody, tumörselektiva toxiner