Clear Sky Science · sv
R5- och R7-positioner på fluorkinolonskelett driver störningar i F-aktinfilament
Att förvandla antibiotika till hjärnhjälpare
Många vanliga hjärnsjukdomar, från Alzheimers till Parkinsons sjukdom, delar en dold syndabock: små strukturella stavar inne i nervceller som med tiden fastnar och blir styva. Dessa stavar består av ett protein som kallas aktin, normalt en flexibel del av cellens inre stomme. Denna studie undersöker en överraskande möjlighet — att en välkänd klass av antibiotika, fluorkinoloner, skulle kunna omdesignas för att varsamt bryta upp dessa skadliga aktinbundter och potentiellt hjälpa till att skydda hjärnan.
När cellens stomme går fel
Hälsosamma hjärnceller omformer ständigt sitt inre skelett för att bilda och ombilda kopplingar. Aktinfilament är centrala i denna process, bildas och löses upp efter behov. Under stress kan dock aktin låsa sig i envisa, stavliknande aggregat som täpper igen cellen, stör transporten av livsviktigt gods och främjar ansamling av sjukdomsassocierade proteiner såsom amyloid och tau. Över år kan dessa stavar mogna till täta strukturer kända som Hirano-kroppar, vilka ofta observeras i hjärnor hos personer med flera neurodegenerativa tillstånd. Eftersom befintliga läkemedel som riktar sig mot aktin ofta är extremt giftiga, är forskare angelägna om att hitta säkrare småmolekyler som kan luckra upp dessa aggregat utan att skada cellerna.
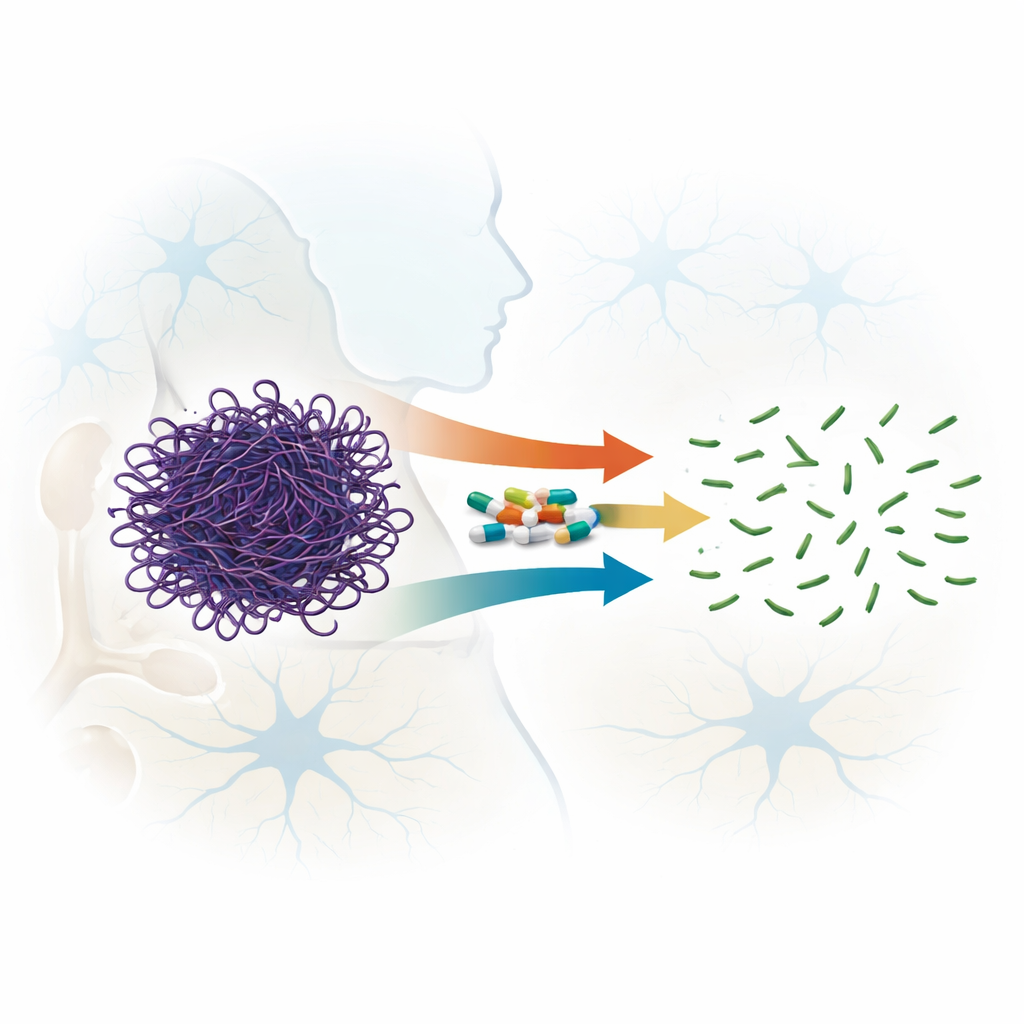
En oväntad talang hos välbekanta läkemedel
Fluorkinoloner är bredspektrumantibiotika som används globalt för att behandla infektioner, och några nyare medlemmar i denna familj kan korsa blod-hjärnbarriären. Tidigare antydningar föreslog att vissa fluorkinoloner kan destabilisera aktinfilament. I detta arbete jämförde författarna systematiskt sju besläktade föreningar, över fyra generationer av läkemedelsfamiljen, för att se hur väl de bryter isär redan bildade aktinfilament snarare än att enbart förhindra deras bildning. Genom ljusspridningsmätningar, elektronmikroskopi och gelfiltrering visade de att alla testade läkemedel kunde störa aktinfilament, men med mycket olika styrka. Två läkemedel, sparfloxacin (en tredje generationens förening) och moxifloxacin (fjärde generationen), utmärkte sig genom att snabbt och irreversibelt hugga långa filament i betydligt mindre bitar, även vid relativt låga läkemedel-till-protein-förhållanden.
Att se filament falla isär
Högupplöst avbildning och biofysiska tester avslöjade hur filamenten förändras vid läkemedelsbehandling. Elektronmikroskopi visade att obehandlat aktin bildar långa, kontinuerliga strängar, medan effektiva fluorkinoloner omvandlar dessa till korta, spridda fragment. Mindre potenta medlemmar gav upphov till vinklade och böjda filament men bröt dem inte helt. Värmebaserade mätningar av proteinstabilitet bekräftade denna fysiska störning: en gång behandlat betedde sig aktin mer som sin fria, oassemblerade form, med lägre smälttemperaturer, men dess grundläggande byggstenstruktur förblev nästan oförändrad. Det tyder på att läkemedlen inte vecklar ut eller skadar aktin i sig — de skruvar främst upp hur enheterna fäster vid varandra i filamenten.
Inzoomning på det molekylära greppet
För att förstå varför vissa fluorkinoloner fungerar bättre än andra kombinerade teamet avancerade nukleärmagnetisk resonansexperiment med datorsimuleringar av läkemedels–proteininteraktioner. De fann att alla föreningar förlitade sig på en gemensam ringformad ”kärna” för att göra kontakt med aktin, särskilt vid två positioner på den kärnan som upprepade gånger berör filamentet. Extra kemiska grupper som är fästa vid specifika platser — kallade R5 och R7 — påverkar dock starkt hur fasta och var varje molekyl binder. I de mest effektiva disruptorerna bär dessa positioner en aminogrupp och skrymmande ringsystem som når in i en liten ficka vid gränssnittet mellan intilliggande aktinsträngar. Där stör de nyckelkontakter som stabiliserar filamenten, inklusive en viktig saltbrygga som normalt hjälper till att hålla filamenten samman.
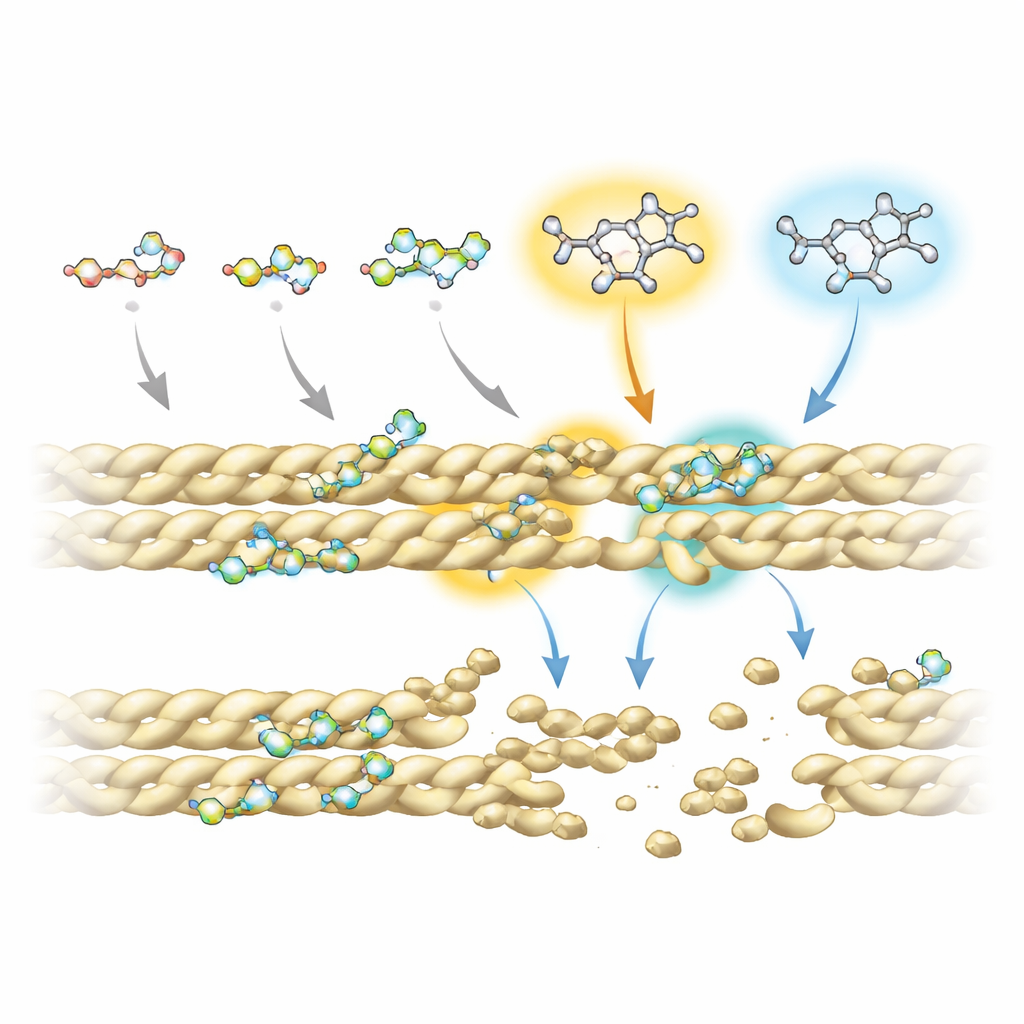
Från jästceller till framtida terapier
Forskarna testade också läkemedlen i en jäststam som naturligt ackumulerar aktinbundter, vilket efterliknar aspekter av sjuka celler. Under mikroskopet visade obehandlad jäst stora, ljusa aktinkluster, medan celler exponerade för fluorkinoloner — särskilt sparfloxacin, moxifloxacin och, vid högre doser, nalidixinsyra — uppvisade mycket mer diffusa, punktlika mönster, vilket indikerar att bundten hade brutits ned. Viktigt är att läkemedlens verkan verkade relativt mild: de försvagade filamentpackningen utan att grovt förvränga aktins underliggande form, och deras bindning var svagare än klassiska aktintoxiner, vilket potentiellt minskar risken för svåra biverkningar.
Att designa smartare aktinriktade läkemedel
Sammanfattningsvis visar denna studie att små justeringar av välkända antibiotika dramatiskt kan förändra hur de interagerar med cellens inre stomme. Genom att peka ut R5- och R7-positionerna som nyckelns ”reglage” för både aktinstörning och hjärnpenetration, skisserar författarna en ritning för att skapa nya fluorkinolon-inspirerade molekyler som selektivt demonterar skadliga aktinaggregat. Även om dessa fynd är ett tidigt laboratoriebevis för principen, öppnar de för möjligheten att framtida läkemedel härledda från välkända antibiotika skulle kunna hjälpa till att rensa toxisk stomme i nervceller och bromsa eller förebygga vissa former av neurodegeneration.
Citering: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Nyckelord: aktinaggregat, fluorkinolonantibiotika, neurodegenerativ sjukdom, omdisponering av läkemedel, cytoskelett