Clear Sky Science · sv
Cellulära åldringsrelaterade geners roll vid ischemia–reperfusion‑skada och identifiering av deras markörer
Varför hjärtskadan kan förvärras när blodet återvänder
När någon får en hjärtinfarkt eller genomgår hjärtkirurgi kämpar läkare för att snabbt återställa blodflödet till den svältande hjärtmuskeln. Paradoxalt nog kan just det livräddande steget själv orsaka ytterligare skada — ett problem som kallas ischemia–reperfusion‑skada. Denna studie undersöker varför vissa hjärtceller reagerar så illa när blodet återvänder, med fokus på biologin bakom cellulärt åldrande och identifiering av ett litet antal gener som kan hjälpa läkare att upptäcka och så småningom behandla denna dolda skada mer precist.
När räddningen blir förnyad skada
Ischemia–reperfusion‑skada sker i två akter. Först blockeras en kranskärl och hjärtvävnaden svälter av syrebrist (ischemi). När blockeringen sedan avlägsnas och blodet sköljer tillbaka (reperfusion) kan en våg av reaktiva molekyler och inflammation skada redan sköra celler. Nuvarande verktyg — såsom EKG, avbildning och blodprov för proteiner som troponin — missar ofta tidig eller subtil skada och kan inte lätt förutsäga vem som får långsiktiga problem. Denna lucka har fått forskare att söka djupare, till de molekylära händelserna inne i hjärtcellerna själva.
Cellulärt åldrande som en dold drivkraft
Forskarnas fokus ligger på cellulär senescens, ett tillstånd där celler upphör att dela sig permanent och antar ett ”larmskickande” beteende. Senescenta hjärtceller utsöndrar en blandning av inflammatoriska molekyler och enzymer kända som det senescens‑associerade sekretoriska fenomenet. Detta kemiska moln kan förvärra ärrbildning, locka immunceller och störa vävnadsreparation, och skapa en ond cirkel av skada och kronisk dysfunktion. Genom att granska offentliga genuttrycksdatabaser från mushjärtan utsatta för ischemia–reperfusion och korsreferera dem med hundratals gener kopplade till cellulärt åldrande, avgränsade teamet fältet till 26 gener som ändrar sig markant efter skada.
Sexton gener som bildar ett diagnostiskt fingeravtryck
För att hitta de mest informativa signalerna bland dessa 26 gener använde forskarna flera maskininlärningsmetoder. Dessa algoritmer söker efter kombinationer av gener som bäst skiljer skadade hjärtan från friska. Efter logistisk regression, LASSO och analys med supportvektormaskiner framträdde sex gener som ett kraftfullt diagnostiskt panel: CDKN2B, ID1, STAT3, TERF2, TP53 och ZNF277. Tillsammans kunde deras aktivitetsmönster identifiera ischemia–reperfusion‑skada med mycket hög noggrannhet i de kombinerade databaserna och överträffade många traditionella blodmarkörer i interna tester. Gen‑till‑väg‑analys knöt dessa markörer till stressrespons‑kretsar som involverar oxidativ skada, celldödsprogram och välkända signalvägar som MAPK och PI3K–AKT — alla faktorer som avgör om en cell återhämtar sig eller glider in i permanent senescens.
Hur immunsystemet går med i berättelsen
Skada som uppstår när blodflödet återställs sker inte isolerat; immunceller strömmar snabbt in i hjärtat. Genom att uppskatta immuncellsaktivitet från samma genuttrycksdata hittade studien tydliga tecken på ökat immunsvar i skadade hjärtan, inklusive flera typer av T‑celler, B‑celler, makrofager och mastceller. En åldringsrelaterad gen, CDKN2B, korrelerade starkt med ”central memory” CD4‑T‑celler, medan TP53 korrelerade med aktiverade mastceller. Dessa kopplingar tyder på att åldringsvägar i hjärtceller och förändringar i immunsystemet förstärker varandra: celler som agerar åldrade kallar på immun hjälp, och dessa immunsvar kan i sin tur fördjupa skada och ärrbildning.
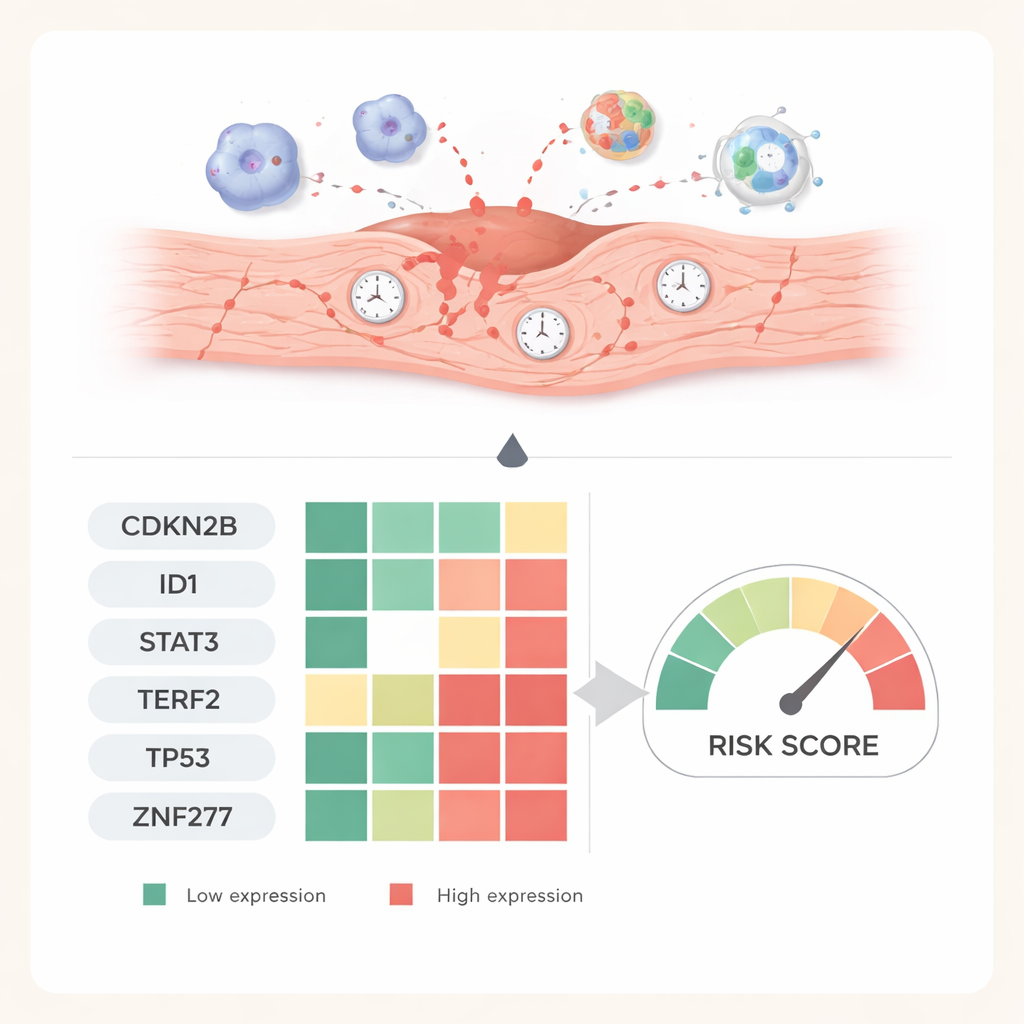
Från datorprediktioner till levande hjärtan
För att testa om dessa sex gener spelar roll bortom datorskärmar skapade forskarna en musmodell för ischemia–reperfusion‑skada. De mätte genaktivitet vid olika tidpunkter efter att blodflödet återställts och använde vävnadsfärgning för att visualisera motsvarande proteiner i hjärtskivor. En gen, CDKN2B, ökade stadigt under en vecka, vilket antyder att den bidrar till att låsa skadade celler i ett långvarigt senescent tillstånd. Andra, inklusive ID1, STAT3, TP53, TERF2 och ZNF277, sjönk kraftigt tidigt och återhämtade sig sedan gradvis, vilket speglar skiftningar mellan akut stress, aktiv skada och senare reparation. Dessa tidsberoende mönster stöder idén att varje gen fångar en annan fas i hjärtats respons.
Vad detta kan innebära för patienter
För en lekman är huvudbudskapet att studien kopplar hjärtinfarkt‑relaterad skada till biologin bakom cellulärt åldrande och identifierar ett sex‑geners ”fingeravtryck” som flaggar denna skada i experimentella modeller. Även om arbetet fortfarande är prekliniskt och huvudsakligen baserat på musdata och offentliga databaser, erbjuder det en vägkarta för nya blod‑ eller vävnadstester som skulle kunna upptäcka ischemia–reperfusion‑skada tidigare och mer specifikt än dagens verktyg. På längre sikt kan förståelsen av hur dessa åldringsrelaterade gener styr inflammation, ärrbildning och reparation öppna dörrar för behandlingar som inte bara återöppnar tilltäppta artärer, utan också hjälper det återuppväckta hjärtat att läka mer fullständigt.
Citering: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
Nyckelord: ischemi reperfusionsskada, cellulär senescens, hjärtinfarkt, biomarkörer, immuninflammation