Clear Sky Science · sv
ACE2‑uttryck i kolonepitelceller är kopplat till virusinfektion, immunitet och energimetabolism
Varför tarmen spelar roll vid ett luftvägsvirus
När vi tänker på COVID‑19 föreställer vi oss lungor som fylls med vätska och patienter som har svårt att andas. Ändå utvecklar många som smittas med SARS‑CoV‑2 också magont, diarré och långvariga tarmproblem. Denna studie undersöker varför tarmarna—särskilt tjocktarmen—kan vara ett viktigt mål för viruset. Genom att zooma in på enskilda celler från barns kolon visar forskarna att en nyckel‑infart för viruset, proteinet ACE2, är mycket aktivt i specifika tarmceller och kopplat inte bara till viral infektion utan också till vårt immunförsvar och hur celler hanterar energi.
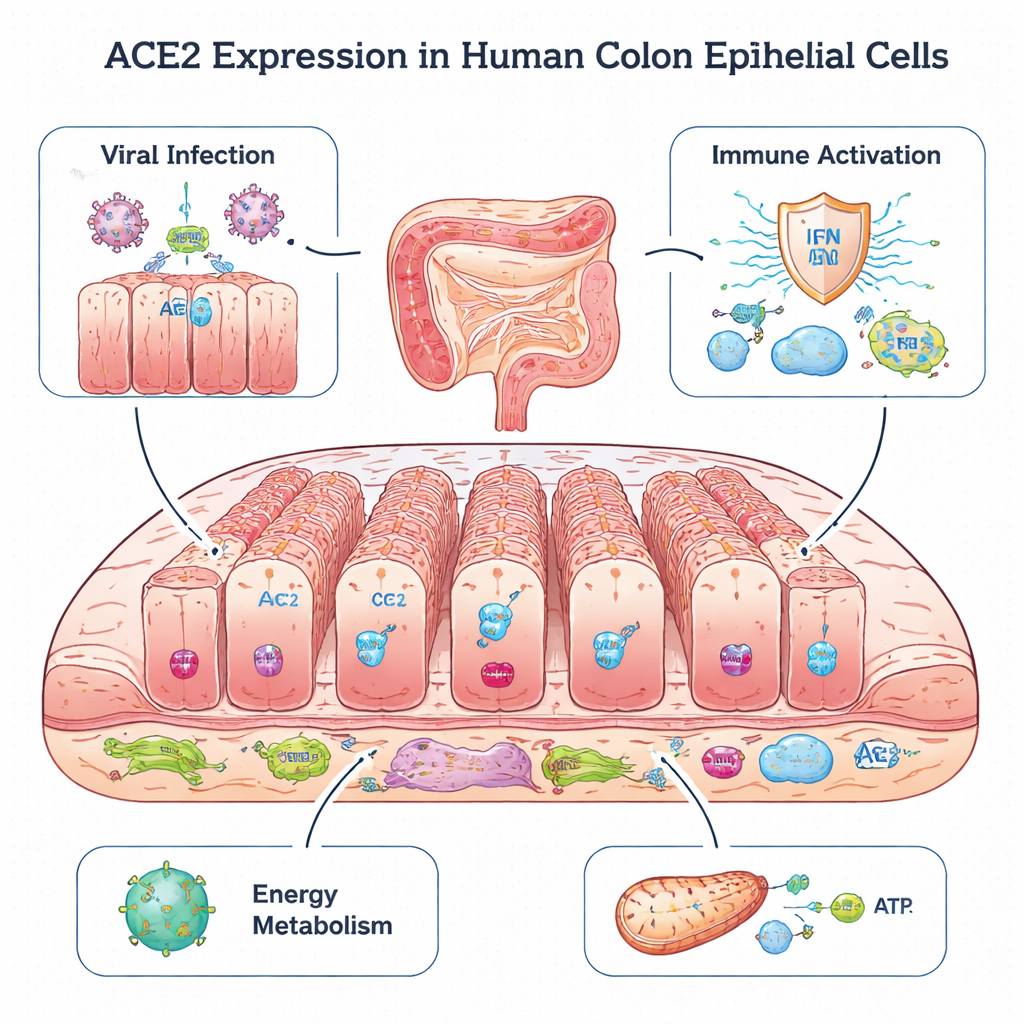
En cellulär dörr i tjocktarmen
ACE2 är mest känt som huvudporten som både det ursprungliga SARS‑viruset och SARS‑CoV‑2 använder för att infectera celler i lungan. Paradoxalt nog tyder djurstudier på att ACE2 också kan skydda vävnader från skada genom att hjälpa till att hålla ett hormonsystem som kontrollerar blodtryck i balans. I tarmen är det redan känt att ACE2 stödjer en hälsosam mikrobiota och förebygger inflammation. I detta arbete återanalyserade forskarna single‑cell RNA‑sekvenseringsdata från kolonbiopsier från 17 barn: vissa hade friska tarmar, medan andra hade kolit eller inflammatorisk tarmsjukdom, inklusive ulcerös kolit och Crohns sjukdom. Denna teknik gjorde det möjligt att se vilka gener som är aktiva i tusentals enskilda celler och att exakt lokalisera var ACE2 är påslaget.
Kolonocyter: primära mål och första försvarare
Analysen visade att ACE2 är koncentrerat nästan uteslutande till kolonocyter, en huvudsaklig typ av epitelcell som bekläder insidan av tjocktarmen och vetter mot tarminnehållet. Jämfört med andra epitelceller visade kolonocyter också högre aktivitet i gener som hjälper virus att tränga in i celler, knoppa av och lämna cellen. Samtidigt uttryckte dessa celler många gener som är involverade i att känna igen viral genetisk information och trigga typ I‑ och typ III‑interferon‑svar—viktiga tidiga larmsystem i immunförsvaret. De producerade också inflammatoriska signaler och molekyler som presenterar virusfragment för T‑celler, vilket tyder på att kolonocyter både är potentiella virala mål och viktiga tidiga väktare som varnar immunsystemet.
Kopplade nätverk för immunitet och energianvändning
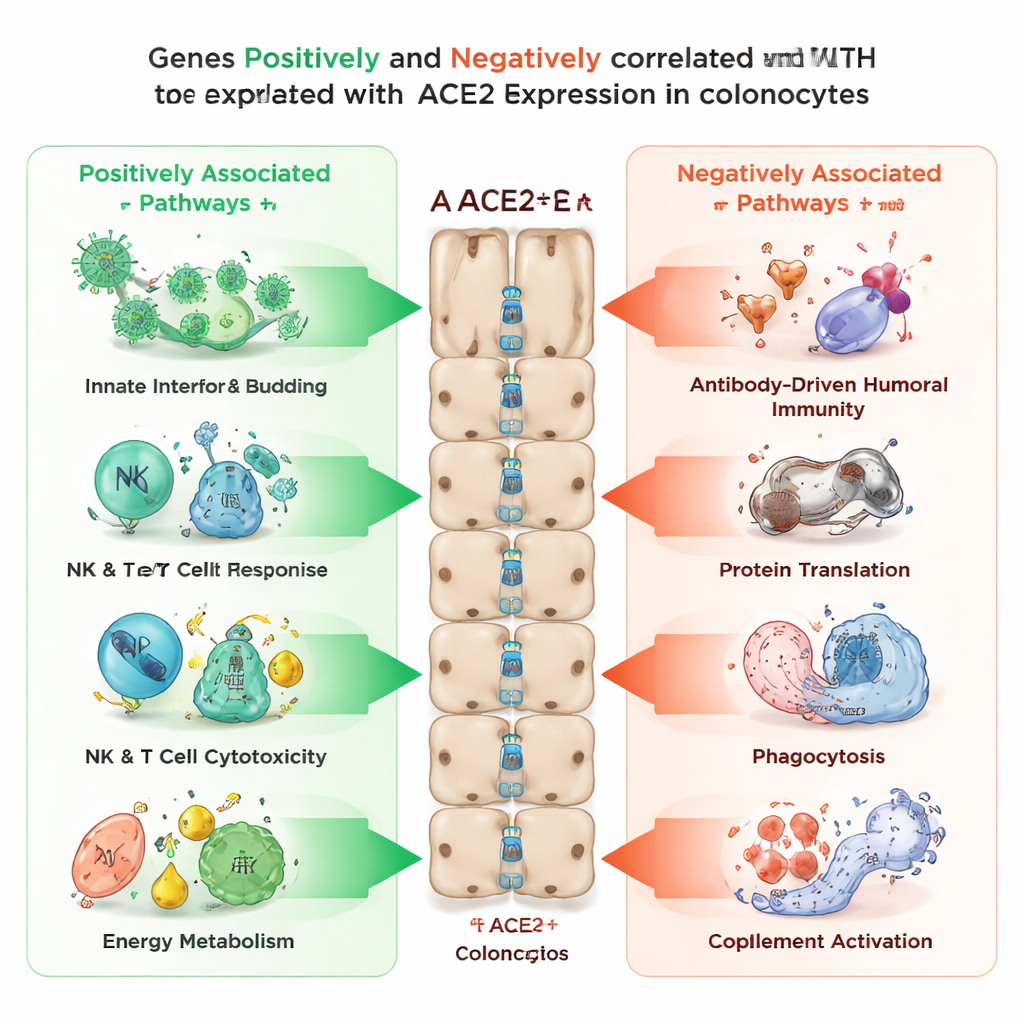
Forskarna undersökte sedan vilka andra gener som tenderar att vara påslagna eller avstängda i samklang med ACE2 i kolonocyter. De fann över 3 400 gener som ökade med ACE2‑nivåer och mer än 2 100 som sjönk när ACE2 ökade. Gener som följde positivt med ACE2 var berikade i processer relaterade till viral inträde och frisättning, medfödd immunsignalering, natural killer‑cellers och T‑cellers dödande aktivitet, samt flera energiproducerande vägar inne i cellerna, inklusive mitokondriell funktion och bearbetning av fetter och socker. I kontrast var gener som rörde sig i motsatt riktning—höga när ACE2 var lågt—kopplade till antikroppsbaserad (humoral) immunitet, cellens proteintillverkning, cell‑ätande processer såsom fagocytos och komplementsystemet, en annan gren av immunförsvaret. Detta mönster tyder på att ACE2 markerar ett tillstånd där kolonocyter är inställda på snabb antiviral igenkänning och energiproduktion, medan andra, långsammare immunsprogram är nedreglerade.
Bevis från inflammerade tarmar
För att kontrollera att dessa mönster verkligen förekommer i vävnader använde teamet multiplex immunofluorescens—en teknik som belyser specifika proteiner med olika färger—på kolonprover från barn med ulcerös kolit, Crohns sjukdom och från kontroller. De bekräftade att ACE2‑protein sitter huvudsakligen på epitelceller markerade med EPCAM. Hos patienter med inflammatorisk tarmsjukdom visade ACE2‑positiva celler högre nivåer av IFNA4 och RSAD2, två proteiner starkt förknippade med interferonsignalering och antiviral aktivitet. Detta indikerar att i den inflammerade tarmen är ACE2‑bärande kolonceller inte bara potentiella ingångar för virus; de är också hotspotar för antiviralt svar.
Vad detta betyder för patienter och framtida terapier
För icke‑specialister är budskapet att tjocktarmen inte är en passiv åskådare vid COVID‑19. Samma protein som låter viruset komma in i celler hjälper också till att samordna tarmens immunitet och energianvändning, särskilt hos barn med redan existerande tarminflammation. Denna dubbla roll kan bidra till att förklara varför vissa patienter utvecklar gastrointestinala symtom och varför personer med inflammatorisk tarmsjukdom har komplexa, men inte entydigt sämre, utfall vid COVID‑19. Arbetet bidrar också till bredare diskussioner om läkemedel som verkar på koagulations‑ och blodtrycksbanor, några av vilka kan minska lung‑ och kärlskador vid svår infektion. Även om studien bygger på korrelationer och inte kan bevisa orsakssamband, lyfter den fram ACE2‑rika kolonceller som viktiga aktörer i skärningspunkten mellan viral inträde, immunförsvar och metabolism—vilket pekar på tarmen som en nyckelspelare och potentiellt behandlingsbar arena i coronavirussjukdomen.
Citering: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Nyckelord: ACE2, kolonocyter, COVID-19 tarm, inflammatorisk tarmsjukdom, antiviral immunitet