Clear Sky Science · sv
Alzheimers relaterad demenssvårighetsklassificering från magnetisk resonansavbildning med derivatfri optimering av konvolutionellt neuralt nätverk
Hjälpa läkare att upptäcka demens tidigare
När befolkningar åldras oroar sig många familjer för minnesförlust och demens. Hjärnavbildningar kan visa tidiga förändringar kopplade till Alzheimers sjukdom, men att läsa tusentals bilder för hand är långsamt och svårt, även för experter. Denna studie presenterar ett smart datorverktyg som granskar MRI-bilder av hjärnan och placerar personer i fyra nivåer av demenssvårighet, från ingen demens till måttlig påverkan. Systemet är utformat för att vara både mycket noggrant och tillräckligt lätt för att köras på vanliga sjukhusdatorer, vilket gör avancerad bildanalys mer tillgänglig.
En ny smart hjälp för hjärnavbildning
Forskarna fokuserar på en typ av artificiell intelligens kallad konvolutionellt neuralt nätverk, eller CNN, som är särskilt bra på att upptäcka mönster i bilder. Istället för att bara avgöra om någon har Alzheimers sjukdom skiljer deras verktyg mellan fyra stadier: icke-demens, mycket mild, mild och måttlig demens. För att åstadkomma detta tränade teamet sin modell på stora offentliga samlingar av MRI-skanningar som redan hade märkts upp av experter. Målet var dubbelt: att uppnå nära perfekt noggrannhet och att hålla modellen kompakt och snabb, så att den kan vara praktisk för vardaglig klinisk användning snarare än enbart för välfinansierade forskningslaboratorier.
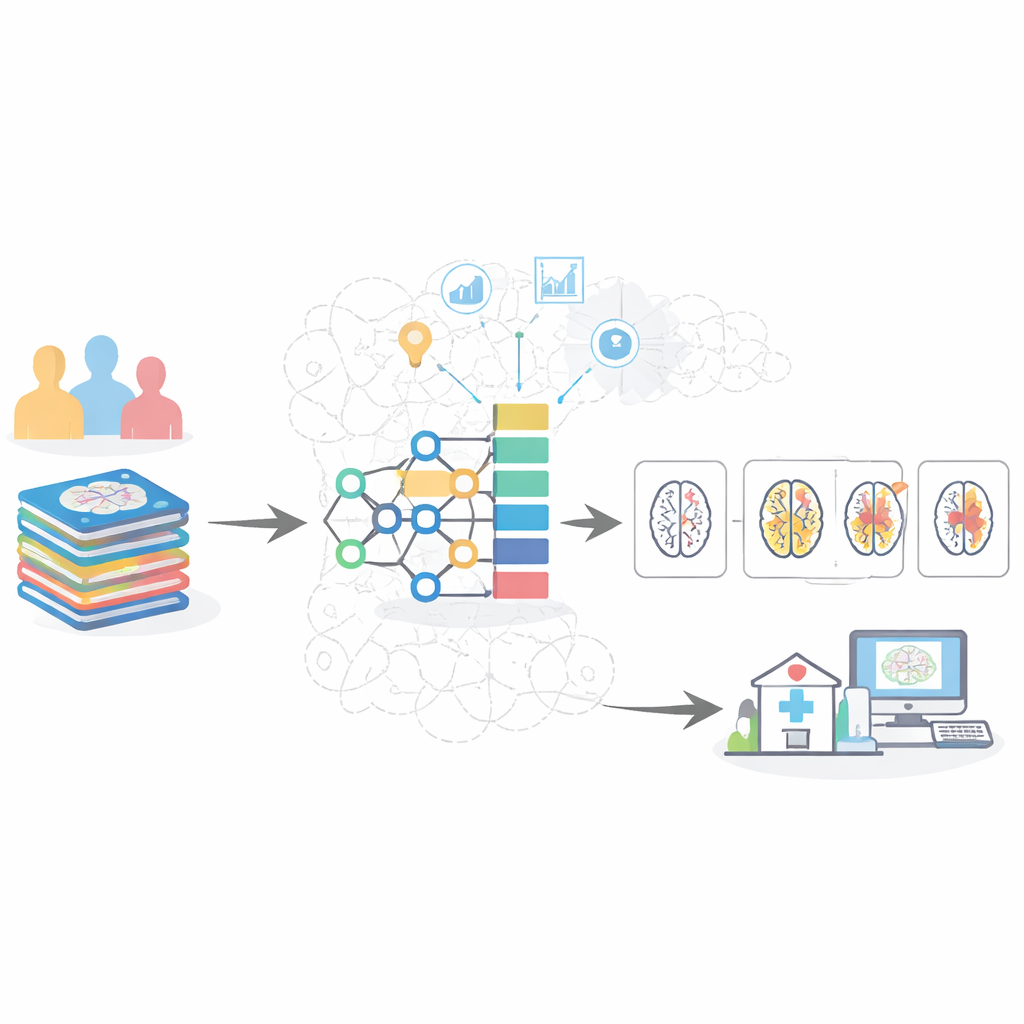
Balansera data och rensa bilderna
En central utmaning i medicinska data är att inte alla sjukdomsstadier är lika väl representerade. I dessa hjärnskanningssamlingar är friska och mycket milda fall vanliga, medan skanningar med måttlig demens är mycket mer sällsynta. Standard-AI-system tenderar då att "spela säkert" genom att överprediktera de vanliga klasserna och missa tidig eller måttlig sjukdom. För att motverka detta använde författarna en tvåstegsstrategi: de tog först bort förvirrande gränsfallsbilder och skapade därefter realistiska syntetiska exempel för de underrepresenterade stadierna. Parallellt förberedde de varje MRI-snitt noggrant genom filtrering, isolering av hjärnan från omgivande vävnad samt normalisering av ljusstyrka och kontrast så att modellen kunde fokusera på medicinskt meningsfulla kännetecken såsom krympning av djupa minnesstrukturer och vidgning av vätskefyllda utrymmen.
Utforma ett mindre, smartare nätverk
I stället för att förlita sig på traditionella träningsmetoder som finjusterar parametrar genom att följa matematiska gradienter använde teamet en grupp så kallade derivatfria optimeringstekniker. De började med ett större, konventionellt CNN och använde sedan evolutionär sökning och neural arkitektursökning för att utveckla en enklare design med endast tre konvolutionella lager och betydligt färre filter. Bayesiansk optimering finjusterade hur nätverket skulle tränas, medan simulerad glödgning och beskärning tog bort onödiga förbindelser efter träning. Slutresultatet, kallat DAPA-CNN, har ungefär 85 % färre justerbara parametrar än startmodellen, använder ungefär en fjärdedel av minnet och tränar på mindre än två tredjedelar av tiden, samtidigt som det fortfarande fångar de avgörande mönstren i skanningarna.
Nästan perfekt prestanda och tydliga visuella förklaringar
Trots sin mindre storlek visade sig DAPA-CNN vara anmärkningsvärt exakt. På en stor Alzheimersdatabas klassificerade den demensstadiet korrekt i nästan varje fall, med noggrannhet och andra prestandamått runt 99 %. Modellen generaliserade också väl till en separat multicentersamling insamlad på olika skannrar, vilket tyder på att den är robust mot verkliga variationer i avbildning. För att göra systemet mer transparent för kliniker genererade författarna class activation maps — värme-liknande överlägg som visar vilka områden av hjärnan som påverkade ett visst beslut. I tidiga stadier betonar dessa kartor områden involverade i minne som är kända för att försämras först vid Alzheimers; i senare stadier sprider de sig till bredare kortikala regioner, i linje med klinisk förståelse av sjukdomsutveckling.
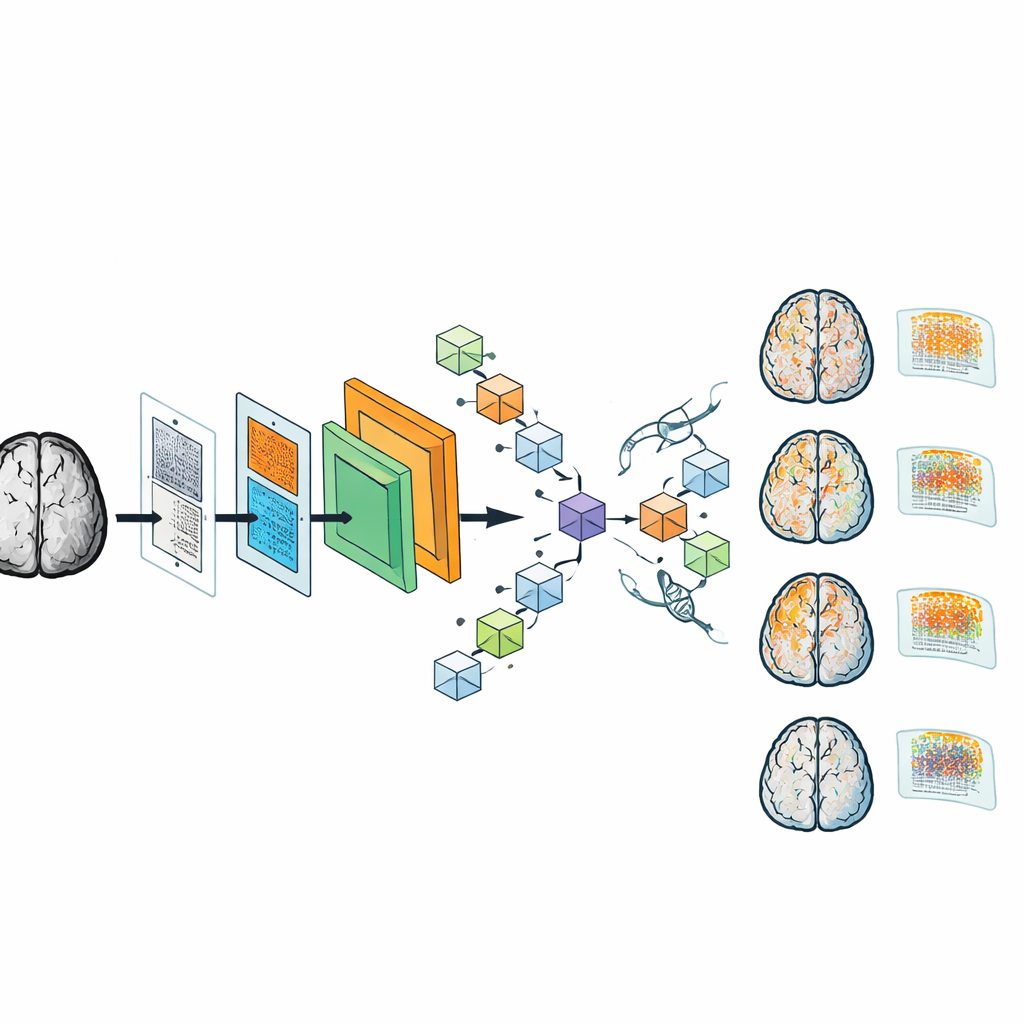
Vad detta betyder för patienter och kliniker
För icke-specialister är huvudbudskapet att studien erbjuder ett snabbt, kompakt och tolkningsbart verktyg för att bedöma demenssvårighet från rutinmässiga MRI-skanningar. Genom att balansera träningsdata och noggrant forma nätverket med derivatfri optimering skapade författarna en modell som kan köras på blygsig hårdvara samtidigt som den levererar nära perfekt noggrannhet och lyfter fram de hjärnregioner som ligger bakom dess beslut. Om detta bekräftas i framtida prospektiva kliniska prövningar kan sådan teknik stödja tidigare diagnos, mer konsekvent stadieindelning mellan sjukhus och bättre uppföljning av hur Alzheimers sjukdom förändrar hjärnan över tid.
Citering: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Nyckelord: Alzheimers sjukdom, hjärn-MRI, demensstadieindelning, djupinlärning, AI för medicinsk bildbehandling