Clear Sky Science · sv
Effekter av molekylär trängsel på proteiners stabilitet i ett bakterieproteom
Varför proteiners trånga tillvaro spelar roll
Inuti varje levande cell utför proteiner sina uppgifter i en miljö så fylld av andra molekyler att nästan halva volymen kan vara upptagen. Ändå studerar de flesta labbexperiment proteiner i utspädda, nästan tomma lösningar. Denna artikel ställer en enkel men viktig fråga: hur förändrar denna trånga verklighet proteinernas stabilitet och beteende, och vad betyder det för hur livet fungerar på molekylär nivå?
Ett blick in i en packad cellulär värld
För att utforska detta arbetade forskarna med en bakterie kallad Cupriavidus necator, en mikroorganism av intresse för gröna teknologier som koldioxidbindning och bioplastproduktion. De bröt försiktigt upp cellerna för att bevara hundratals olika proteiner nära sina naturliga former. Därefter tillsatte de höga koncentrationer av stora, vattenälskande polymerer—vanliga ”trängselmedel” kallade PEG, dextran och Ficoll—som ofta används för att efterlikna cellers täta inre.
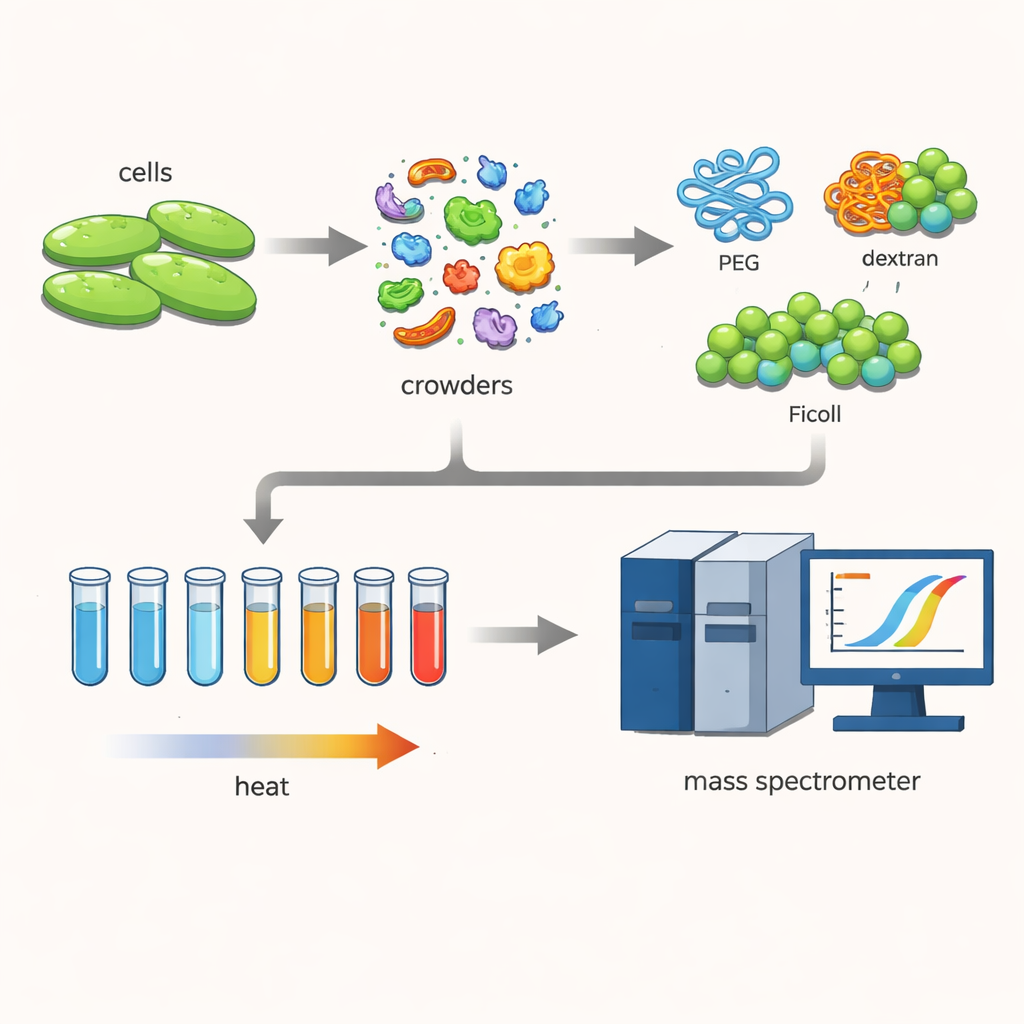
Att betrakta hur proteiner ”smälter”
Teamet använde en metod känd som termisk proteomprofilering. De värmde många små prover av proteinblandningen stegvis från 30 till 70 grader Celsius. När temperaturen steg veckade sig mindre stabila proteiner upp och klumpade ihop sig, vilket fick dem att falla ur lösningen. Genom att märka de återstående lösliga proteinerna och mäta dem med en känslig masspektrometer kunde forskarna rekonstruera smältkurvor för varje protein och bestämma dess smältpunkt—punkten där hälften har lämnat det lösliga, fungerande tillståndet. Genom att jämföra dessa temperaturer med och utan trängselmedel framkom hur den trängda miljön försköt proteinernas stabilitet.
En blandad bild: vissa proteiner stadigare, andra skörare
I genomsnitt sänkte tillsatsen av var och en av de sex polymerträngselmedlen smälttemperaturerna i bakterieproteomet, vilket antyder en svag övergripande destabiliserande effekt. Men denna globala trend dolde en mycket mer nyanserad bild. För dussintals individuella proteiner höjde eller sänkte trängselmedlen tydligt stabiliteten, ibland med flera grader. De flesta proteiner påverkades av endast ett av de sex reagensen, men ett fåtal svarade på flera, och nästan alla dessa var antingen konsekvent stabiliserade eller konsekvent destabiliserade, vilket antyder gemensamma underliggande egenskaper i hur de interagerar med trängselmedel.
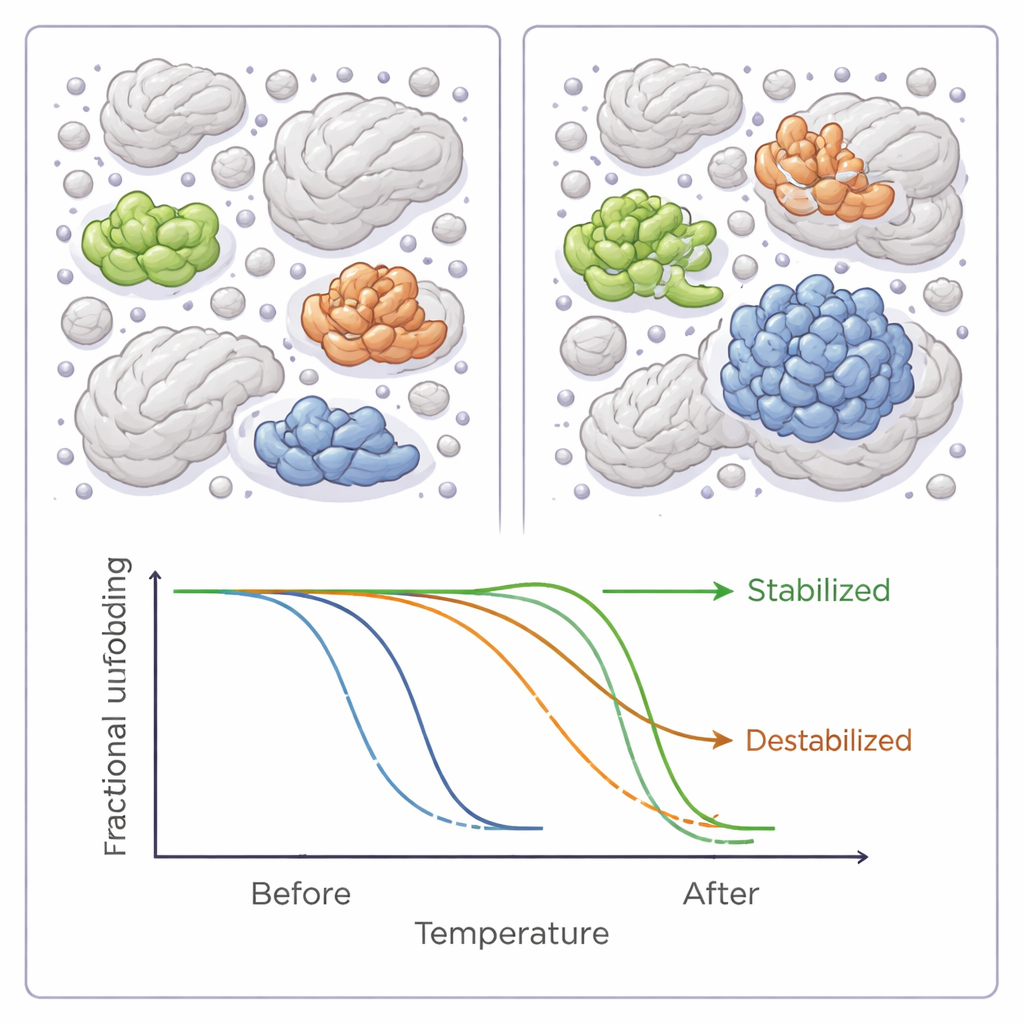
Vad får ett protein att vinna eller förlora i trängsel
När författarna granskade egenskaperna hos dessa känsliga proteiner framträdde mönster. Proteiner som blev mer stabila i trängda förhållanden tenderade att vara mer hydrofoba—det vill säga att de har fler vattenavstötande ytor—och var oftare klassiska enzymer med väldefinierade aktiva ytor. De var också mer benägna att vara involverade i protein–protein-interaktioner eller bära kemiska modifieringar som finjusterar deras funktion. Destabiliserade proteiner var däremot i genomsnitt mindre och hade färre sådana modifieringar. Dessa fynd speglar datormodeller och andra experiment som tyder på att trängsel kan gynna vissa proteiner medan den gör andra mer sårbara, beroende på storlek, form och hur de vanligtvis interagerar med partners.
Bortom enkel ihoptryckning: hur trängselmedel egentligen fungerar
Traditionella förklaringar för molekylär trängsel fokuserar på “uteslutet volym”-effekten, idén att stora molekyler helt enkelt lämnar mindre plats och skjuter proteiner att förbli veckade. Om detta vore hela bilden skulle man förvänta sig att trängselmedel främst stabiliserar proteiner och att det fanns starka samband med hur skrymmande eller viskösa trängselmedlen är. Istället såg författarna bara svaga kopplingar till polymerernas storlek och tjocklek. Deras data passade bättre med en bild av “preferentiell exclusion”: trängselmedel och proteiner undviker varandra kemiskt, vilket indirekt gynnar vissa veckade tillstånd men också kan störa känsliga interaktioner som håller andra proteiner stabila. Kort sagt, det är inte bara fysisk ihoptryckning utan subtila kemiska dragningar och stöter som formar proteinernas beteende.
Vad detta betyder för förståelsen av livets kemi
För icke-specialister är huvudbudskapet att proteiner inne i celler inte kan förstås fullt ut isolerat, simmandes i klar buffert. Den täta molekylära djungeln runt dem kan göra vissa proteiner stadigare och andra mer ömtåliga, vilket förändrar hur hela nätverk av reaktioner beter sig. Denna studie, genom att mäta stabilitetsförändringar för hundratals proteiner samtidigt, visar att trängseleffekter är komplexa och proteinspecifika, och sannolikt drivs av direkta interaktioner lika mycket som av enkel packning. När forskare designar läkemedel, industriella enzymer eller konstruerade mikrober kommer erkännandet av denna trånga verklighet vara avgörande för att förutsäga hur proteiner verkligen beter sig i levande system.
Citering: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Nyckelord: molekylär trängsel, proteinstabilitet, termisk proteomprofilering, bakterieproteom, cellmiljö