Clear Sky Science · sv
Negr1-brist förändrar glutamatsignalering och kinureninvägen i en musemodell för psykiatriska sjukdomar
Varför denna hjärnstudie är viktig
Många vanliga psykiska sjukdomar, från depression till schizofreni, är kopplade till subtila förändringar i hur hjärnceller kommunicerar. Denna studie undersöker en riskgen, kallad NEGR1, i möss för att se hur dess frånvaro ändrar hjärnans kemi och beteende. Genom att följa hur dessa möss rör sig efter en drog som kortvarigt stör en nyckelreceptor i hjärnan, och genom att mäta relaterade hjärnkemikalier, visar forskarna hur genetik, kön och hjärnans ämnesomsättning kan samverka för att forma sårbarhet för psykiatriska störningar.
En gen som håller hjärnsignaler i balans
NEGR1-genen kodar för ett cellmembranbundet protein som hjälper nervceller att bilda och stabilisera kontaktpunkter. Tidigare studier visade att borttagning av denna gen hos möss förändrar hjärnans struktur, minskar vissa hämmande (GABA) kopplingar och ändrar responser på dopaminrelaterade läkemedel som amfetamin. Eftersom dessa förändringar tyder på ett skifte mot starkare excitatoriska signaler, riktade teamet in sig på ett annat stort excitatoriskt system: glutamat och dess NMDA-receptorer, som är centrala för inlärning, minne och flexibel beteende. De studerade också “kinureninvägen”, en metabol väg som bryter ner aminosyran tryptofan till föreningar som antingen kan förstärka eller blockera NMDA-receptorer.
Tester av beteende med en medvetandepåverkande drog
För att undersöka NMDA-receptorernas funktion använde forskarna MK-801, ett välkänt läkemedel som kortvarigt blockerar dessa receptorer och kan efterlikna aspekter av glutamatobalans som ses vid psykiatriska tillstånd. Han- och honmöss bar antingen den normala Negr1-genen eller saknade den helt. Djurens fick dagliga injektioner av MK-801 och testades i en öppen fält-arena, där deras totala rörelse, tid i hörnen och snurrliknande rotationer automatiskt registrerades. Hos drogförändrade (naiva) hanar gav en enda dos MK-801 ett starkare aktivitetsspur hos Negr1-defici entmöss än hos normala möss, vilket tyder på att deras hjärnor var ovanligt känsliga för denna störning av glutamatsignalering.
Ett förvånande mönster av snabb tolerans
När MK-801 gavs upprepade gånger förändrades mönstret. Hos hannar sköt aktiviteten i höjden vissa dagar men föll vartannat dag, vilket bildade ett zick‑zack‑mönster som antydde snabb, partiell tolerans mot drog effekterna. Under nio dagar visade normala hannar en stigande respons i linje med sensibilisering, medan Negr1-deficienta hannar uppvisade en dämpad uppbyggnad av aktivitet och mildare dag‑till‑dag‑förändringar, vilket pekar på ändrad NMDA‑receptorkänslighet. Honor av båda genotyper anpassade sig ännu snabbare: omkring dag fem gav MK-801 inte längre starka beteendeeffekter, så behandlingen avbröts. I alla mätningar hade kön en stor påverkan, och tydliga genotypeffekter framträdde främst hos hannar.
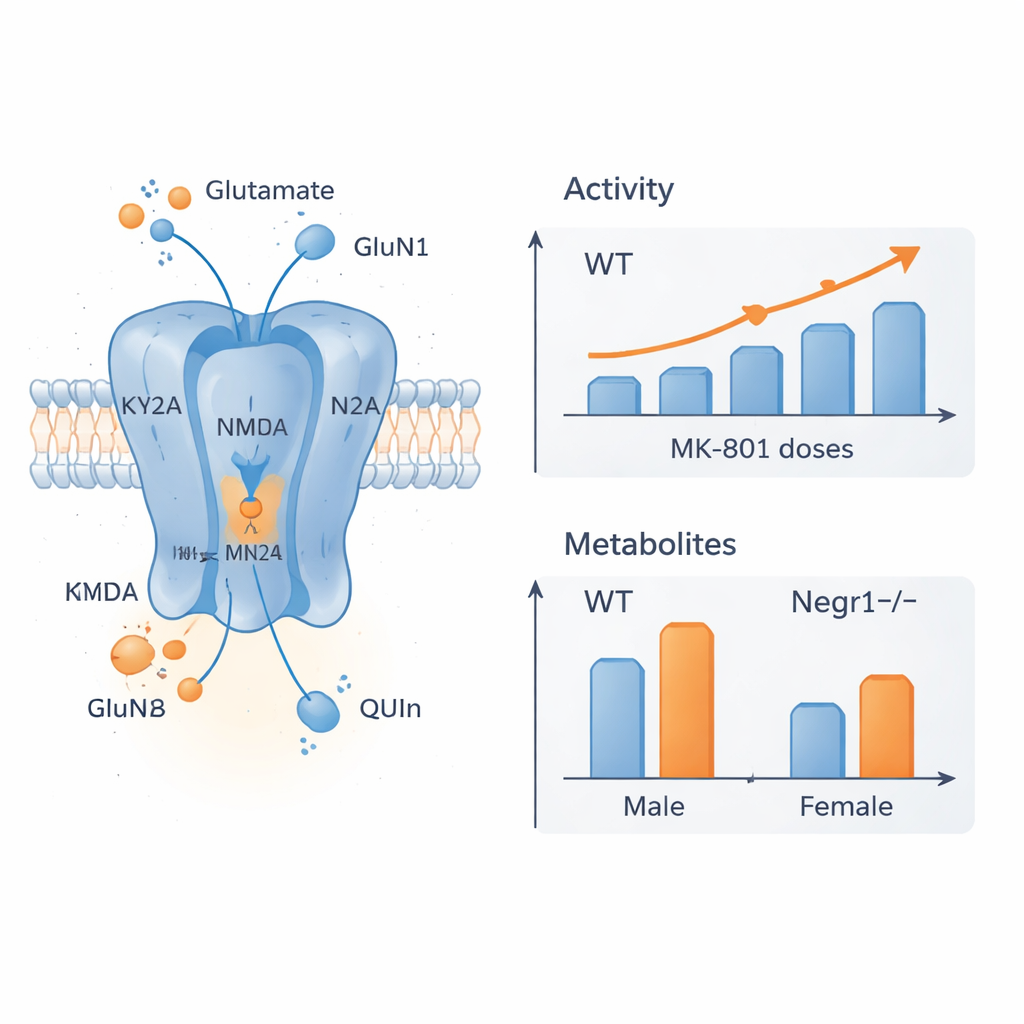
Skiften i receptorer och hjärnkemikalier
För att ta reda på vad som låg bakom dessa beteendeskillnader mätte teamet genaktivitet för viktiga NMDA‑receptorsubenheter och för ett enzym som producerar D‑serin, en medsignal för dessa receptorer. De fokuserade på hjärnområden som är avgörande för stämning och kognition: frontal cortex och hippocampus. I frontal cortex visade honmöss utan Negr1 som behandlats med MK-801 reducerad uttrycksnivå av kärnreceptorsubenheter, vilket tyder på att deras hjärnor justerar receptorns sammansättning som svar på både mutation och drog. I hannars hippocampus visade Negr1-deficienta möss högre basala nivåer av vissa NMDA‑subenheter, i linje med tidigare bevis för fler tillgängliga receptorer; MK-801‑behandling drog då tillbaka dessa nivåer mot det normala. Parallellt avslöjade detaljerade kemiska analyser av blod och flera hjärnområden att flera metaboliter i kinureninvägen och glutamat självt var förändrade på ett köns‑ och områdesspecifikt sätt, med frontal cortex mest påverkad och vissa förändringar som blev mer uttalade med åldern.
Vad detta betyder för förståelsen av psykisk ohälsa
Tillsammans framställer dessa fynd NEGR1 som en molekylär organisatör som hjälper till att hålla excitatoriska och inhibitoriska hjärnsignaler i balans, delvis genom att forma NMDA‑receptorernas funktion och tryptofanmetabolism. När Negr1 saknas reagerar möss annorlunda på NMDA‑receptorblockad, visar könsberoende skiften i hjärnkemikalier och utvecklar gradvis tolerans på ovanliga sätt. För en allmän läsare är huvudbudskapet att en enda riskgen inte verkar isolerat: dess effekter beror på kön, hjärnområde och metabolt tillstånd. Detta arbete stärker idén att rikta in sig på vägar kopplade till NEGR1—snarare än endast enskilda receptorer—så småningom kan hjälpa att skräddarsy behandlingar för psykiska sjukdomar som kännetecknas av glutamatobalans.
Citering: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Nyckelord: NEGR1-genen, NMDA-receptor, glutamatsignalering, kinureninvägen, psykiatriska sjukdomar