Clear Sky Science · sv
Strukturanalys av OCT4-bindning till mänskliga LIN28B-nukleosomer
Hur celler får åtkomst till dolda genetiska instruktioner
Varje cell i din kropp bär på samma DNA, ändå används bara en delmängd av dessa genetiska instruktioner i en viss celltyp. En stor del av detta kontrollsätt styrs av hur DNA packs tätt runt proteiner kallade histoner och bildar strukturer som kallas nukleosomer. Denna täta packning kan dölja viktiga DNA-sekvenser för den cellulära maskineriet som läser gener. Den här studien undersöker hur ett speciellt protein, OCT4, lyckas hitta och binda sitt mål-DNA även när det är virat och delvis dolt i nukleosomer — en process som är central för stamcellsidentitet och cellulär omprogrammering.
Varför pionjärfaktorer är viktiga för stamceller
OCT4 tillhör en liten men kraftfull grupp proteiner som kallas pionjär-transkriptionsfaktorer. Till skillnad från de flesta DNA-bindande proteiner kan pionjärer tränga in i kompakterade, ”avstängda” regioner av genomet och hjälpa till att slå på gener, vilket spelar en avgörande roll för att forma cellidentitet och vid omprogrammering av vuxna celler till stamcells-liknande tillstånd. OCT4 samarbetar med partners som SOX2, KLF4 och c-MYC för att inducera pluripotens — egenskapen som gör att stamceller kan utvecklas till nästan vilken celltyp som helst. Att förstå exakt hur OCT4 fäster vid DNA som är inbäddat i nukleosomer är viktigt för att avkoda hur celler byter öde och för att utforma mer precisa sätt att styra cellidentitet inom forskning och medicin.
Undersöka om artskillnader spelar roll
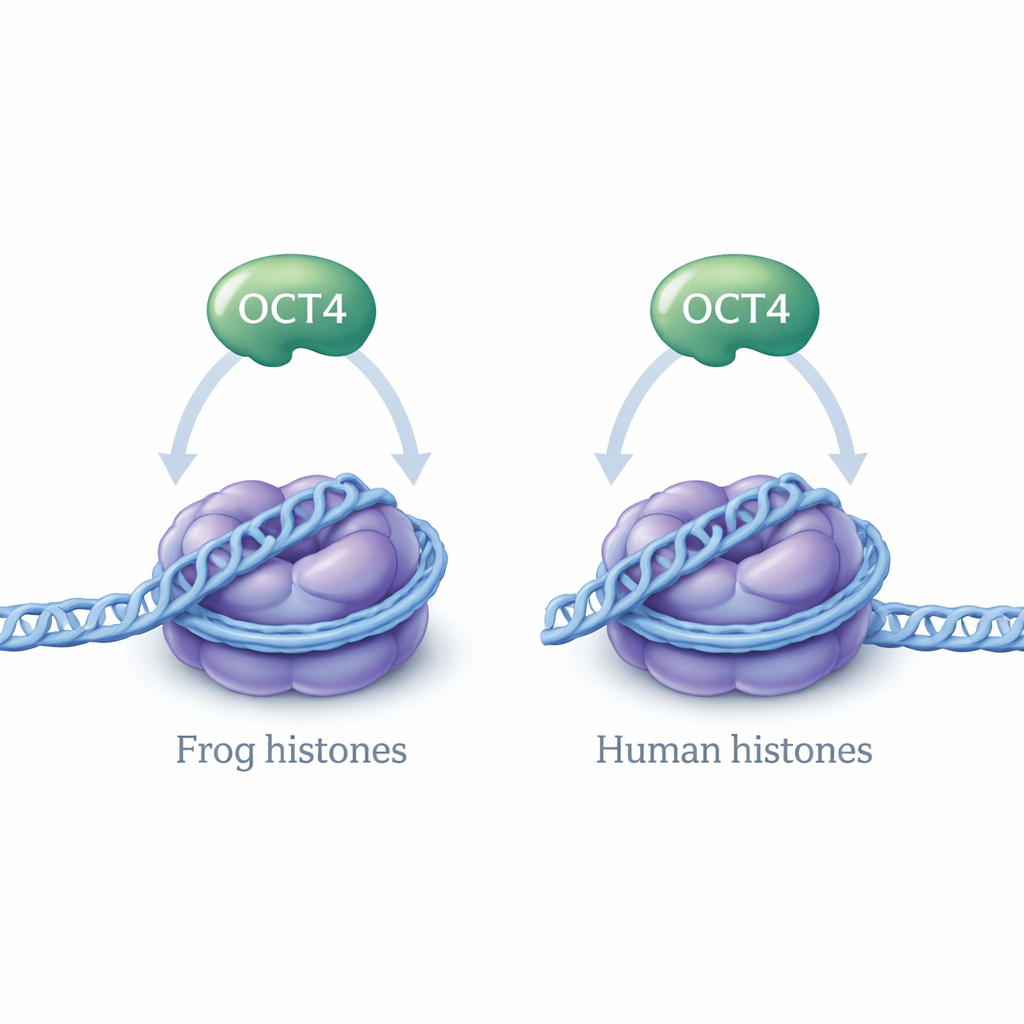
De flesta strukturella studier av nukleosomer använder histonproteiner antingen från grodor (Xenopus laevis) eller människor, eftersom dessa proteiner är mycket lika men inte identiska. Små skillnader i deras aminosyrasekvenser kan i princip påverka hur DNA viras eller hur reglerande proteiner som OCT4 binder. I tidigare arbete visade författarna att OCT4 binder till en specifik regulatorisk DNA-sekvens från det mänskliga LIN28B-genen när detta DNA är inbäddat i nukleosomer byggda med grodhiston. I den nya studien ställde de en enkel men viktig fråga: beter sig OCT4 på samma sätt när nukleosomerna är byggda av mänskliga histoner i stället för grodhiston?
Bygga och undersöka LIN28B-nukleosomer
För att svara på detta rekonstituerade forskarna nukleosomer i laboratoriet med ett 182 baspar långt segment av LIN28B-DNA och antingen mänskliga eller grodhistoner, monterade med en noggrann ”långsam dialys”-metod som efterliknar förhållanden i celler. Gelbaserade analyser bekräftade att båda typerna av histonoktamerer bildade nukleosomer effektivt. De undersökte därefter hur dessa nukleosomer placerar sig på LIN28B-DNA. Både gel-experiment och DNA-klippning följt av sekvensering (MNase-seq) visade att LIN28B-DNA kan anta flera positioner på histonkärnan, och detta beteende förändrades inte när nukleosomerna värmdes till kroppstemperatur. Avgörande var att det inte gjorde någon märkbar skillnad för hur DNA positionerades eller hur tätt OCT4 band beroende på om histonerna kom från grodor eller människor.
Visualisera OCT4 på nukleosomen
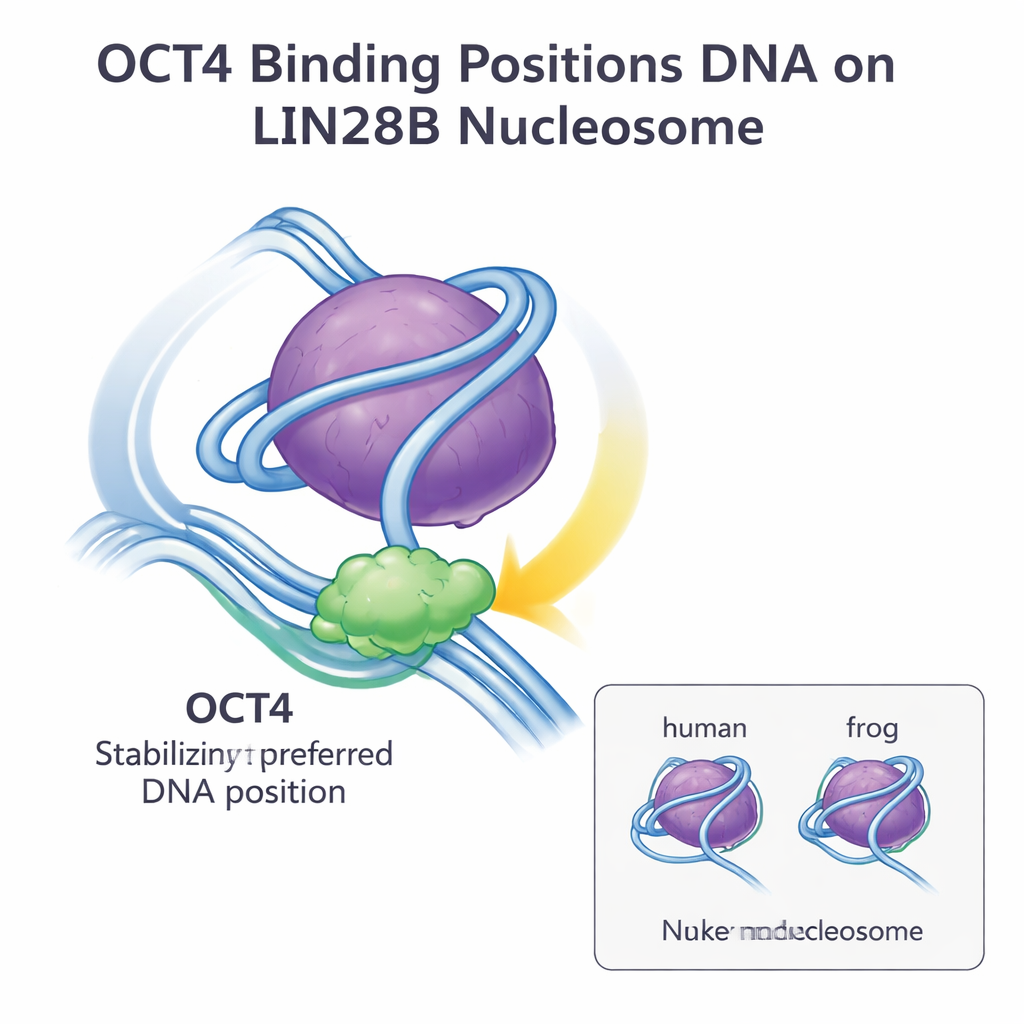
Teamet använde sedan kryogen elektronmikroskopi (cryo-EM) för att visualisera strukturen av OCT4 bundet till LIN28B-nukleosomer innehållande mänskliga histoner. Från ungefär 15 000 partiklar rekonstruerade de en tredimensionell karta med cirka 6 ångström upplösning. Bilderna visade att båda DNA-bindande delarna av OCT4 kontaktar samma exponerade DNA-segment nära nukleosomens in- och utgångspunkt, den så kallade länkregionen. Detta är exakt den plats och orientering som tidigare observerats när OCT4 var bundet till nukleosomer gjorda med grodhiston. När den äldre modellen passades in i den nya cryo-EM-kartan var överensstämmelsen utmärkt, vilket indikerar att den övergripande arkitekturen för OCT4–LIN28B-nukleosomkomplexet i stort sett är identisk för båda arterna.
En generell strategi för att öppna kromatin
Tillsammans visar dessa fynd att små sekvensskillnader mellan grod- och människohistoner inte förändrar hur OCT4 känner igen och binder LIN28B-nukleosomen. LIN28B-DNA ligger naturligt i flera möjliga positioner på histonkärnan, men OCT4-bindning väljer och stabiliserar en föredragen position, vilket gör fler bindningsställen mer åtkomliga för OCT4 och dess partner. Denna strategi med ”DNA-positionering och stabilisering” verkar vara ett generellt sätt för pionjärfaktorer att få åtkomst till stängt kromatin och främja kooperativ bindning av andra regulatorer. För en allmän publik är slutsatsen att nukleosomens grundläggande design och hur nyckelreglerande proteiner som OCT4 samarbetar med den är högt bevarade över arter, vilket förstärker idén att insikter från modellorganismer på ett tillförlitligt sätt kan informera vår förståelse av mänsklig genreglering och stamcellsbiologi.
Citering: Sinha, K.K., Halic, M. Structural analysis of OCT4 binding to human LIN28B nucleosomes. Sci Rep 16, 5704 (2026). https://doi.org/10.1038/s41598-026-35959-8
Nyckelord: pionjär-transkriptionsfaktorer, OCT4, nukleosomstruktur, kromatinåtkomlighet, styrning av stamcellsgener