Clear Sky Science · sv
APOBEC3B förbättrar effektiviteten hos PARP-hämmare vid eliminering av ovariala cancerceller med stamcellsegenskaper
Varför denna forskning är viktig för patienter med äggstockscancer
Många kvinnor med avancerad äggstockscancer svarar inledningsvis väl på moderna läkemedel kallade PARP-hämmare, som utnyttjar svagheter i tumörens DNA-reparationssystem. Men med tiden återkommer sjukdomen ofta när cancerceller lär sig överleva dessa behandlingar. Denna studie undersöker en oväntad följeslagare inne i cancercellerna själva — ett DNA-ändrande enzym kallat APOBEC3B — och visar att det, under rätt omständigheter, faktiskt kan göra det lättare att eliminera ovariala cancerceller med stamcellsegenskaper med hjälp av PARP-hämmare.
En dödlig cancer som återkommer
Höggradig serös äggstockscancer är den vanligaste och mest dödliga formen av äggstockscancer. Den diagnostiseras ofta sent, när sjukdomen redan har spridit sig i buken, och mer än 80 % av patienter med avancerad sjukdom får tillbaka cancer inom fem år. En viktig misstänkt bakom dessa återfall är en liten population av "cancerceller med stamcellsegenskaper." Dessa celler kan förnya sig själva, överleva cytostatikabehandling och återbygga tumörer efter behandling. Att förstå vad som gör dessa stamliknande celler resistenta — och hur man kan rikta behandling mot dem — är avgörande för att förbättra långsiktig överlevnad.
Ett muterande enzym med ett dubbelliv
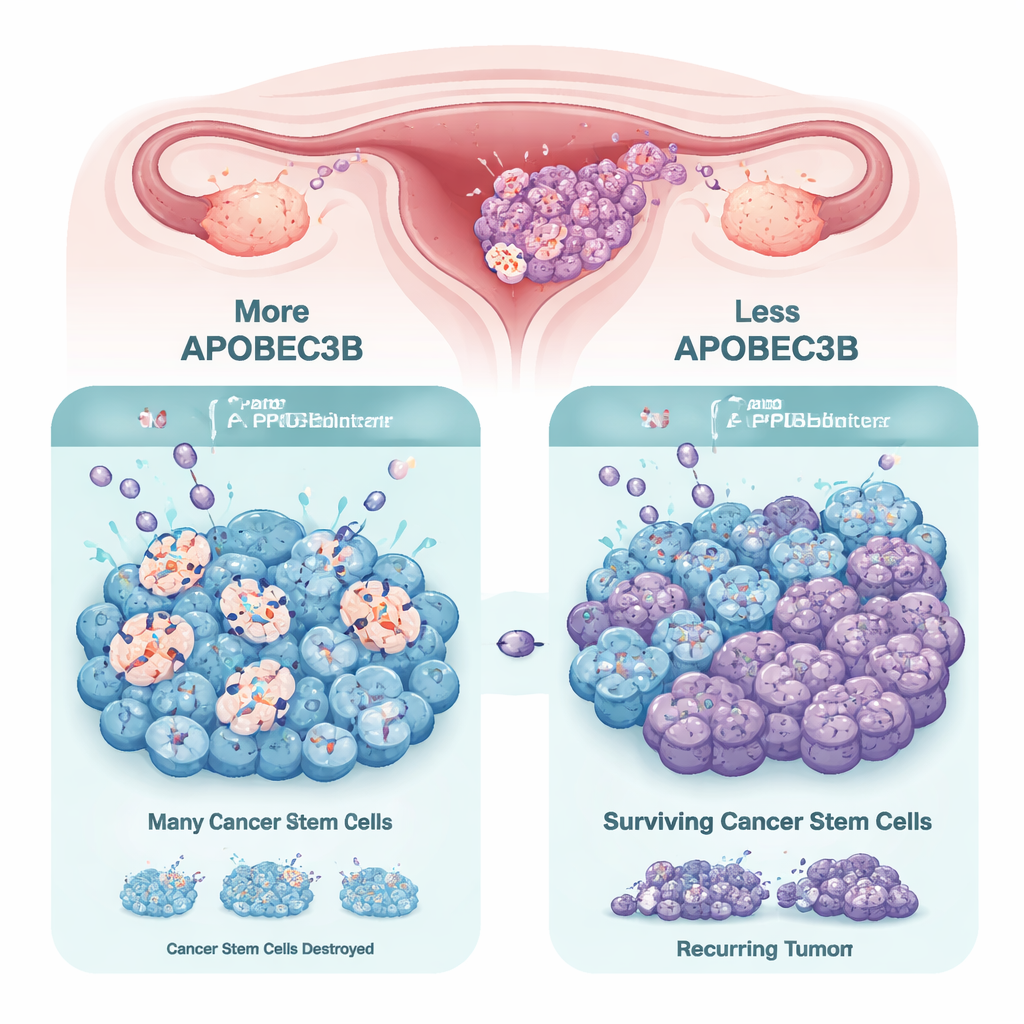
APOBEC3-familjen av enzymer hjälper normalt till att skydda våra celler mot virus genom att ändra specifika DNA-bokstäver, vilket kan introducera mutationer. I många cancrar är ett familjemedlem, APOBEC3B, överaktivt och bidrar till DNA-skador och genetiskt kaos, vilket kan driva tumörevolution och terapiresistens. I ovariala tumörer och patientnära modeller bekräftade forskarna att APOBEC3B vanligen är det mest rikliga APOBEC3-enzymet. Men när de jämförde vanliga tumörceller med stamcellsliknande "tumorsfärer" odlade i tre dimensioner, upptäckte de att de stamliknande cellerna konsekvent sänker nivån av APOBEC3B. Detta tyder på att cancerceller med stamcellsegenskaper kan minska sin mutationsbörda för att bevara sin överlevnad och förmåga till självförnyelse.
Att sänka APOBEC3B gör stamceller tuffare
För att testa om APOBEC3B faktiskt påverkar stamcellsegenskaper använde teamet genetiska verktyg för att slå ner dess uttryck i ovariala cancermodeller härledda från patienter och i etablerade cellinjer. När APOBEC3B-nivåerna sänktes bildade cancerceller tumorsfärer mer effektivt och visade högre nivåer av klassiska stamcellsmarkörer såsom SOX2, OCT4 och NANOG. Andelen celler med stamcellslika egenskaper ökade, vilket indikerar att förlust av APOBEC3B hjälper cancerceller att skifta till ett mer motståndskraftigt, stamliknande tillstånd. I möss växte inte tumörer som saknade APOBEC3B snabbare på egen hand, men de beter sig annorlunda när de behandlades med PARP-hämmare.
Mer APOBEC3B, mer skada — och bättre läkemedelsrespons
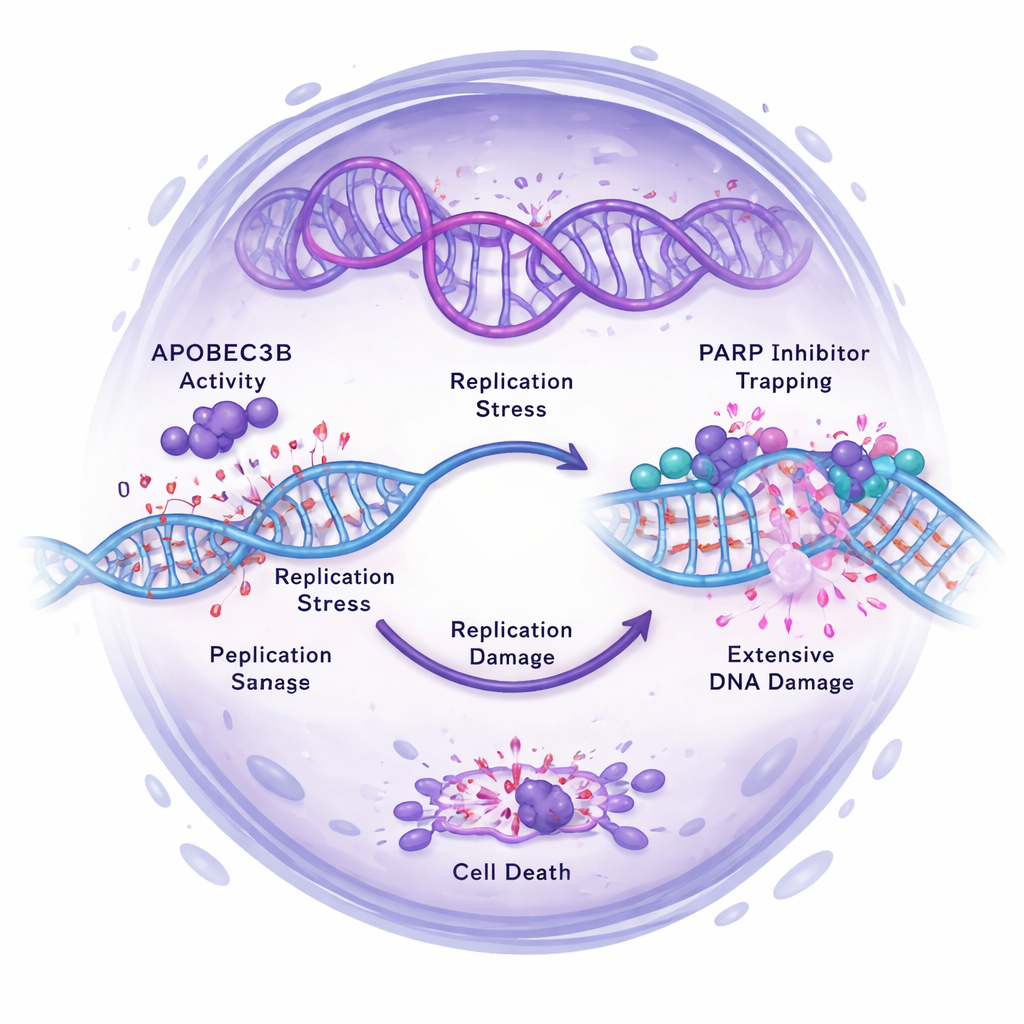
Forskarna frågade sig sedan hur APOBEC3B påverkar effekten av PARP-hämmare som Olaparib, vilka verkar genom att blockera DNA-reparation och driva cancerceller över gränsen till dödlig DNA-skada. I flera ovariala cellinjer gjorde minskad APOBEC3B cellerna mer resistenta mot PARP-hämmare, särskilt i 3D-tumorsfärer som är rika på stamliknande celler. Omvänt gjorde ökad APOBEC3B vissa celler känsligare för PARP-hämmare och kraftigt minskade deras överlevnad. I musförsök krympte eller bromsade tumörer med normal APOBEC3B dramatiskt med Olaparib, medan APOBEC3B-bristande tumörer fortsatte växa trots behandling. Molekylära analyser visade förklaringen: höga APOBEC3B-nivåer ökade replikationsstress och dubbelsträngsbrott i DNA, vilket aktiverade DNA-skade-signalvägar. När APOBEC3B slogs ner minskade PARP-hämmarinducerad DNA-skada, checkpoint-aktivering och replikationsstress, och cellerna var mer benägna att stanna säkert i cellcykeln istället för att dö.
Ett nytt sätt att tänka kring resistens och behandlingsdesign
Genom att fördjupa sig med RNA-sekvensering fann teamet att kombinationen av APOBEC3B-förlust och PARP-hämning omprogrammerade många gener involverade i DNA-replikation och reparation, vilket ytterligare stöder idén att APOBEC3B förstärker de skadliga effekterna av PARP-hämmare på cancercellernas genom. De testade också om ett annat reparationsenzym, UNG, krävdes för denna effekt och fann att känsligheten för PARP-hämmare i celler med hög APOBEC3B i stort sett var oberoende av UNG. Sammantaget pekar uppgifterna på APOBEC3B-drivet replikationsstress — inte bara dess mutagena aktivitet — som den huvudsakliga faktorn som hjälper PARP-hämmare att döda ovariala cancerceller med stamcellsegenskaper.
Vad detta betyder för patienter och framtida terapier
För en lekman är budskapet att inte allt genetiskt kaos i en tumör är dåligt. I denna studie gjorde högre nivåer av det muterande enzymet APOBEC3B faktiskt ovariala cancerceller med stamcellsegenskaper mer sårbara för PARP-hämmare genom att överbelasta deras DNA-repareringskapacitet. När APOBEC3B sänktes blev cancercellerna mer stamliknande och bättre på att tåla behandling. Dessa fynd tyder på att mätning av APOBEC3B-nivåer kan hjälpa till att förutsäga vilka patienter som får mest nytta av PARP-hämmare, och att tidpunkt eller kombination med framtida APOBEC3B-riktade läkemedel måste hanteras varsamt. Att utnyttja APOBEC3B:s "självsabotage" på cancerceller kan öppna nya strategier för att förebygga återfall och mer effektivt eliminera rötterna till ovariala tumörer.
Citering: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Nyckelord: äggstockscancer, PARP-hämmare, cancerceller med stamcellsegenskaper, APOBEC3B, läkemedelsresistens