Clear Sky Science · sv
Hämning av autofagi förstärker sulforafans anticancer‑egenskaper
Därför spelar broccolins ämnen och ett gammalt malariamedel roll
Blåscancer är vanligt och ofta dödligt när det sprider sig, och många patienter slutar så småningom svara på behandlingar. Denna studie undersöker ett oväntat samarbete: sulforafan, en naturlig förening från broccoli, och klorokin, ett länge använt malariamedel. Tillsammans stör de cancercellernas interna återvinningssystem och rörlighet på sätt som en dag skulle kunna göra blåscancerbehandlingar mer effektiva och hållbara.
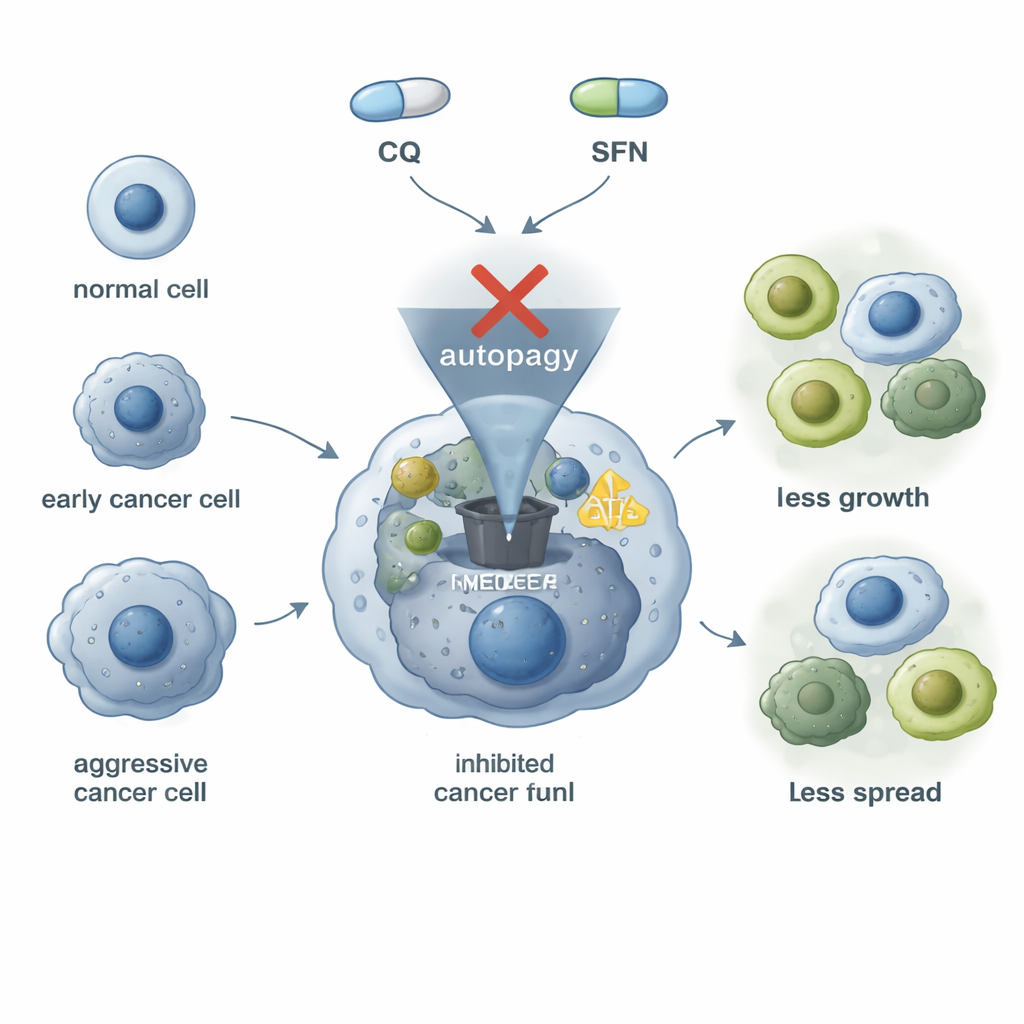
Utmaningen med svårbehandlade blåstumörer
Blåscancer är inte en enda sjukdom; tumörer skiljer sig åt i sina gener, hur aggressiva de är och hur de svarar på terapi. Många blåscancerceller är beroende av hög nivå av ”självrengöring”, en process som kallas autofagi, för att överleva stress, reparera skador och motstå läkemedel. Samma celler visar ofta höga mängder av ett ytprotein kallat ICAM-1 och ett annat protein, N‑cadherin, båda kopplade till ett mer rörligt, invasivt tillstånd som gör det lättare för cancern att sprida sig. Eftersom standardbehandlingar inte fullt ut tar itu med dessa överlevnadsstrategier söker forskare sätt att stänga av både återvinningsmaskineriet och det invasiva beteendet samtidigt.
Återanvändning av klorokin och utnyttjande av broccolins försvar
Klorokin, mest känt som malariamedel, kan blockera det sista steget i autofagi: ögonblicket när sopfyllda säckar förenas med sura kompartment som bryter ner material till användbar energi. På egen hand saktade klorokin tillväxten och rörligheten hos tre olika blåscancercellinjer i laboratoriet, vilket visar en grundläggande anticancer‑effekt. Men det ökade också oväntat ICAM-1‑nivåerna i alla dessa cancerceller, ett oroväckande tecken eftersom högre ICAM-1 är förknippat med mer aggressivt beteende. Sulforafan, en förening som naturligt finns i korsblommiga grönsaker som broccoli, har rapporterats hämma tillväxten hos många cancertyper och, viktigast, sänka ICAM-1‑nivåer. Det gjorde den till en attraktiv partner för klorokin: ett läkemedel för att blockera återvinningssystemet och ett för att dämpa en nyckelmarkör för aggressivitet.
Hur läkarkedjan försvagar cancerceller
Forskarna behandlade tre blåscancercellinjer med klorokin, sulforafan eller båda och följde ett nätverk av signalproteiner som styr tillväxt, rörlighet och autofagi. Klorokin blockerade konsekvent autofagi, vilket ledde till en uppbyggnad av vanliga återvinningsmarkörer inne i cellerna. När sulforafan tillsattes förstärktes flera av klorokins önskvärda effekter: det minskade ICAM-1‑ och N‑cadherin‑nivåerna i två av de tre cellinjerna, drev beta‑catenin (ett tillväxtrelaterat protein) mot nedbrytning och påverkade nyckelomkopplare (såsom AKT, GSK‑3β, mTOR och ULK) på sätt som i stort sett motverkade överlevnad och självrengöring. Samtidigt skadade den kombinerade behandlingen mitokondrierna – cellens kraftverk – och, beroende på cellinje, förändrade balansen av reaktiva syreradikaler, små molekyler som kan få celler att luta mot självförstörelse.
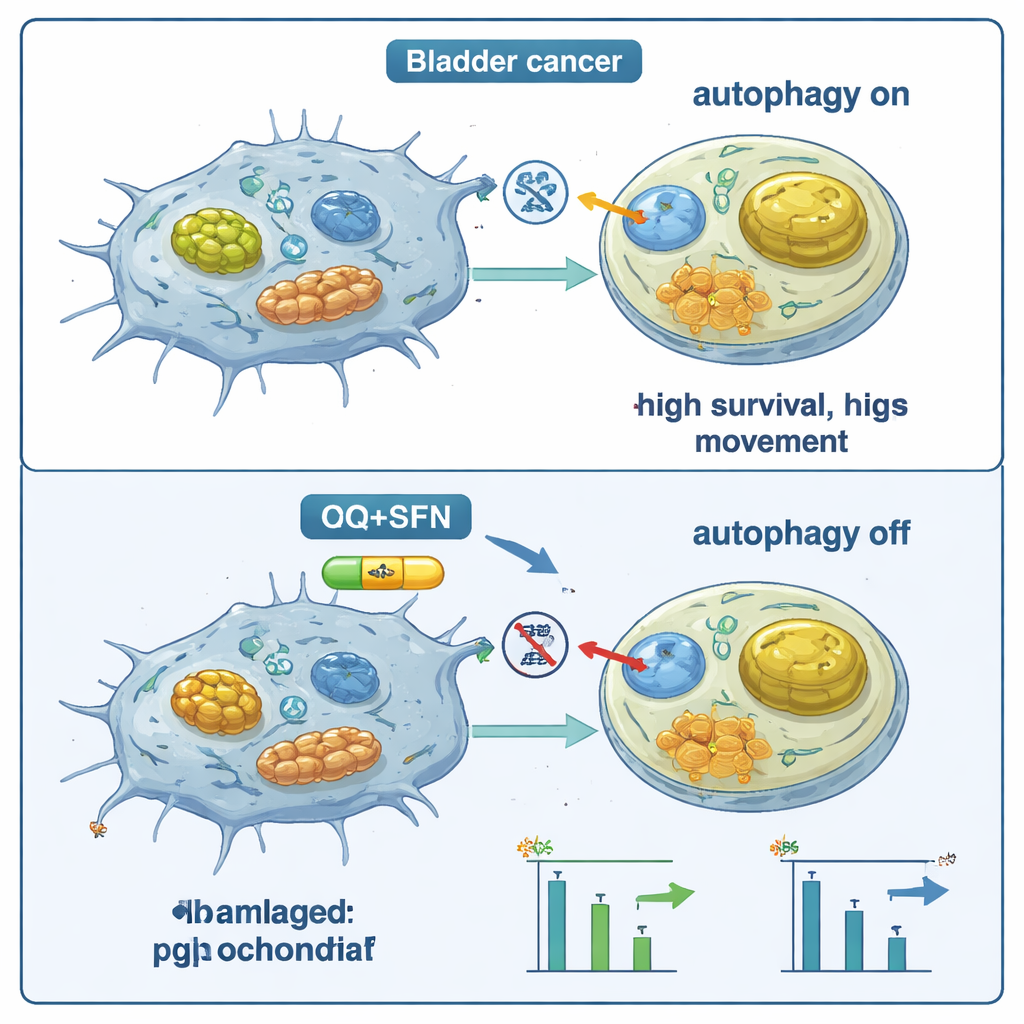
Långsammare tillväxt och mindre rörelse beror på celltyp
Bortom dessa molekylära förändringar ställde teamet två praktiska frågor: delar cellerna sig mindre, och rör de sig mindre? I alla tre blåscancercellinjer minskade kombinationen av sulforafan och klorokin cellproliferationen, med särskilt starka effekter i en linje som redan hade höga ICAM-1‑nivåer. Ett s.k. scratch‑eller “sår”‑test visade att behandlade celler krympte långsammare ihop för att stänga en öppning, vilket indikerar minskad migratorisk förmåga, återigen med starkast effekt när båda medlen användes tillsammans. Dock svarade inte alla cellinjer på samma sätt. I en linje med relativt låg ICAM-1 verkade blockad av autofagi ibland skydda den aggressiva profilen, vilket understryker att utfallet i hög grad beror på varje tumörs molekylära uppbyggnad.
Vad detta kan innebära för framtida behandlingar
För en icke‑specialist är huvudbudskapet att cancerceller använder ett internt återvinningsprogram och vissa ytproteiner för att överleva, dela sig och sprida sig, och att dessa egenskaper kan angripas från flera håll. I denna studie hjälpte sulforafan till att motverka en oönskad sidoeffekt av klorokin – dess tendens att öka en tumörfrämjande markör – samtidigt som den förstärkte den övergripande anticancer‑påverkan på blåsceller odlade i labb. Resultaten översätts ännu inte direkt till en kliniskt färdig terapi, och de belyser att vissa tumörer beroende på sin sammansättning kan dra nytta av autofagihämning. Ändå stöder arbetet idén att noggrant utvalda kombinationer av ett vanligt läkemedel och en naturlig kostförening kan anpassas efter tumörtyp för att bromsa blåscancertillväxt, begränsa spridning och förbättra svar på befintliga behandlingar.
Citering: Zarzycka, M., Kotula-Balak, M. & Gil, D. Inhibiting autophagy enhances anti-cancer properties of sulforaphane. Sci Rep 16, 5296 (2026). https://doi.org/10.1038/s41598-026-35891-x
Nyckelord: blåscancer, autofagi, sulforafan, klorokin, ICAM-1