Clear Sky Science · sv
Likheter i genuttryck och metyleringsförändringar mellan två råttmodeller för förvärvad epilepsi
Varför förändrade gener spelar roll för anfall
Epilepsi drabbar miljontals människor och för ungefär en av tre räcker inte dagens läkemedel för att helt kontrollera deras anfall. De flesta läkemedel dämpar helt enkelt hjärnans elektriska stormar utan att hindra att epilepsi utvecklas från början. Denna studie undersöker om bestående kemiska markörer på DNA och sättet gener slås av eller på kan förklara hur en frisk hjärna blir epileptisk — och om dessa förändringar är gemensamma för olika former av sjukdomen.
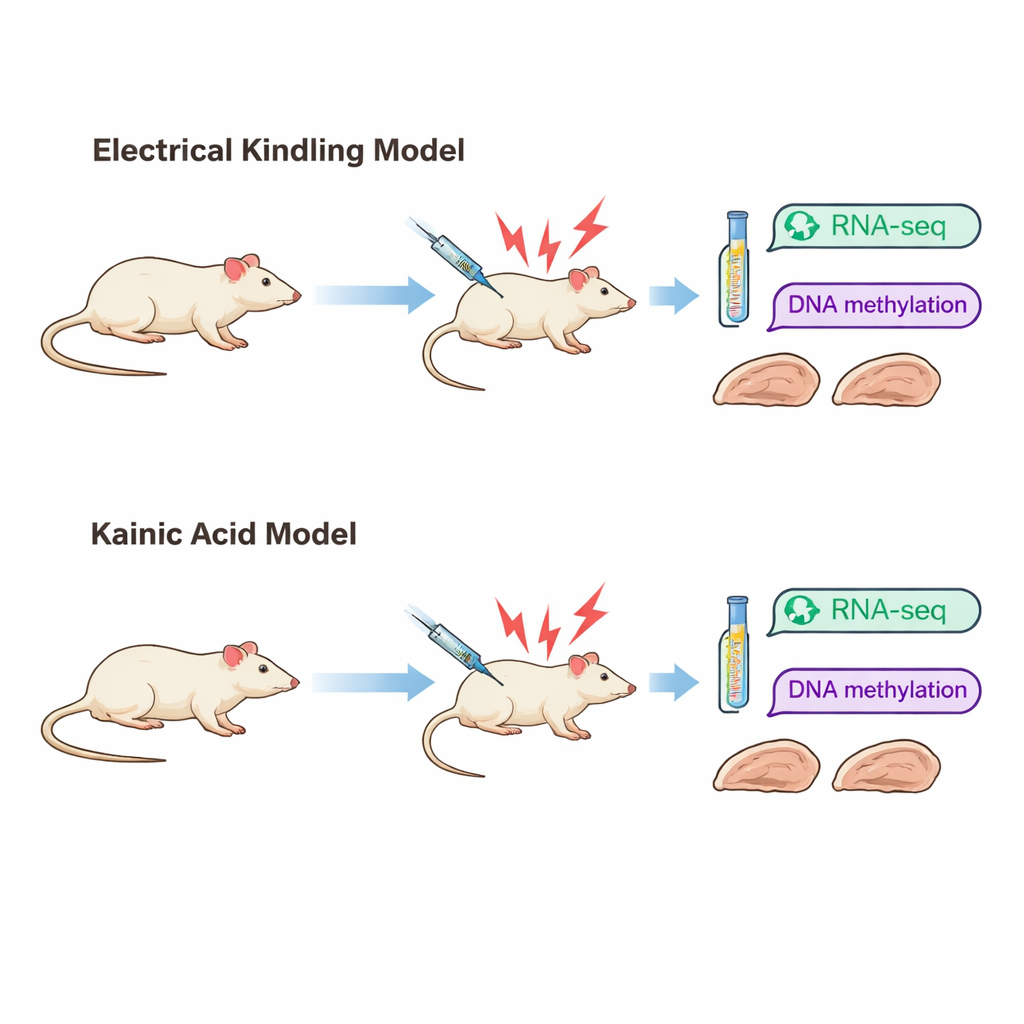
Två olika vägar till samma sjukdom
Forskarna fokuserade på temporal lobsepilpsi, en vanlig form av tillståndet som ofta är svår att behandla. De använde två väletablerade råttmodeller som återspeglar olika sätt epilepsi kan uppstå på. I "kindling"-modellen ges korta elektriska pulser till en del av hippocampus över tid tills anfall blir lätta att framkalla. I "kaininsyra"-modellen orsakar en kemikalie en intensiv period av anfall, varefter spontana anfall senare dyker upp. Även om båda modellerna slutligen ger liknande yttre beteende — svåra kramper — ser hjärnskadorna väldigt olika ut. Kindlade råttor visar i stort sett bevarad vävnadsstruktur, medan kaininsyra-behandlade råttor uppvisar uttalad cellförlust och ärrbildning i viktiga hippocampusregioner.
Att läsa hjärnans genetiska aktivitet
För att se hur dessa olika vägar till epilepsi påverkar hjärnan på molekylär nivå undersökte teamet hippocampus efter att råttor i varje modell hade upplevt tre svåra anfall. De mätte vilka gener som var mer eller mindre aktiva med RNA-sekvensering och kartlade kemiska markörer kallade metylgrupper på DNA med en metod känd som reduced-representation bisulfite sequencing. Förändringar i genaktivitet speglar hur celler svarar och anpassar sig, medan metyleringsmärken ofta ses som ett längreids "minne" som kan påverka om gener är påslagna eller avstängda.
Förändringar i genaktivitet överstiger DNA-märken
De två modellerna gav markant olika mönster av genaktivitet. Kindling-modellen visade förändringar i mer än tio gånger så många gener som kaininsyra-modellen. När forskarna dock överlappade de två listorna fann de fortfarande över hundra gener som skiftade i båda modellerna, och de flesta av dessa rörde sig i samma riktning. Ett exempel är Mmp9, en gen kopplad till hur hjärnceller omformar sina kopplingar och till skador relaterade till anfall; den var starkt uppreglerad i båda modellerna. Dessa delade förändringar antyder att det finns kärnmässiga genetiska svar vid epileptogenes, även när den initiala triggere och synliga hjärnskador skiljer sig åt.
DNA-märken berättar en annan historia
När teamet tittade på DNA-metylering förändrades bilden. Båda modellerna visade många gener med förändrad metylering, och det fanns en betydande överlappning mellan dem. Dock visade endast en måttlig delmängd av gener både förändrad metylering och förändrad aktivitet inom samma modell, och ännu färre uppträdde så i båda modellerna. I några av dessa delade gener, såsom Nedd9 och Ptpre, ökade uttrycket i båda modellerna, men riktningen för metyleringsförändringen vid enskilda platser kunde vara motsatt mellan modellerna. Överlag fanns ingen enkel regel om att "mer metylering betyder mindre genaktivitet" eller vice versa. Detta tyder på att i dessa epilepsimodeller är de flesta skiften i genaktivitet inte direkt drivna av breda förändringar i DNA-metylering.
Vad detta betyder för framtida behandlingar
För dem som hoppas på bättre epilepsibehandlingar ger dessa resultat både försiktighet och vägledning. Arbetet visar att de genetiska program som aktiveras under utvecklingen av epilepsi kan vara ganska specifika för modellen, och att DNA-metylering bara är en del av en större, mer komplex regleringsbild. Lovande gentarget identifierade i en enda djurmodell kanske inte generaliserar, så de bör testas över flera modeller innan man går vidare mot behandlingar för människor. Samtidigt kan den lilla uppsättning gener som förändras både i uttryck och metylering över modellerna utgöra särskilt robusta startpunkter för att utveckla sjukdomsmodifierande terapier som syftar till att inte bara dämpa anfall, utan att förhindra att epilepsi etablerar sig.
Citering: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Nyckelord: epileptogenes, DNA-metylering, genuttryck, temporal lobsepilpsi, råttmodeller