Clear Sky Science · sv
Sepsisassocierad muskelnedbrytning lindras av farmakologisk hämning av STAT3‑signalvägen hos möss
Varför svåra infektioner kan ta din styrka
Att överleva en livshotande infektion som sepsis är bara halva striden. Många patienter lämnar intensivvården så försvagade att det blir svårt att gå, gå i trappor eller ens lyfta armarna. Denna studie ställer en enkel men brådskande fråga: kan vi stoppa kroppen från att äta upp sina egna muskler under sepsis, och i så fall hur? Genom att använda möss, muskelceller i odling och observationer från patienter på en intensivvårdsavdelning spårar forskarna en nyckel‑signalväg som driver muskelförlust — och visar att ett riktat läkemedel delvis kan blockera skadan.
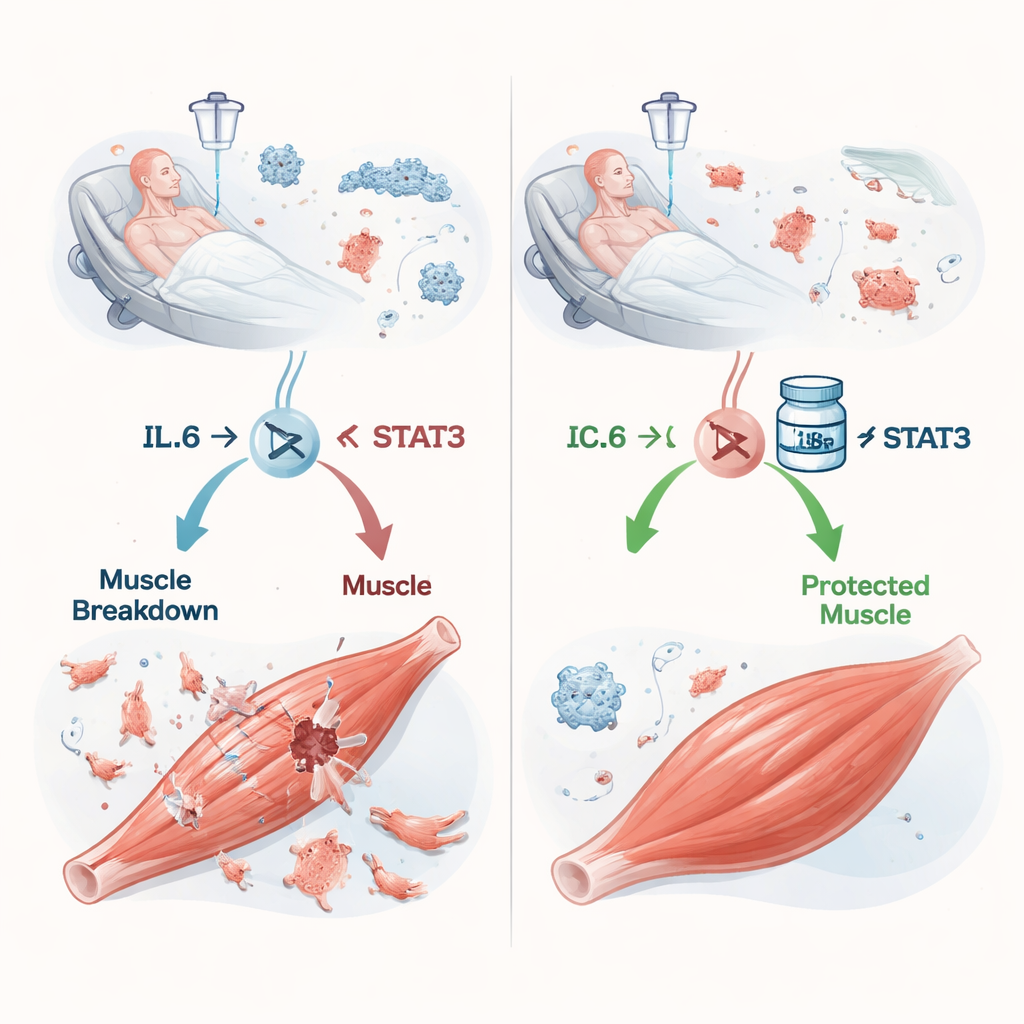
En kedjereaktion från infektion till muskelförlust
Sepsis uppstår när kroppens svar på infektion tappar kontrollen och blodbanan översvämmas av inflammatoriska molekyler. En av de viktigaste är interleukin‑6 (IL‑6). Tidigare arbete antydde att IL‑6 kan signalera till muskler att bryta ner sina egna proteiner, men detaljerna var oklara. Författarna fokuserade på STAT3, ett protein inne i cellerna som förmedlar IL‑6:s budskap till cellkärnan där gener slås på eller av. Hos möss som fick en cecal slurry — i praktiken en kontrollerad blandningsinfektion med bakterier — sköt IL‑6‑nivåerna i blod och benmuskler i höjden när sepsisen förvärrades. Samtidigt aktiverades STAT3 i muskeln, och djuren tappade vikt, muskelmassa och greppstyrka i en grad som följde sjukdomens svårighetsgrad och som nära efterliknade det som ses hos svårt sjuka patienter.
Hur sepsis omprogrammerar muskelceller
För att förstå vad sepsis gjorde inne i muskelfibrerna analyserade teamet genaktivitet i tibialis anterior, en stor lårmuskel. Tusentals gener ändrade sin aktivitet hos sepsissjuka möss jämfört med friska kontroller. Vägledningar involverade i inflammation, cellulär stress och särskilt IL‑6/STAT3‑signalering slog på. Två huvudsystem för nedbrytning av proteiner rampade upp: ubiquitin–proteasomsystemet, som märker specifika muskelproteiner för destruktion, och autofagi, en mer generell återvinningsprocess. Nyckelenzym för ”muskelnedbrytning”, MuRF1 och atrogin‑1, ökade kraftigt, medan tillväxtfrämjande vägar och klassiska celldödssignaler förblev till stor del oförändrade. I parallella experiment visade odlade musmuskelceller som exponerades för lipopolysackarid (LPS), en komponent i gramnegativa bakteriers cellväggar, samma mönster: aktivering av IL‑6 och STAT3, ökning av MuRF1 och atrogin‑1, mer autofagi och synlig förtunning av muskelfibrerna.
Att blockera en viktig strömbrytare för att skydda muskeln
Det centrala experimentet testade om nedstängning av STAT3 kunde skona muskeln. Möss med sepsis behandlades med en småmolekylär STAT3‑hämmare kallad C188‑9, med start en timme efter infektionen och därefter dagligen. Läkemedlet mildrade inte den inledande "cytokinstormen" — blodnivåerna av IL‑6 och en annan inflammatorisk faktor, TNF‑α, förblev höga och kroppsvikt samt aptit återhämtade sig inte snabbt. Ändå skyddade C188‑9 tydligt skelettmuskulaturen: behandlade möss bibehöll mer tibialis‑muskelmassa, hade starkare grepp och större muskelfibrer under mikroskop än obehandlade sepsissjuka möss. Inne i musklerna minskade C188‑9 kraftigt aktiverat STAT3 och sänkte nivåerna av MuRF1 och atrogin‑1, men lämnade autofagimarkörer i stort sett oförändrade. I odlingsskåls‑experiment dämpade förbehandling av muskelceller med C188‑9 på samma sätt STAT3‑aktiveringen och ökningen av MuRF1 och atrogin‑1, och förhindrade LPS‑inducerad krympning av fibrerna, återigen utan att stänga av autofagin.
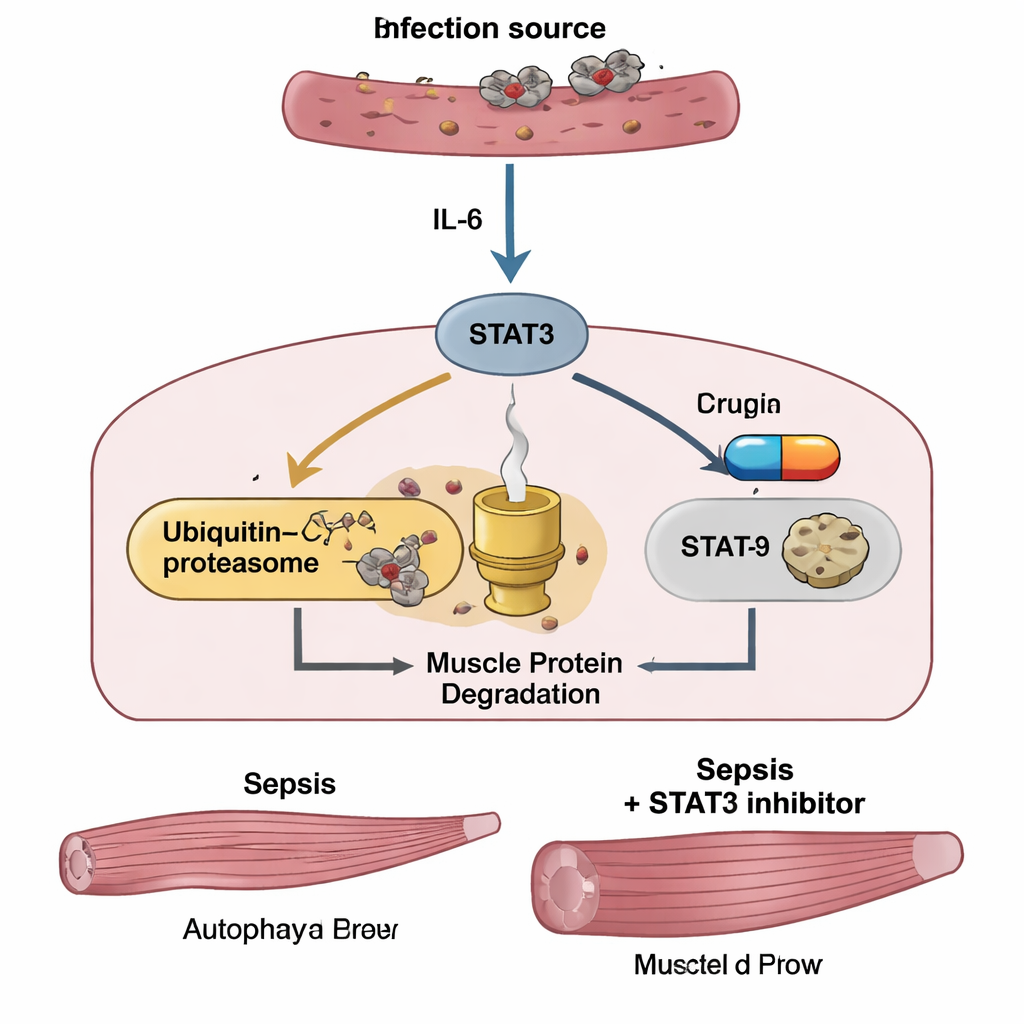
Ledtrådar från patienter på intensivvårdsavdelning
För att se om dessa mekanismer är relevanta hos människor följde forskarna 67 vuxna med sepsis som lagts in på en intensivvårdsavdelning i Japan. Blodprover vid intag visade att patienter med septisk chock hade särskilt höga IL‑6‑nivåer. I hela gruppen korrelerade IL‑6 — men inte TNF‑α — nära med sepsisens svårighetsgrad och med blodmarkörer för inflammation och muskelskada. I en undergrupp av 45 patienter som genomgick två CT‑skanningar av buken förutsade IL‑6‑nivåerna vid intag hur mycket psoasmuskelaturen vid nedre ryggraden krympte under de följande en till tre veckorna. De som förlorade mest muskelmassa hade märkbart sämre tvåårsöverlevnad än de som bibehöll mer muskelmassa, vilket understryker att sepsisrelaterad svältning inte bara är kosmetisk — den är kopplad till långsiktig dödlighet.
Vad detta kan innebära för framtida behandlingar
Tillsammans skissar mus‑, cell‑ och patientdata en trovärdig berättelse: under sepsis aktiverar stigande IL‑6 STAT3 i muskeln, vilket i sin tur slår på ett proteinnedbrytande system som blir av med muskelfibrernas kontraktila maskineri. Autofagi ökar också men tycks vara mindre direkt styrd av STAT3. Genom att farmakologiskt blockera STAT3 med C188‑9 kunde forskarna avbryta denna "självkanibaliserings"‑väg hos möss och odlade muskelceller, och bevara styrka även när infektionen och inflammationen fortsatte. Även om detta arbete fortfarande är prekliniskt och inte bevisar att STAT3‑hämmare hjälper mänskliga patienter, pekar det ut IL‑6/STAT3‑axeln som ett lovande mål för läkemedel som syftar till att förebygga eller minska den djupa muskelsvaghet som plågar många överlevare efter sepsis.
Citering: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Nyckelord: sepsis, muskelnedbrytning, STAT3, inflammation, återhämtning efter kritisk sjukdom