Clear Sky Science · sv
Lättviktig SwiM-UNet med mångdimensionell adapter för effektiv medicinsk bildsegmentering på enheten
Smartare undersökningar vid sängkanten
Hjärnavbildningar kan avslöja livshotande tumörer, men att omvandla råa bilder till tydliga konturer som läkare kan agera utifrån är fortfarande tidskrävande och resurskrävande. I denna studie presenteras SwiM‑UNet, en ny algoritm som kan segmentera hjärntumörer från 3D‑MR‑bilder med topprestation samtidigt som den körs effektivt på lokala enheter, vilket för flyttar exakt bildanalys närmare patientens sängkant eller till och med in i mobila kliniker. 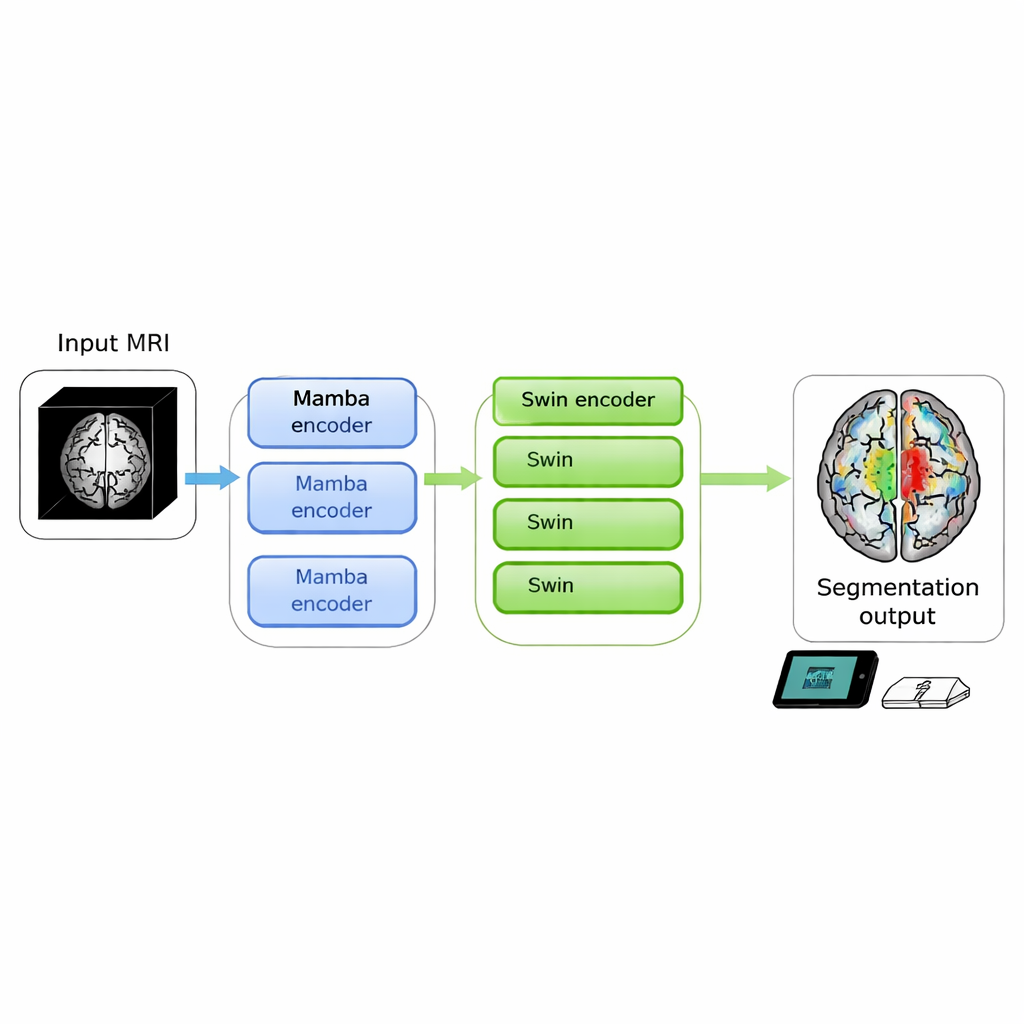
Varför exakta tumörkonturer spelar roll
Modern medicin förlitar sig i hög grad på bilddiagnostik för att planera operationer, strålbehandling och läkemedelsbehandlingar. För hjärntumörer behöver läkare inte bara se att en tumör finns, utan också veta exakt var dess olika delar börjar och slutar. Denna uppgift, kallad segmentering, görs vanligtvis eller förfinas av specialister skiva för skiva—en tidskrävande process som kan fördröja beslut och som varierar mellan experter. Automatiska segmenteringsverktyg baserade på djupinlärning har förbättrat situationen, men de mest precisa metoderna kräver ofta stora grafikprocessorer, vilket gör dem svåra att använda direkt i kliniken, särskilt på mindre eller bärbara maskiner.
Två kraftfulla idéer som inte enkelt får plats på små maskiner
Senaste genombrotten inom datorseende kommer främst från två modelldelar. Transformer‑baserade system, till exempel Swin Transformer, är utmärkta på att upptäcka globala mönster över en hel 3D‑skanning och har drivit topppresterande hjärntumörsegmenterare. Deras kärnoperation, självuppmärksamhet, blir dock extremt kostsam när bildstorleken växer, vilket begränsar användningen i realtid eller på kompakt hårdvara. En nyare familj, känd som Mamba och baserad på state‑space‑modeller, erbjuder en smart lösning: den bearbetar sekvenser i i praktiken linjär tid och minskar antalet beräkningar som krävs. Tidiga experiment inom medicinsk bilddiagnostik visade att Mamba‑stilmodeller är snabba och effektiva men vanligtvis halkar efter transformermodeller i segmenteringskvalitet, särskilt för komplexa tumörformer.
Att blanda hastighet och noggrannhet i en design
Författarna ville förena styrkorna från båda världar i en enda 3D‑modell. Deras SwiM‑UNet behåller den välkända U‑formade strukturen som är vanlig inom medicinsk bildbehandling, med en encoder som komprimerar information och en decoder som bygger upp detaljerade segmenteringar. I de tidiga stadierna, där skanningen fortfarande är stor och högupplöst, använder de effektiva Mamba‑block för att hålla beräkningarna rimliga. Längre ner i nätverket, efter att datan har nedprovtagits, byter de till avskalade Swin Transformer‑block som då har råd att modellera långräckta relationer utan att överväldiga hårdvaran. En specialanpassad brygga kallad MS‑adapter länkar dessa två regime. Den betraktar funktioner längs volymens bredd, höjd och djup separat, och även över kanaler, och lär sig genom små grindningsenheter hur mycket varje vy bör påverka den slutliga representationen. 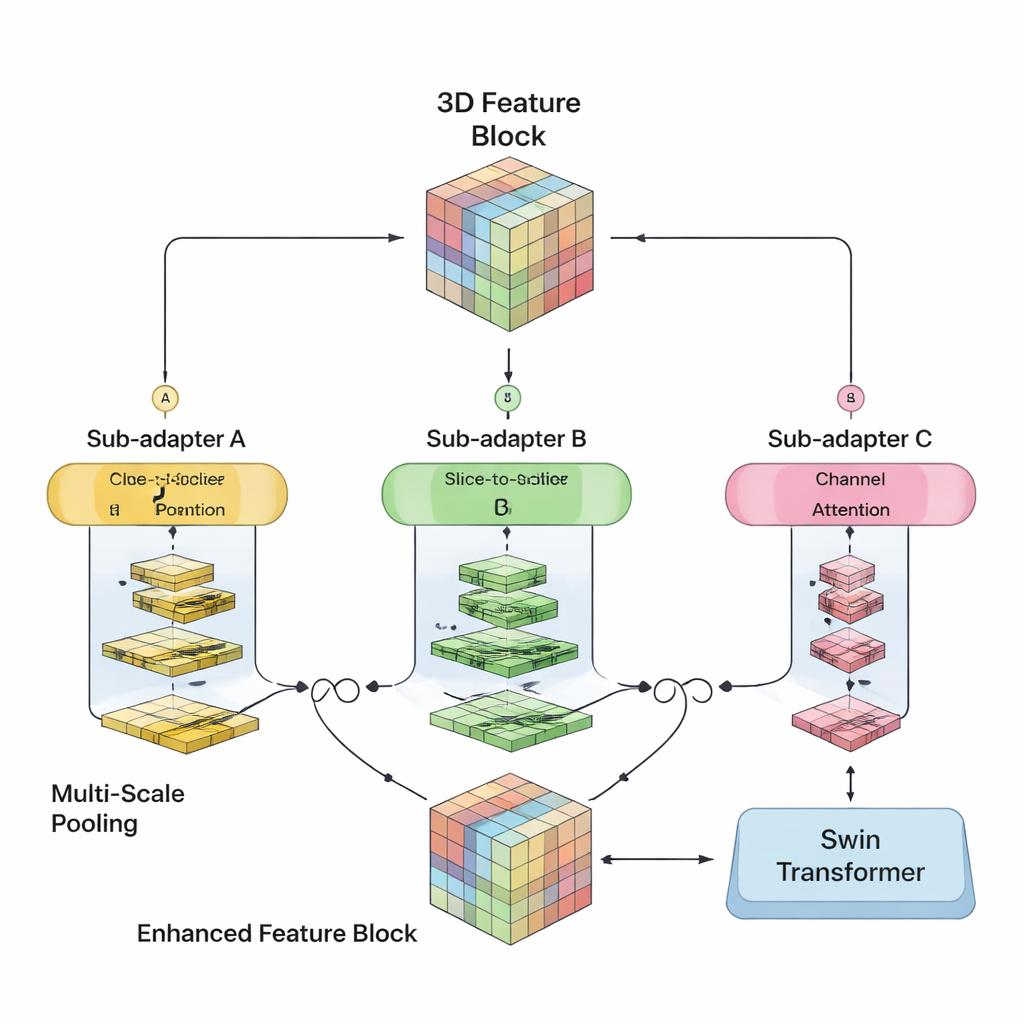
Göra mer med mindre beräkningar
Utöver detta hybrida upplägg minskar teamet överflödiga beräkningar genom att använda låg‑rankade fullt anslutna lager och en decoder som avsiktligt reducerar antalet kanaler den behöver hantera. De testade flera varianter med olika blandningar av Mamba‑ och Swin‑lager och fann att användning av Mamba i de tre första encoder‑stegen och Swin endast i det djupaste steget gav den bästa balansen mellan hastighet och noggrannhet. På två stora offentliga dataset för hjärntumörer från BraTS 2023 och 2024 uppnådde SwiM‑UNet högre noggrannhet och mer precisa gränser än ledande modeller som enbart använder transformer, enbart Mamba eller tidigare hybrider, samtidigt som den använde avsevärt färre flyttalsoperationer och kortade inferenstiden till omkring 45 millisekunder per skanningspatch på ett modernt grafikkort.
Redo för verkliga enheter
För att kontrollera om dessa vinster spelar roll utanför labbet jämförde författarna modellens beräkningskrav med kapaciteterna hos typiska kliniska kant‑system—bärbara MR‑konsoler, datorer för punktavlastning och operationssalens arbetsstationer. Deras analys tyder på att, till skillnad från tyngre transformermodeller, passar SwiM‑UNet bekvämt inom sådana enheters effekt-, minnes‑ och hastighetsgränser och ofta uppfyller kraven för realtidsbruk. Den presterade också väl på ett separat buk‑CT‑dataset, vilket indikerar att angreppssättet kan generalisera bortom hjärntumörer och även bortom MR.
Vad detta betyder för patienter och kliniker
I praktiska termer visar SwiM‑UNet att det är möjligt att närma sig noggrannheten hos de mest sofistikerade segmenteringsmodellerna samtidigt som beräkningarna hålls tillräckligt lätta för användning på enheten. Det kan möjliggöra snabbare, mer konsekventa tumörkonturer på akutmottagningar, i landsbygds‑sjukhus eller mobila bildenheter utan att skicka känsliga bilder till avlägsna servrar. Även om ytterligare arbete krävs för att anpassa metoden till olika skannrar och förhållanden, pekar denna hybriddesign mot en framtid där högkvalitativ bildanalys körs där patienten befinner sig, inte bara i datacenter.
Citering: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Nyckelord: segmentering av hjärntumör, AI för medicinsk bilddiagnostik, hybrida neurala nätverk, inferens på enheten, 3D-MR‑analys