Clear Sky Science · sv
α7-nikotinerga acetylkolinreceptorns roll i att främja M2-makrofagpolarisation vid inflammatoriska platser
Hur nerver hjälper till att lugna okontrollerad inflammation
När vi skär oss i ett finger eller bekämpar en infektion sätter kroppen igång en inflammationsreaktion för att skydda oss. Men om den reaktionen pågår för länge kan den skada frisk vävnad och driva fram kroniska sjukdomar. Denna studie undersöker hur en specifik ”lugnande” receptor på immunceller, kallad α7-nikotinerga acetylkolinreceptorn (α7nAChR), hjälper till att styra inflammationen mot läkning i stället för skada, och ger ledtrådar till nya behandlingar för tillstånd som sepsis, tarmsjukdomar och artrit.
Två sidor av immunsystemets städpatruller
Makrofager är immunceller som fungerar som städ- och reparationslag. De kan växla mellan två huvudlägen. I sitt ”attackerande” läge, ofta kallat M1, utsöndrar de aggressiva ämnen för att döda mikrober och avlägsna skräp. I sitt ”läkande” läge, känt som M2, frigör de dämpande signaler som tystar inflammation och främjar vävnadsreparation. Ett hälsosamt svar börjar med fler M1-celler och övergår sedan gradvis till M2-celler när faran avtar. Författarna ville ta reda på om α7nAChR, en receptor ursprungligen känd för sin roll i nervkommunikation och nikotinets effekter på hjärnan, också hjälper till att styra makrofager mot detta läkande M2-tillstånd under inflammation.
En nervkopplad växel mot läkning
För att undersöka detta använde forskarna möss som antingen hade eller saknade α7nAChR och framkallade inflammation i bukhålan på två sätt: med en bakteriekomponent (som efterliknar infektion) och med försiktig hantering av tarmen (som efterliknar steril kirurgisk skada). De mätte molekylära markörer som skiljer M1 från M2-beteende och använde flödescytometri för att räkna andelen av varje makrofagtyp. Hos normala möss dominerade M1-signaler i det tidiga skedet av inflammationen, men under de följande en till två dagarna steg markörer för M2-celler, vilket speglade en naturlig övergång till reparation. Hos möss som saknade α7nAChR var däremot proinflammatoriska markörer högre, läkningsmarkörer lägre, och andelen M2-makrofager i det inflammerade området var konsekvent reducerad, vilket försköt den lokala balansen mot ett M1-dominerat, mer skadligt tillstånd.
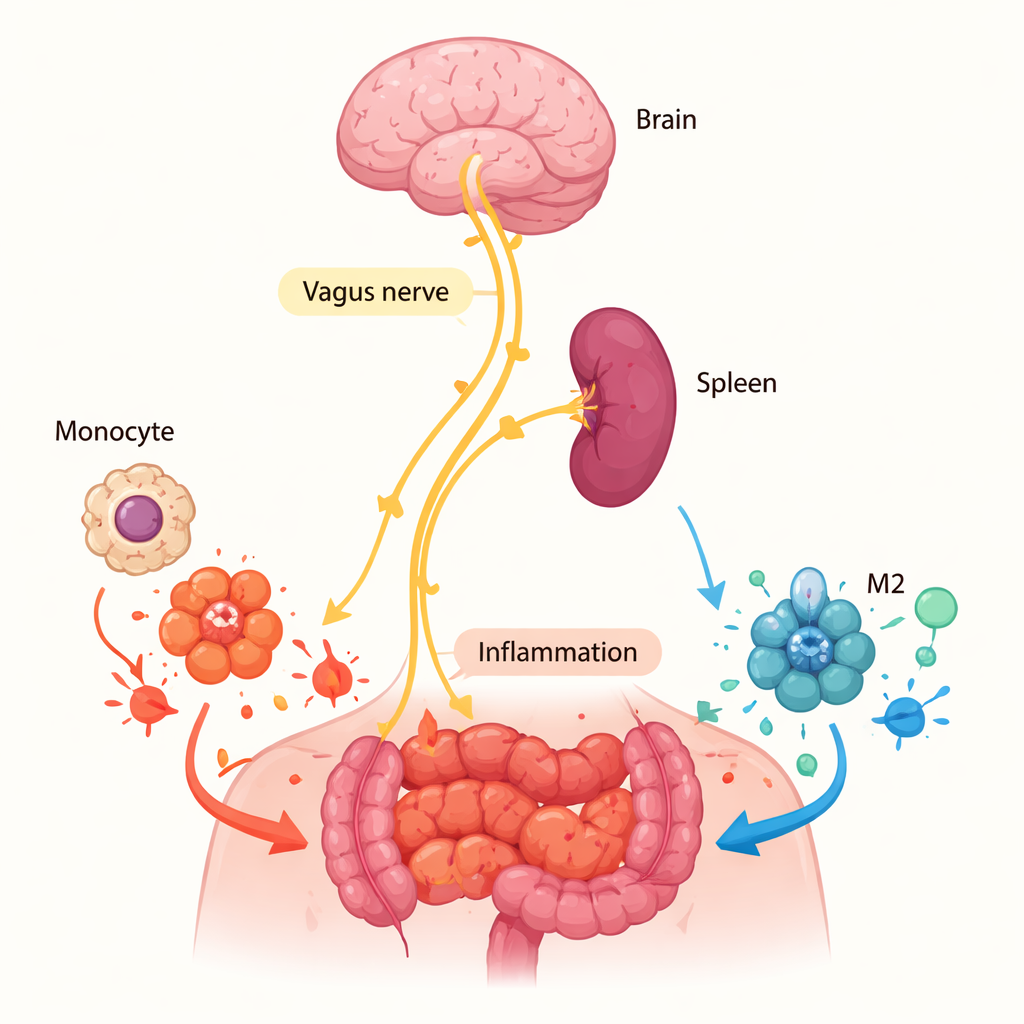
Varför mjälten betyder mer än såret
Nästa fråga var var α7nAChR utförde sitt arbete. Den kunde ha agerat direkt på den inflammerade platsen om lokala celler frigjorde acetylkolin, kemikalien som aktiverar receptorn. Men mätningar av acetylkolin i bukvätska och i cellkulturer från det inflammerade vävnadsområdet var i praktiken obefintliga, vilket talar emot en stark lokal signal. I stället riktades uppmärksamheten mot mjälten, ett centralt immunorgan som redan är känt för att delta i en ”kolinerg anti-inflammatorisk väg” kontrollerad av vagusnerven. När forskarna kirurgiskt avlägsnade mjälten från normala möss och sedan inducerade bukinflammation sjönk andelen M2-makrofager i bukhålan och det totala antalet makrofager föll. Detta mönster speglade vad de såg hos möss utan α7nAChR, vilket tyder på att nervdrivna signaler i mjälten förbereder monocyt—makrofagernas föregångare—att bli M2-celler innan de ens anländer till den inflammerade vävnaden.
Testa växeln i mänskliga celler
För att se om samma receptor kan ställa in mänskliga celler vände forskarna sig till odlingsbara monocyter från en leukemisk cellinje (THP-1) och från donerat mänskligt blod. De styrde dessa celler att utvecklas till antingen M1- eller M2-makrofager med standardimmunstimuli och tillsatte sedan ett specifikt läkemedel som aktiverar α7nAChR. I båda de mänskliga cellkällorna gav aktivering av α7nAChR ingen ökning av M1-markörer men ökade tydligt centrala kännetecken för M2-beteende, inklusive ytproteinet CD206 och den antiinflammatoriska molekylen interleukin-10. Dessa experiment stöder idén att α7nAChR fungerar som en biaserande växel som gör det lättare för utvecklande makrofager att anta en läkande identitet utan att helt slå av immunsvaret.
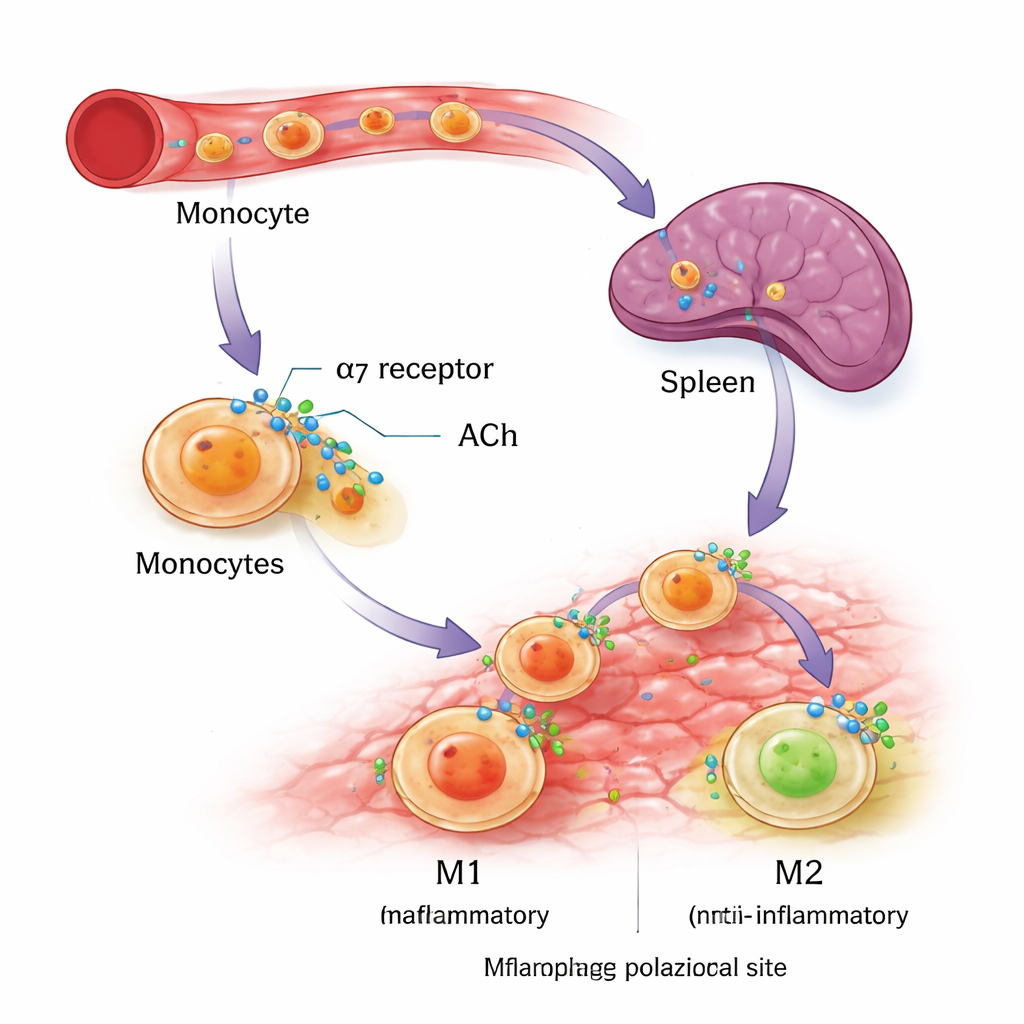
Från nikotinsignaler till framtida terapier
Resultaten hjälper till att förklara flera förbryllande observationer, såsom varför stimulering av vagusnerven kan förbättra inflammatoriska sjukdomar och varför rökare, trots många hälsorisker, verkar ha något lägre risk för vissa tarmsjukdomar—nikotin kan aktivera α7nAChR. Snarare än att bara blockera inflammatoriska kemikalier verkar α7nAChR hjälpa kroppen att omvandla sina immunstädpatruller till mer reparationsfokuserade M2-celler, särskilt genom mjältebaserad utbildning av monocyter. För en lekman betyder detta att vårt nervsystem gör mer än att känna smärta eller kontrollera muskler; det vägleder också tyst immunceller när de ska bekämpa och när de ska läka. Att lära sig att säkert slå om denna inbyggda växel med läkemedel eller riktad nervstimulering kan öppna nya sätt att lugna skadlig inflammation samtidigt som kroppens förmåga att försvara sig bevaras.
Citering: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Nyckelord: makrofagpolarisation, inflammation, vagusnerv, nikotinerga acetylkolinreceptorn, immunreglering