Clear Sky Science · sv
Fysiologiskt relevanta former av Tc‑ och Re‑pyrofosfat radioaktiva spårämnen och grunden för deras transthyretin‑amyloidkänslighet
Varför denna hjärtavbildningshistoria är viktig
Många utvecklar tysta avlagringar av missveckade proteiner, så kallade amyloider, i hjärtat när de åldras. Några av dessa avlagringar, särskilt de som består av ett blodprotein som heter transthyretin, kan göra hjärtat stelare och leda till allvarlig sjukdom. Läkare förlitar sig i allt högre grad på ett radioaktivt spårämne känt som technetium‑99m pyrofosfat (99mTc‑PYP) för att se dessa avlagringar på skanningar. Ändå har det visat sig överraskande oklart vilken exakt form detta spårämne antar i kroppen och varför det verkar "föredra" vissa amyloidtyper. Denna artikel kombinerar teori och experiment för att avslöja hur spårämnet verkligen ser ut under levande‑liknande förhållanden och hur den formen kan göra att det söker sig till skadliga transthyretin‑fibriller.
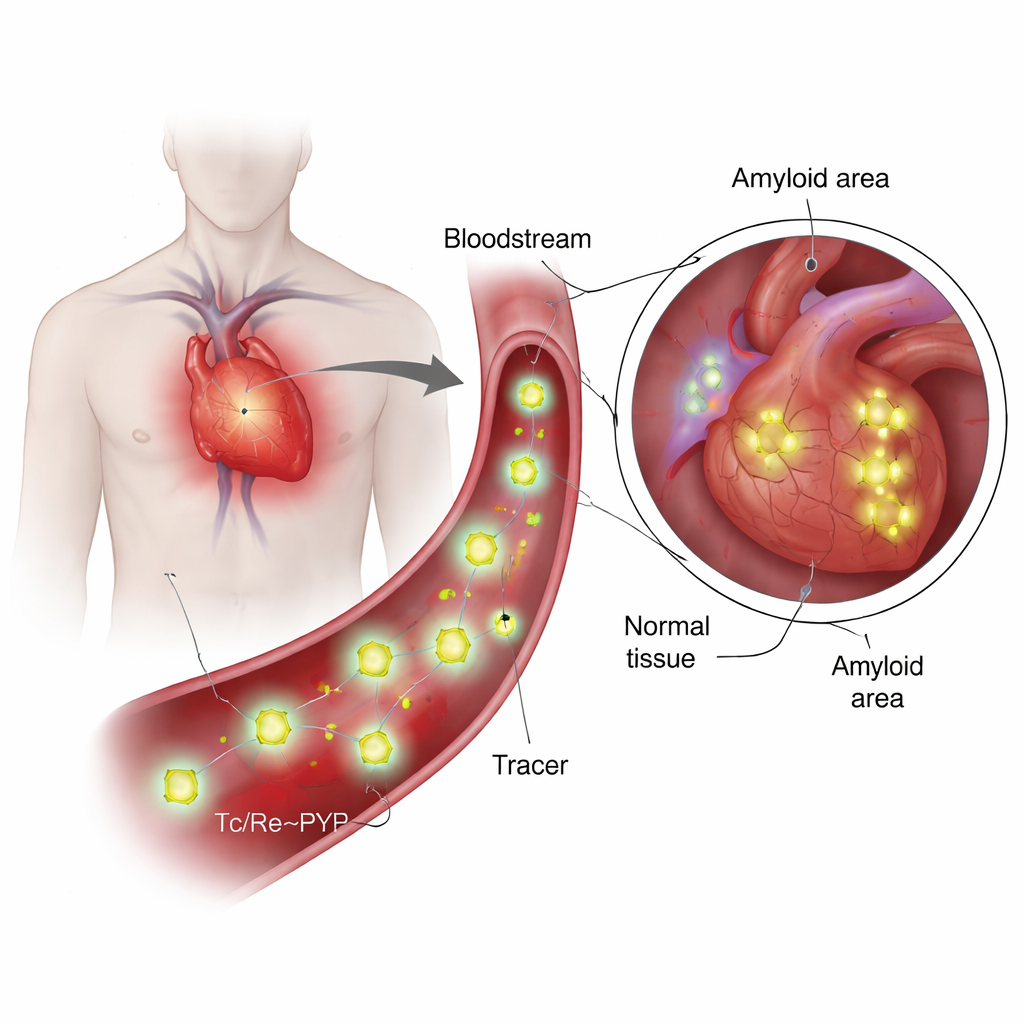
Vad är dessa spårämnen och varför är de speciella?
99mTc‑PYP har använts i årtionden för att avbilda ben, eftersom det tenderar att samla sig där kalcium och mineralomsättning är hög. Mer nyligen upptäckte läkare att det också kan skilja mellan två huvudtyper av kardiell amyloidos: en uppbyggd av antikropps‑lätta kedjor (AL) och en av transthyretin (ATTR). Vid ATTR lyser hjärtat ofta starkt på PYP‑skanningar, medan AL‑fall ofta förblir svaga, även när kalciumbildningen ser liknande ut. Denna mismatch väckte en viktig fråga: sitter spårämnet bara på kalcium, eller interagerar det direkt med amyloidproteinet självt? Att besvara det kräver kunskap om spårämnets verkliga kemiska struktur under blodliknande förhållanden, något tidigare arbete endast skisserat i grova drag.
Använda en säkrare ersättare för att se det osynliga
Eftersom technetium är radioaktivt och förekommer endast i små mängder i medicinska preparat är det svårt att studera direkt med många laboratorietekniker. Författarna använde därför rhenium, ett nära besläktat element med nästan identisk storlek och bindningspreferenser men mer praktisk kemi, som ersättare. De framställde rhenium‑pyrofosfatblandningar under förhållanden som efterliknar kliniska PYP‑kit och undersökte dem med en uppsättning verktyg: högnivå kvantkemiska beräkningar, UV‑vis spektrala mätningar, olika vibrationsspektroskopier (infrarött och Raman), kärnmagnetisk resonans, masspektrometri och tenn Mössbauer‑spektroskopi. Tillsammans tillät dessa metoder dem att testa många kandidatstrukturer och begränsa vilka arter som sannolikt existerar vid neutral pH, som i blodet.
En flexibel men igenkännbar molekylform
Den samlade evidensen pekar på en gemensam "kärnstruktur": ett oktaedriskt komplex där ett technetium‑ eller rheniumatom i oxidationstillstånd +4 är bundet till två pyrofosfatgrupper och två vattenmolekyler. Enkelt uttryckt sitter metallen i centrum av ett nästan oktaedriskt burformat arrangemang av syreatomer, där pyrofosfaterna fungerar som flertandade ankare och vattenmolekylerna upptar de återstående positionerna. Denna grundläggande diaqua‑dipyrofosfat‑enhet är inte styv. Eftersom pyrofosfatarmarna kan vrida sig och bilda interna vätebindningar med de bundna vattnen, provar molekylen många något olika former i lösning. Beräkningar och spektra antyder att dessa variationer förskjuter dess ljusabsorptions‑ och vibrationssignaturer, vilket förklarar varför experimentella band är breda och varför tidigare studier haft svårt att fastställa en enda ren struktur.
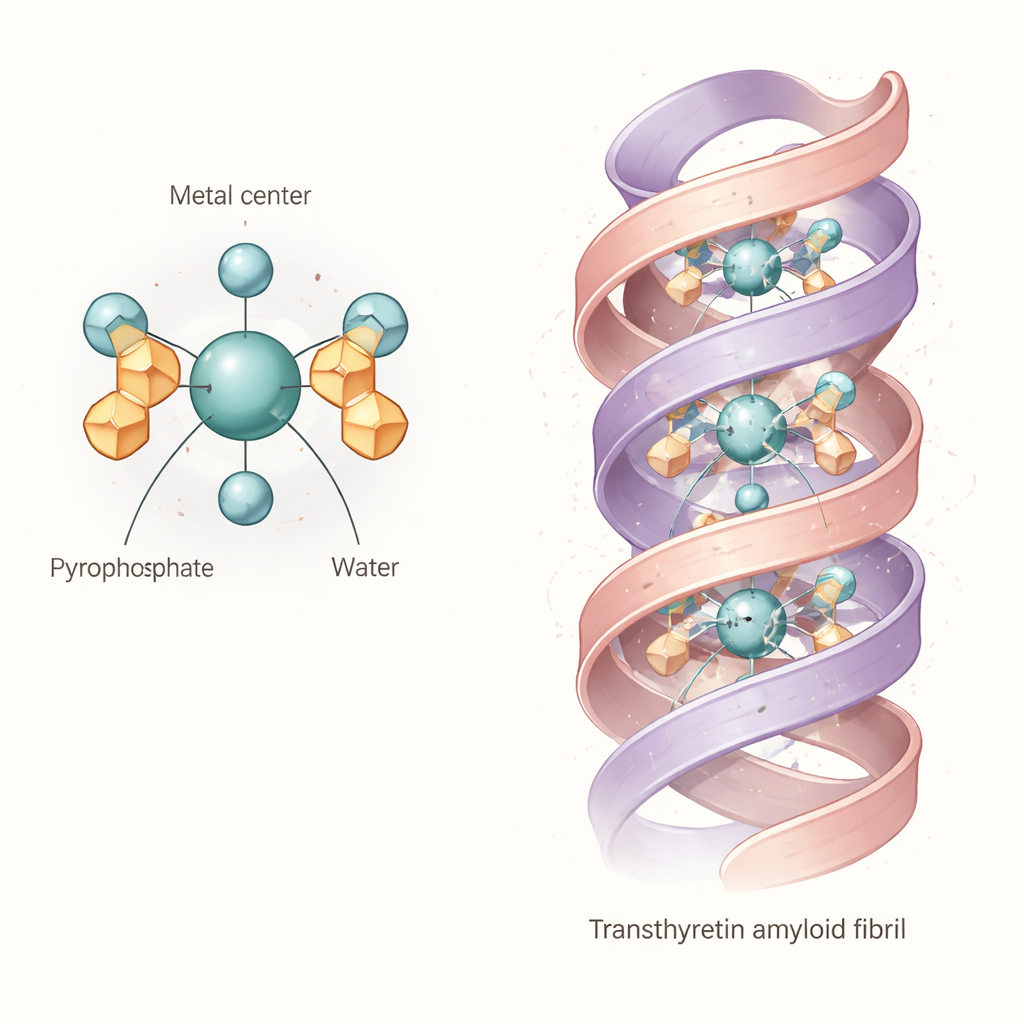
Vad detta betyder för bindning till hjärt‑amyloid
Författarna frågade sedan om detta flexibla komplex rimligen skulle kunna passa in direkt i transthyretin‑amyloidfibriller. Med hjälp av en detaljerad kryo‑elektronmikroskopistruktur av en human transthyretin‑fibrill utförde de datorbaserade dockningssökningar med den modellerade technetium‑pyrofosfatenheten. Resultaten visar att diaqua‑dipyrofosfat‑enheten kan passa in i en central kanal som löper längs fibrillen, och bilda flera vätebindningar och saltbryggor med laddade sidokedjor som kantar kaviteten. Detta tyder på att, åtminstone för vissa transthyretinfibrillformer, sitter spårämnet inte bara på närliggande mineralavlagringar; det kan vara direkt omfamnad av proteinets skelett. Den strukturella "give" i spårämnet hjälper sannolikt det att anpassa sig till något olika fickor och laddningsmönster i verkliga patientfibriller.
Konsekvenser för diagnostik och framtida spårämnen
För en lekmannaläsare är slutsatsen att den vida använda PYP‑hjärtundersökningen bygger på ett spårämne som är mer subtilt och proteinmedvetet än man tidigare trott. Under fysiologiska förhållanden är det bäst att betrakta det som en liten, vattenbärande metall‑pyrofosfatbur som kan flexa och bilda flera kontaktpunkter med transthyretin‑amyloidkanaler. Denna insikt hjälper till att förklara varför spårämnet ger starka signaler vid vissa amyloidsjukdomar men inte andra, och varför små förändringar i proteinet eller dess omgivning kan orsaka förvirrande förluster av känslighet. Genom att klargöra spårämnets arbetssätt och laddningsmönster lägger studien en grund för att designa nästa generations avbildnings‑ eller terapeutiska medel som mer selektivt känner igen sjukdomsorsakande fibriller i hjärtat och bortom.
Citering: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Nyckelord: kardial amyloidos, transthyretin, technetium‑pyrofosfat, molekylär avbildning, radiotrackerkemi