Clear Sky Science · sv
HIV Vpr orsakar demetylisering av SNCA antisense-promotor, vilket leder till neurokognitiv försämring
Varför HIV fortfarande kan påverka hjärnan
Personer som lever med HIV blir allt äldre och lever friskare liv tack vare moderna antiretrovirala läkemedel. Ändå upplever många fortfarande problem med minne, koncentration och rörelse, även när viruset i blodet är väl kontrollerat. Denna studie undersöker varför detta sker genom att zooma in på ett litet viral protein, kallat Vpr, och ett hjärnprotein, alfa‑synuklein, som också är centralt vid Parkinsons sjukdom. Att förstå hur dessa två molekyler samverkar kan avslöja varför HIV kan påskynda hjärnans åldrande och föreslå nya sätt att skydda hjärnan.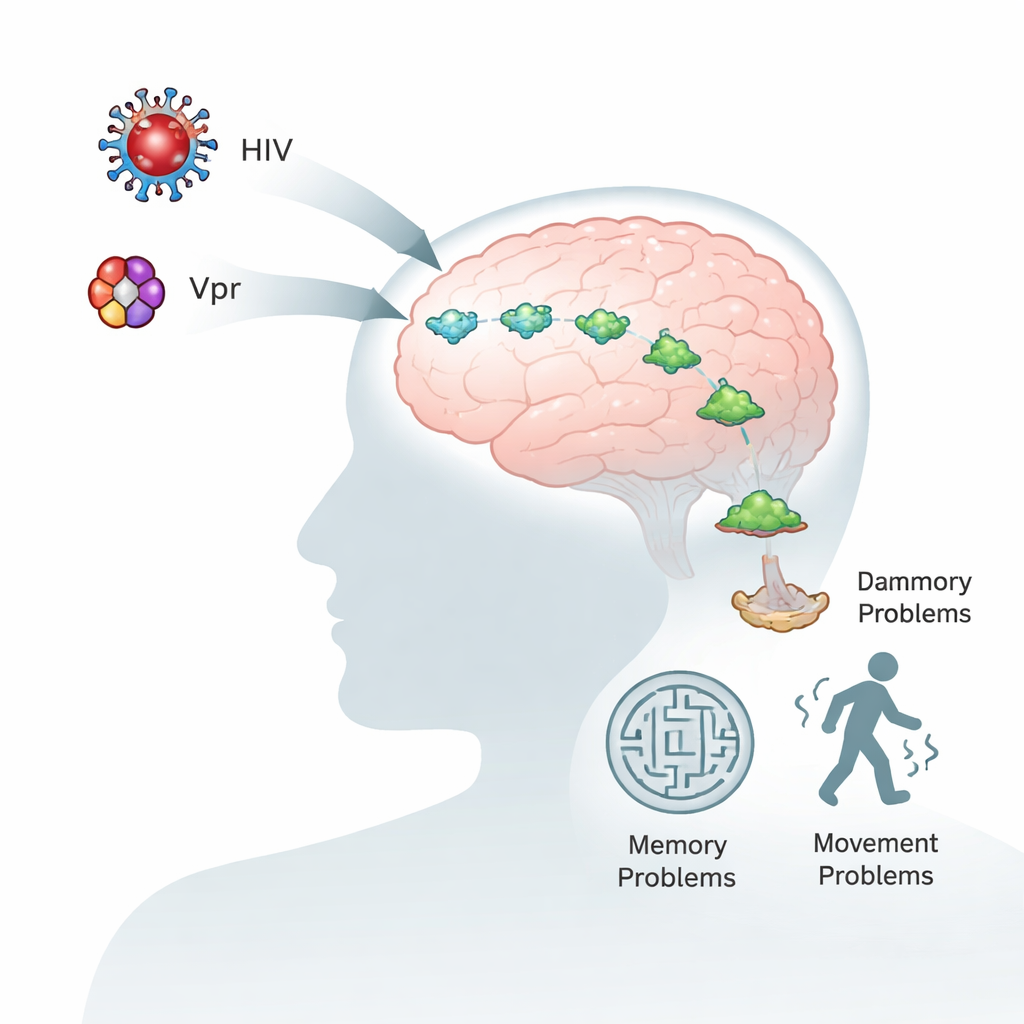
Ett hjärnprotein i skärningspunkten mellan HIV och Parkinson
Alfa‑synuklein är ett protein som hjälper nervceller att kommunicera, särskilt i hjärnregioner som styr rörelse och minne. När för mycket alfa‑synuklein ansamlas, bildar det klumpar som skadar synapser, belastar energiproducerande mitokondrier och driver inflammation. Sådana klumpar är ett kännetecken för Parkinsons sjukdom. Författarna visar att alfa‑synuklein också ökar med normalt åldrande hos möss, och att HIV:s Vpr‑protein driver dess nivåer ännu högre i nervliknande celler. Detta placerar alfa‑synuklein i skärningspunkten mellan HIV‑relaterade kognitiva problem och klassiska rörelsestörningar.
Hur ett virusprotein skriver om cellens "interpunktion"
Varje cell använder kemiska märkningar på DNA—ofta beskrivna som molekylära interpunktionsmarkörer—för att slå på eller av gener. I detta arbete fokuserade teamet på en mindre känd kontrollbrytare inne i alfa‑synuklein‑genen kallad antisense‑promotorn. I friska celler är denna brytare kraftigt märkad med metylgrupper, vilket håller den relativt tyst. Forskarna fann att Vpr avlägsnar dessa märkningar vid specifika platser i detta område, en process känd som demetylisering. När dessa markörer tas bort blir antisense‑promotorn mer aktiv och driver ökad produktion av alfa‑synuklein, vilket banar väg för skadlig aggregering.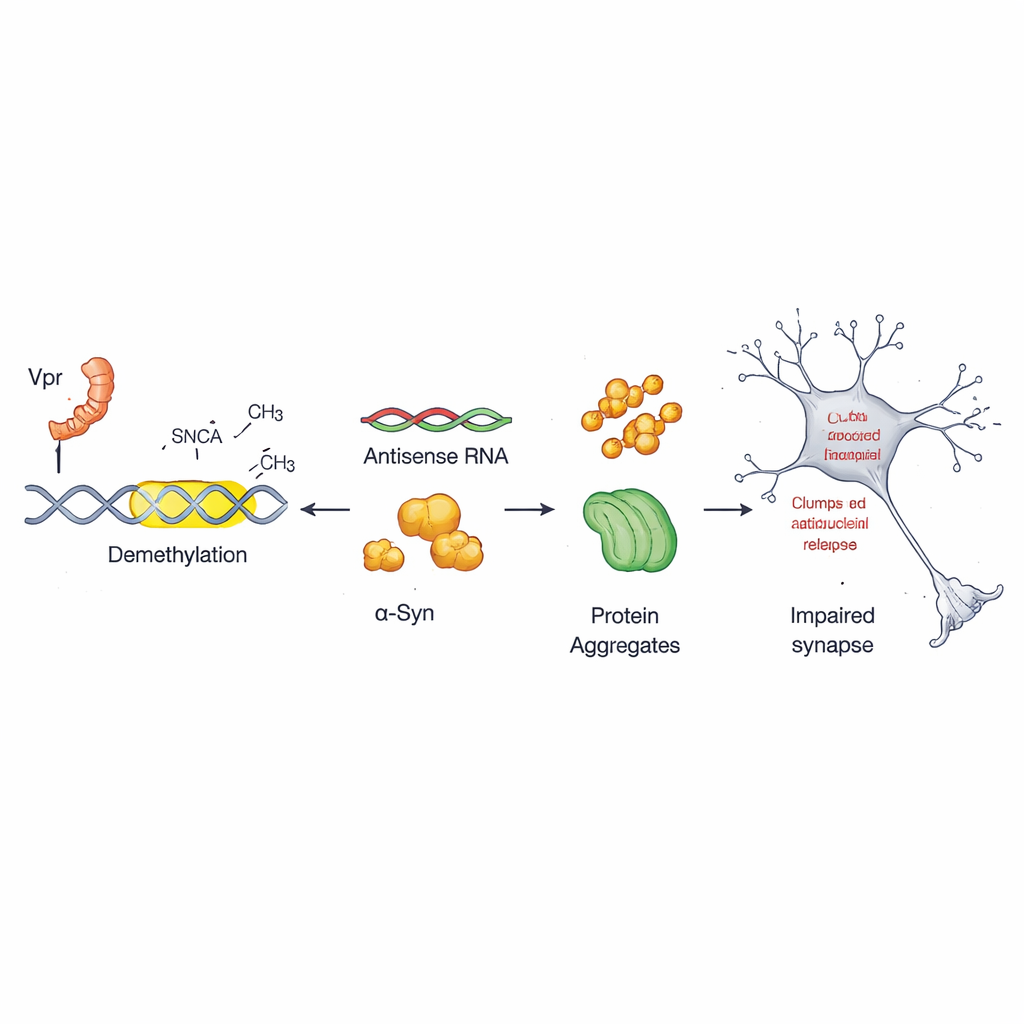
Bevis från celler, möss och mänskliga hjärnor
Genom att använda odlade mänskliga nervliknande celler och primära musneuroner visade författarna att tillsats av Vpr ökar alfa‑synukleins budbärar‑RNA‑nivåer och proteinmängd över tid. Ett läkemedel som generellt främjar DNA‑demetylisering efterliknade några av dessa effekter, vilket underströk epigenetisk kontrolls roll. I kontrast förhindrade en förening kallad DMOG, som blockerar demetyliserande enzymer, att Vpr fullt ut aktiverade antisense‑promotorn. Teamet studerade sedan mänskliga hjärnprover från personer med och utan HIV. Hjärnor från HIV‑positiva donatorer—både före och efter antiretroviral behandling—hade färre metylmärken i samma DNA‑region och högre nivåer av alfa‑synuklein och dess antisense‑transkript, särskilt hos donatorer med HIV‑relaterad demens. Detta tyder på att viruset lämnar ett bestående epigenetiskt ärr i hjärnan.
Från molekylära förändringar till minnesproblem
För att koppla dessa molekylära skiften till beteende undersökte forskarna hur Vpr påverkar hjärnkretsar hos möss. När de applicerade Vpr på skivor av mushippocampus, en region viktig för minne, var den grundläggande signalstyrkan mellan neuroner oförändrad, men förmågan att stärka kopplingar—en process kallad långtidspotentiering—minskade. I levande möss ledde riktade injektioner av Vpr i hippocampus till sämre prestation i en rumslig minnesuppgift där djuren måste komma ihåg objektens placering. Tillsammans tyder dessa experiment på att Vpr‑drivna alfa‑synuklein‑förändringar inte bara är biokemiska nycker; de översätts till försvagade synapser och mätbara minnesnedsättningar.
Vad detta betyder för personer som lever med HIV
Denna studie föreslår en tydlig händelsekedja: HIV frigör Vpr, Vpr omprogrammerar en nyckel‑DNA‑brytare som kontrollerar alfa‑synuklein, proteinet ansamlas och klumpar sig, och neuroner förlorar gradvis förmågan att kommunicera och stödja minne. Eftersom liknande alfa‑synuklein‑problem ligger till grund för Parkinsons sjukdom antyder arbetet att HIV och klassiska neurodegenerativa sjukdomar delar överlappande mekanismer. Viktigt är att fynden lyfter fram möjliga nya strategier—såsom läkemedel som stabiliserar DNA‑metylering vid antisense‑promotorn eller begränsar alfa‑synuklein‑ansamling—för att bromsa eller förhindra HIV‑relaterad kognitiv nedgång och rörelseproblem.
Citering: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Nyckelord: HIV-relaterade neurokognitiva störningar, alfa-synuklein, epigenetik, DNA-metylation, Parkinson-liknande symtom