Clear Sky Science · sv
Undersökning av Acoramidis-baserade jonvätskor som potentiella stabilisatorer av transthyretin med DFT-beräkningar, molekylär dockning och ADMET-studier
Varför ett piller mot en sällsynt hjärtsjukdom är så svårt att ta fram
Transthyretin-amyloidos (ATTR) är en allvarlig sjukdom där ett blodprotein ansamlas i hjärtat och nerverna och gradvis skadar dem. Ett nytt läkemedel, Acoramidis, kan hjälpa till att stoppa denna ansamling, men det finns ett praktiskt problem: läkemedlet löser sig dåligt i vatten, vilket försvårar kroppens upptag när det tas som piller. Denna studie utforskar ett smart sätt att omforma Acoramidis till nya saltliknande former, kallade jonvätskor, som skulle kunna göra läkemedlet lättare att svälja och mer effektivt.
Att göra ett lovande läkemedel drickbart
För att ett piller ska fungera måste det först lösa sig i mag- och tarmvätskorna och sedan passera tarmväggen in i blodomloppet. Acoramidis är effektivt på att stabilisera transthyretin (TTR)-proteinet, vilket hjälper till att förhindra skadliga proteinansamlingar kopplade till ATTR, men det är dåligt lösligt och har svag oral biotillgänglighet. Forskarna tog sig an detta genom att kemiskt para ihop Acoramidis med olika laddade partnermolekyler och skapade tre nya jonvätskepreparat (IL1, IL2 och IL3). Dessa versioner är designade för att bete sig mer som flytande salter än som styva kristaller, vilket potentiellt kan öka läkemedlets löslighet och spridning i kroppen. 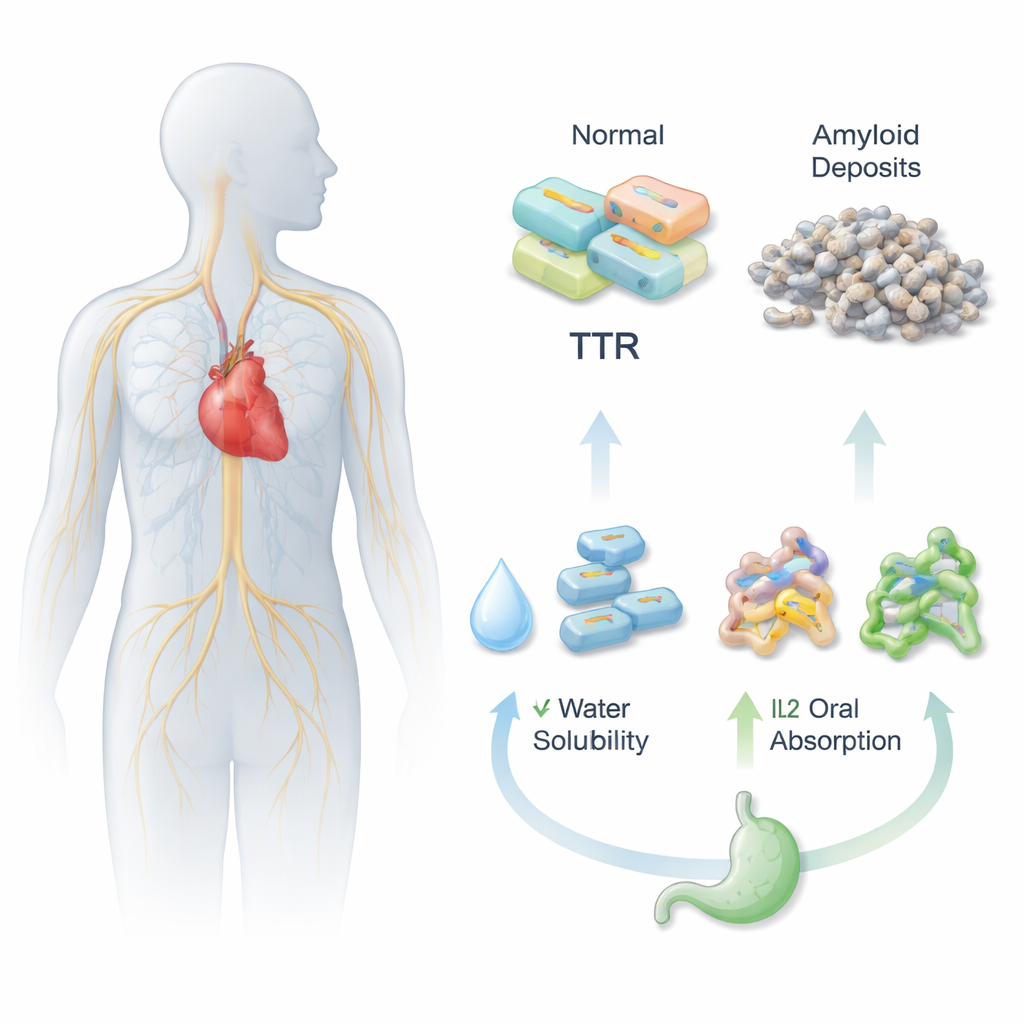
Undersöka de nya molekylerna på en dator
I stället för att gå direkt till djur- eller mänskliga försök använde teamet avancerade datormetoder för att förutsäga hur dessa nya former skulle bete sig. Kvantkemiska beräkningar uppskattade hur polär varje molekyl är — en viktig indikator på vattenlöslighet — och hur lätt dess elektroner kan förskjutas, vilket relaterar till hur den kan interagera med proteiner. IL1 stack ut med högst dipolmoment och starkast elektronisk responsivitet, vilket tyder på att den bör lösa sig bättre i vatten och bilda starkare, mer flexibla kontakter med sina mål. Energiberäkningarna antydde också att IL1 är mer termiskt stabil än ursprungsdrogen och de andra två jonvätskorna, vilket betyder att den bör vara mindre benägen att falla sönder innan den når sitt mål.
Hur hårt läkemedlet kan hålla sitt mål
Nästa steg var att använda molekylär dockning, ett virtuellt "lås-och-nyckel"-test, för att se hur väl Acoramidis och dess tre jonformer passar i bindningskanalen på TTR-proteinet. Alla fyra föreningarna dockade i rätt region av TTR, men IL1 bildade det tätaste greppet med mest fördelaktig bindningsenergi och flera stabiliserande kontakter — särskilt vätebindningar — med viktiga aminosyror i proteinet. Denna starkare bindning antyder att IL1 kan vara ännu bättre än moderläkemedlet på att hålla TTR i sin säkra, fyrdelade struktur och sålunda hjälpa till att förhindra den farliga sönderfallet och felveckningen som leder till amyloida depositioner.
Kommer kroppen att ta upp och rensa dessa nya former?
Slutligen använde teamet nätbaserade farmakologiska verktyg för att undersöka hur kroppen kan hantera dessa föreningar — hur väl de löser sig, passerar tarmväggen, cirkulerar i blodet och slutligen elimineras. Alla tre jonvätskorna förutspåddes vara mer vattenlösliga än Acoramidis, där IL3 visade den högsta råa lösligheten. Mått på tarmpermeabilitet och total oral absorption förbättrades för samtliga jonvätskor, med IL1 och IL2 som gav den bästa balansen mellan tarmgenomträngning och förväntad biotillgänglighet. Proteinbindning i blod, rensningshastigheter och halveringstider förändrades också på sätt som tyder på att jonvätskeformerna skulle kunna ge mer tillförlitlig exponering efter oral dosering, där IL1 återigen visade en särskilt fördelaktig profil. 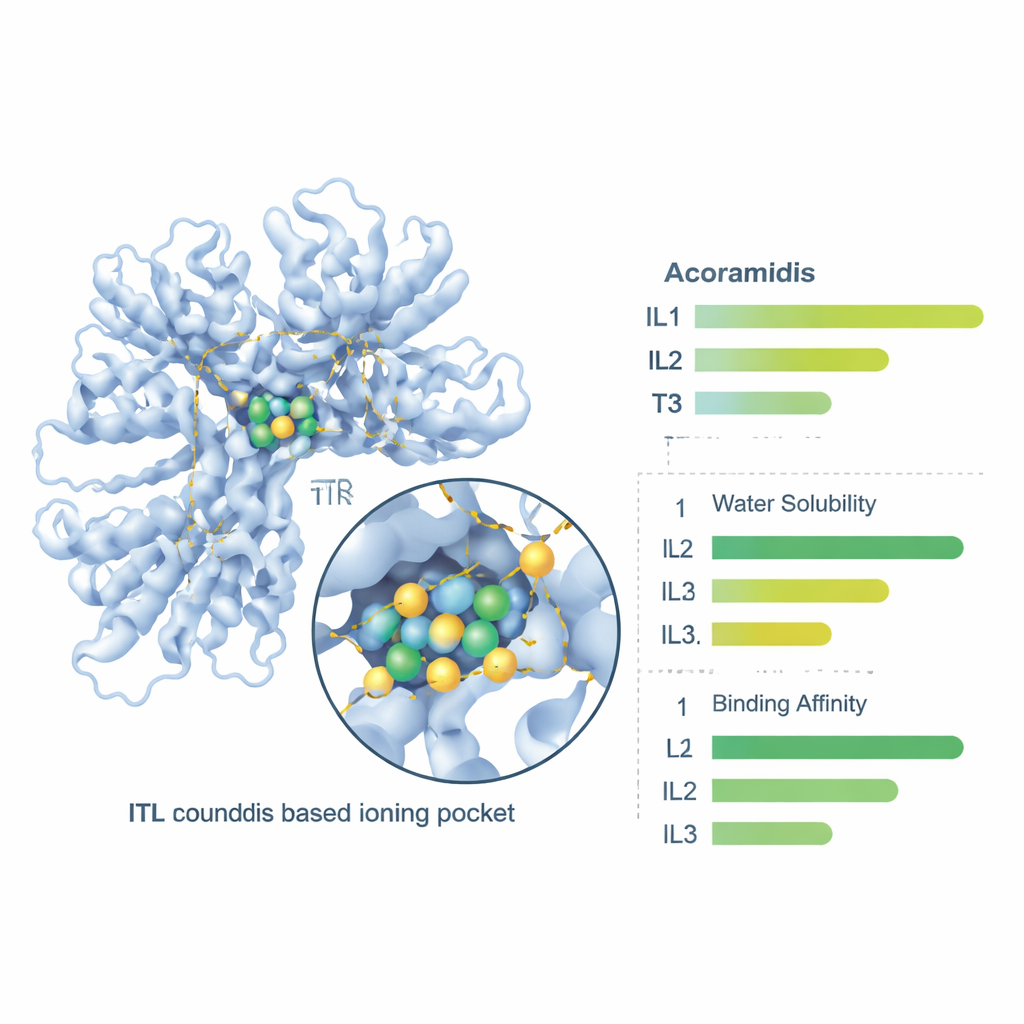
Vad detta kan innebära för framtida ATTR-behandlingar
För en icke-specialist är huvudbudskapet att läkemedlet Acoramidis redan verkar lovande för en sällsynt men allvarlig hjärt- och nervsjukdom, men dess dåliga löslighet begränsar hur väl det kan fungera peroralt. Genom att omvandla Acoramidis till särskilt designade jonvätskor visar denna studie — helt genom datorbaserade tester — att det kan vara möjligt att skapa versioner som löser sig bättre, binder starkare till sitt proteinmål och absorberas mer effektivt. Bland de tre kandidaterna verkar IL1 hitta den bästa balansen mellan stabilitet, bindningsstyrka, löslighet och förväntat oralt upptag, vilket gör den till en stark kandidat för framtida laboratorie- och klinisk utveckling med målet att leverera mer effektiva, lättanvända behandlingar för ATTR.
Citering: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Nyckelord: transthyretin-amyloidos, Acoramidis, jonvätskor, proteinfelveckning, oral läkemedelsleverans