Clear Sky Science · sv
In silico‑design av ett multi‑epitopevaccin riktat mot DENV‑1 och DENV‑3
Varför denguevacciner fortfarande spelar roll
Denguefeber är inte längre en sällsynt tropisk sjukdom; den hotar nu miljarder människor i mer än 100 länder och överbelastar regelbundet sjukhus i delar av Asien, Latinamerika och andra regioner. Trots att två licensierade vaccin finns på marknaden är skyddet ojämnt, särskilt för personer som aldrig tidigare haft dengue och i områden där flera virustyper cirkulerar samtidigt. Denna studie ställer en aktuell fråga: kan datorstyrd design hjälpa oss att bygga ett säkrare, mer precist vaccin, särskilt inriktat på farliga samtidigainfektioner med två dengue‑typer som ofta förekommer tillsammans?
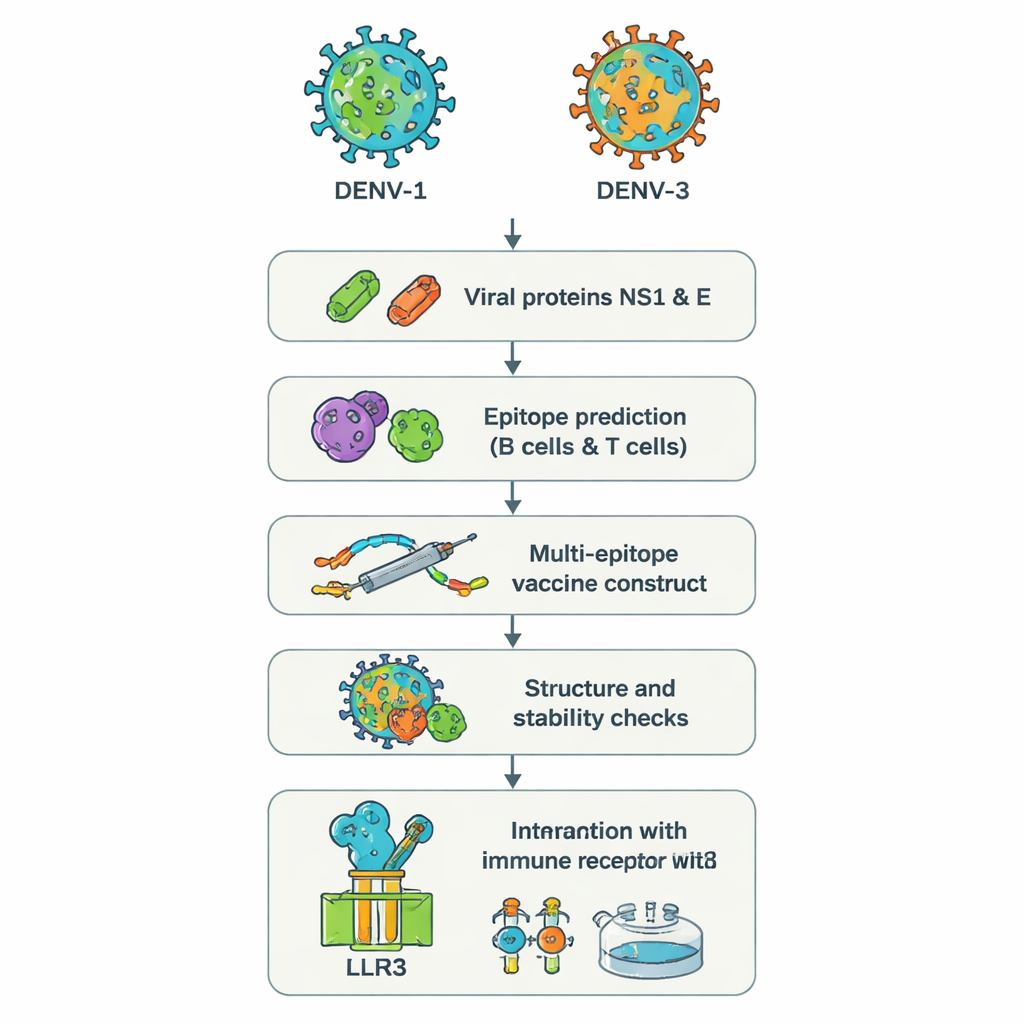
Två listiga virustyper och varför de är ett problem
Denguevirus förekommer i fyra varianter, kallade serotyper DENV‑1 till DENV‑4. Infektion med någon av dem kan orsaka hög feber, svår smärta och i vissa fall livshotande blödningar eller chock. Oroande nog kan en andra infektion med en annan serotyp ibland göra sjukdomen värre snarare än bättre, eftersom befintliga antikroppar kan underlätta för det nya viruset att ta sig in i celler — en process som kallas antikroppsberoende förstärkning. Vid nyliga utbrott har läkare rapporterat patienter som samtidigt infekterats med DENV‑1 och DENV‑3, en kombination som kopplats till allvarligare sjukdom och förvirrande laboratorieresultat. Nuvarande vaccin skyddar inte alltid tillförlitligt alla åldersgrupper och alla serotyper, särskilt personer utan tidigare exponering, vilket lämnar en farlig lucka i försvarslinjen.
Att designa ett vaccin från molekylen uppåt
I stället för att odla hela virus i laboratoriet använde forskarna en metod som ibland kallas ”reverse vaccinology”. De utgick från de genetiska sekvenserna för två dengueproteiner, NS1 och E, från DENV‑1 och DENV‑3. Dessa proteiner är centrala för hur viruset invaderar celler och hur immunsystemet uppfattar det. Kraftfulla webb‑baserade verktyg genomsökte proteinsekvenserna för att hitta korta segment — epitoper — som sannolikt känns igen av mänskliga B‑celler (som bildar antikroppar) och T‑celler (som dödar infekterade celler och koordinerar svar). Av hundratals kandidater valde teamet ett litet urval som förutspåddes vara tydligt synliga för immunsystemet, delade mellan de två serotyperna och kapabla att utlösa hjälpsamma antivirala signaler såsom interferon‑gamma.
Bygga ett enda multifunktionellt vaccinmolekyl
De valda epitoperna sattes därefter digitalt ihop till ett lång artificiellt protein, ett så kallat ”multi‑epitope”‑vaccin. Korta aminosyralänkar fungerar som flexibla mellanrum så att varje epitop behåller sin form och förblir åtkomlig för immunceller. En extra bit, baserad på en naturlig mänsklig antimikrobiell peptid kallad beta‑defensin, lades till som adjuvans för att förstärka det övergripande svaret. Datordrivna analyser förutspådde att den slutliga konstruktionssekvensen, innehållande 575 aminosyror, skulle vara stabil, vattenälskande (och därmed lättare att lösa) och osannolik att verka som ett allergen. Ytterligare strukturförutsägande verktyg genererade en tredimensionell modell och kontrollerade att de flesta byggstenarna satt i realistiska positioner, liknande dem som ses i kända proteinstrukturer.
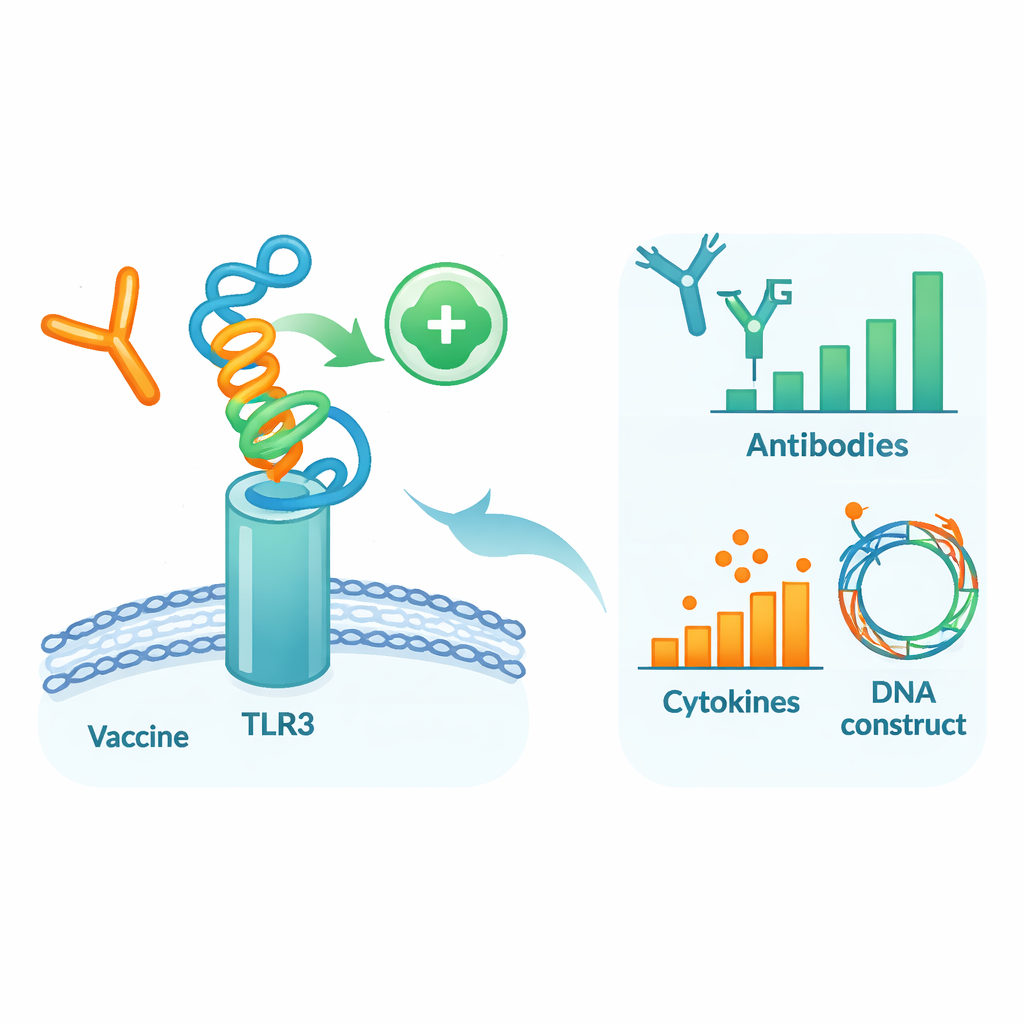
Testa kandidaten i en virtuell kropp
För att se hur detta designade protein skulle kunna bete sig i en människoliknande miljö utförde författarna en serie detaljerade datorsimuleringar. Först dockade de vaccinmodellen mot TLR3, ett sensorprotein på immunceller som upptäcker virusmaterial och hjälper till att initiera tidiga försvar. Molekylärdynamiksimuleringar — virtuella filmer av atomer i rörelse — föreslog att vaccinet och TLR3 bildar ett stabilt komplex, understött av gynnsamma bindningsenergier och många vätebindningar. Ytterligare analyser av rörelse och energi pekade ut specifika regioner i båda molekyler som fungerar som kontakt‑”hotspots”. Därefter användes en immunsystems‑simulator för att efterlikna tre vaccindoser över flera månader. Det virtuella immunsystemet producerade starka vågor av skyddande IgG‑antikroppar, långlivat B‑ och T‑cellsminne samt signalmolekyler förenliga med ett robust antiviralt svar.
Från datormodell till laboratoriefärdig plan
Slutligen anpassade forskarna vaccinets genetiska kod för effektiv produktion i vanliga laboratoriemikrober och placerade framgångsrikt denna optimerade DNA‑sekvens i en standard uttrycksplasmid, redo för framtida experimentella tester. I enkla termer levererar deras arbete en detaljerad ritning för ett nytt denguevaccin som riktar in sig på noggrant utvalda delar av DENV‑1 och DENV‑3, förutspås vara stabilt och säkert och bör kraftigt engagera båda armarna av immunsystemet. Även om dessa resultat är helt beräkningsbaserade och måste bekräftas i celler, djur och så småningom människor, visar de hur modern bioinformatik snabbt kan generera skräddarsydda vaccinkandidater för komplexa problem som dengue‑samtidsinfektioner.
Citering: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Nyckelord: denguevaccin, multi‑epitop, DENV‑1, DENV‑3, immunoinformatik