Clear Sky Science · sv
Integrativ analys av proteomik och metabolomik avslöjar störningar i aminosyrametabolismen i adriamycin‑resistenta akuta myeloiska leukemiceller
Varför vissa leukemiläkemedel slutar fungera
Kemoterapi har förändrat behandlingen av akut myeloisk leukemi (AML), en snabbt växande blodcancer. Ändå återkommer sjukdomen hos många patienter eftersom cancercellerna lär sig överleva de läkemedel som är avsedda att döda dem. Denna studie ställer en enkel men avgörande fråga: vad förändras inne i leukemiceller när de blir resistenta mot adriamycin, ett av standardkemoterapimedlen, och kan dessa förändringar peka på nya sätt att återställa läkemedlets effekt?
En titt inuti leukemiceller
För att undersöka detta jämförde forskarna en vanlig human AML‑cellinje, kallad HL60, med en systerlinje som gjorts resistent mot adriamycin (HL60/R). I stället för att titta på en enda gen eller ett enda protein i taget använde de två breda, kompletterande angreppssätt. Proteomik mätte tusentals olika proteiner — cellens arbetsmolekyler som utför de flesta uppgifter. Metabolomik mätte hundratals små molekyler som utgör cellens ämnesomsättning, inklusive fetter, sockerarter och aminosyror. Genom att kombinera dessa omik‑lager byggde teamet en detaljerad bild av hur resistenta celler skiljer sig från sina fortfarande känsliga motsvarigheter.
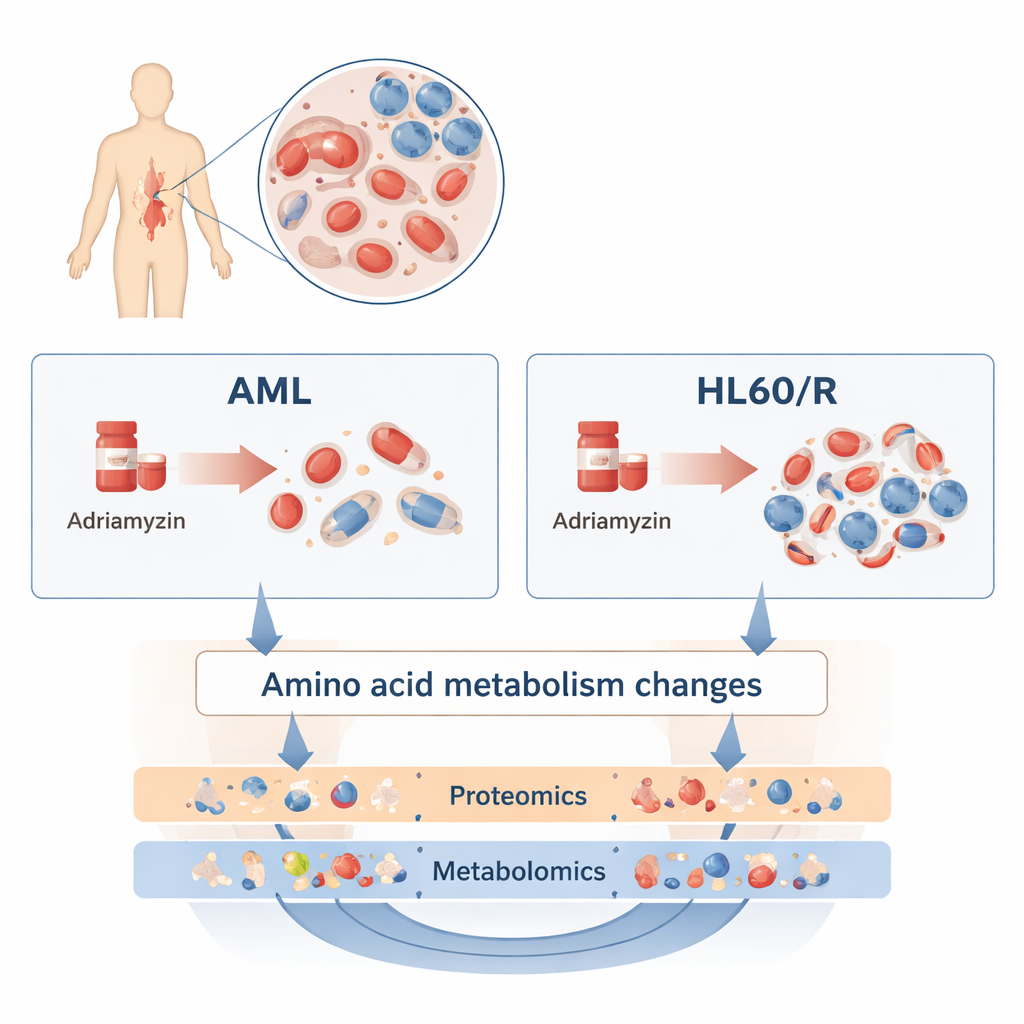
Omfattande omprogrammering av cellens maskineri
Proteomikstudien avslöjade omfattande förändringar: mer än 3 200 proteiner förekom i högre eller lägre nivåer i adriamycin‑resistenta celler jämfört med normala HL60‑celler. Många av dessa proteiner grupperade i banor som styr hur celler använder energi och svarar på stress. Särskilt proteiner i cAMP‑signalvägen, HIF‑1‑vägen (som hjälper celler hantera lågt syre) och oxidativ fosforylering (en huvudprocess för energiproduktion i mitokondrierna) var förändrade. Dessa skiften tyder på att resistenta leukemiceller omprogrammerar hur de andas, växer och kommunicerar för att motstå kemoterapi.
Metabolismen förskjuts mot aminosyror
Metabolomikanalysen berättade en kompletterande historia. Av omkring 1 400 detekterade metaboliter förändrades 260 signifikant i de resistenta cellerna. Statistiska modeller separerade klart resistenta från icke‑resistenta celler, vilket indikerar en konsekvent metabolisk signatur för resistens. När de förändrade metaboliterna kartlades mot kända biokemiska vägar framträdde flera banor. Många av de mest påverkade vägarna var kopplade till aminosyror, proteiners byggstenar — särskilt de som involverar alanin, aspartat, glutamat, cystein, metionin och glutation. Andra nätverk, såsom purin‑ och pyrimidinmetabolism (viktigt för DNA och RNA) och hantering av vissa lipider, var också störda, vilket understryker att resistens är kopplad till omfattande metabol ombyggnad.
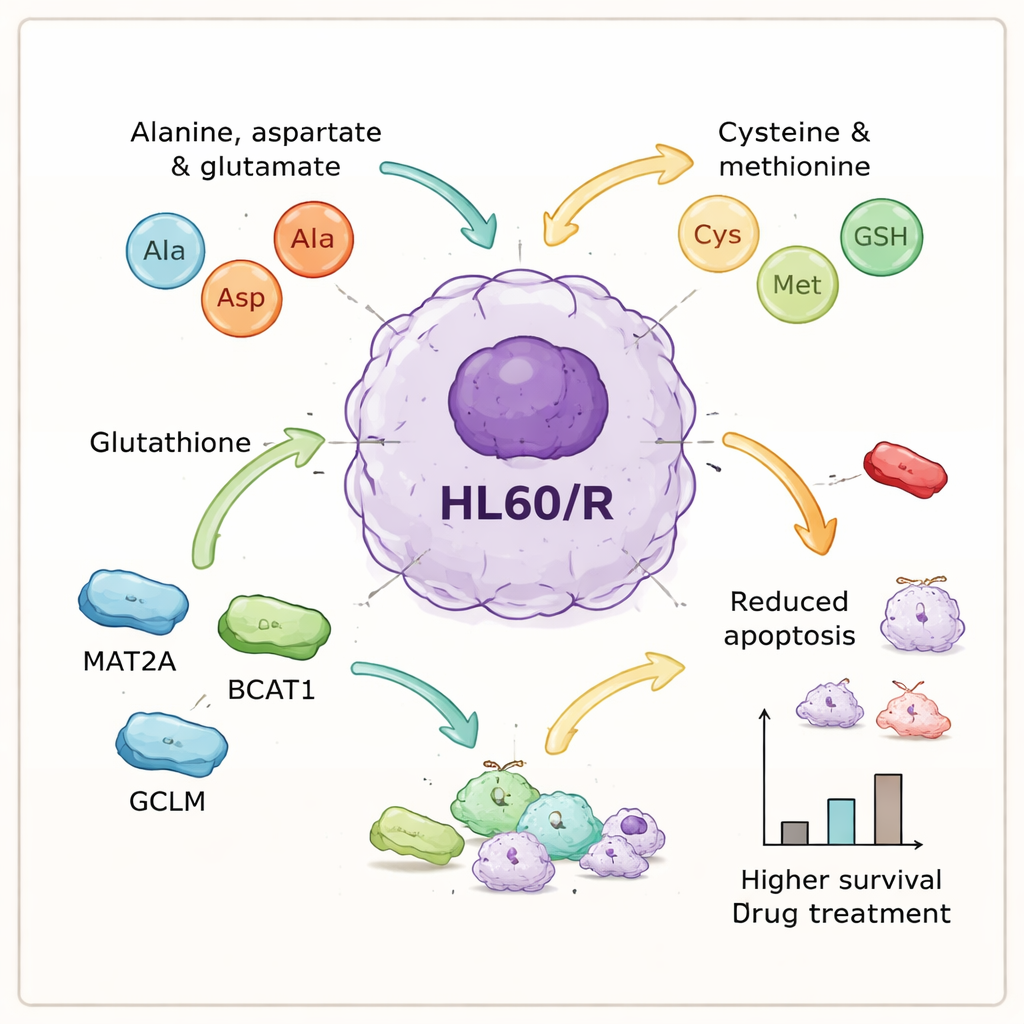
Nyckelspelare som hjälper cancerceller att uthärda
Genom att integrera protein‑ och metabolitdata fokuserade författarna på en uppsättning aminosyra‑relaterade processer som verkade centrala för resistensen. De valde sex proteiner knutna till dessa vägar — GOT1, GPX1, AHCY, MAT2A, BCAT1 och GCLM — för närmare granskning. Laboratorietester bekräftade att fem av dem var mer rikligt förekommande i resistenta celler, i linje med idén att aminosyrahanteringen är uppreglerad, medan ett antioxidantenzym, GPX1, var minskat. För att undersöka orsak och verkan använde teamet små interfererande RNA för att nedreglera tre av de uppreglerade proteinerna — MAT2A, BCAT1 och GCLM — i de resistenta cellerna. När dessa proteiner slogs ner genomgick cellerna betydligt mer programmerad celldöd efter behandling, vilket innebar att de förlorade mycket av sitt hårt förvärvade skydd mot adriamycin.
Vad detta betyder för framtida behandlingar
Tillsammans tyder dessa fynd på att adriamycin‑resistenta AML‑celler överlever inte bara på grund av enstaka mutationer, utan för att de omformar sin interna kemi, med aminosyrametabolismen som en central knutpunkt. Genom att rikta mer resurser till särskilda aminosyra‑ och glutationvägar verkar cellerna bättre kunna hantera stress, reparera skador och undvika död vid exponering för kemoterapi. För icke‑specialister är huvudbudskapet att resistens inte är slumpmässig: den följer identifierbara mönster som kan mätas och potentiellt riktas. På sikt skulle läkemedel som stör specifika aminosyra‑hanterande proteiner som MAT2A, BCAT1 eller GCLM kunna kombineras med adriamycin eller liknande medel och ge kliniker nya verktyg för att förebygga eller övervinna resistens hos patienter med akut myeloisk leukemi.
Citering: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Nyckelord: akut myeloisk leukemi, läkemedelsresistens, adriamycin, aminosyrametabolism, multi‑omik