Clear Sky Science · sv
En funktionell och robust cellmodell för storskalig screening av Piezo1-modulatorer
Varför de små trycksensorerna i våra celler spelar roll
Varje gång blod sköljer genom våra kärl, eller när vi bara går över ett rum, känner våra celler små mekaniska krafter. Ett nyckelprotein som fungerar som "trycksensor" kallat Piezo1 hjälper celler att omvandla dessa krafter till elektriska och kemiska signaler som håller vävnaderna friska. Eftersom Piezo1 är inblandad i blodkärlsbildning, benstyrka, immunfunktion och sällsynta ärftliga sjukdomar, vill läkemedelsutvecklare hitta molekyler som kan justera dess aktivitet. Artikeln som beskrivs här presenterar ett nytt, snabbare sätt att söka efter sådana molekyler med konstruerade celler och ljusbaserade avläsningar i stället för långsamma, arbetsintensiva tekniker.
Att omvandla beröring till en ljussignal
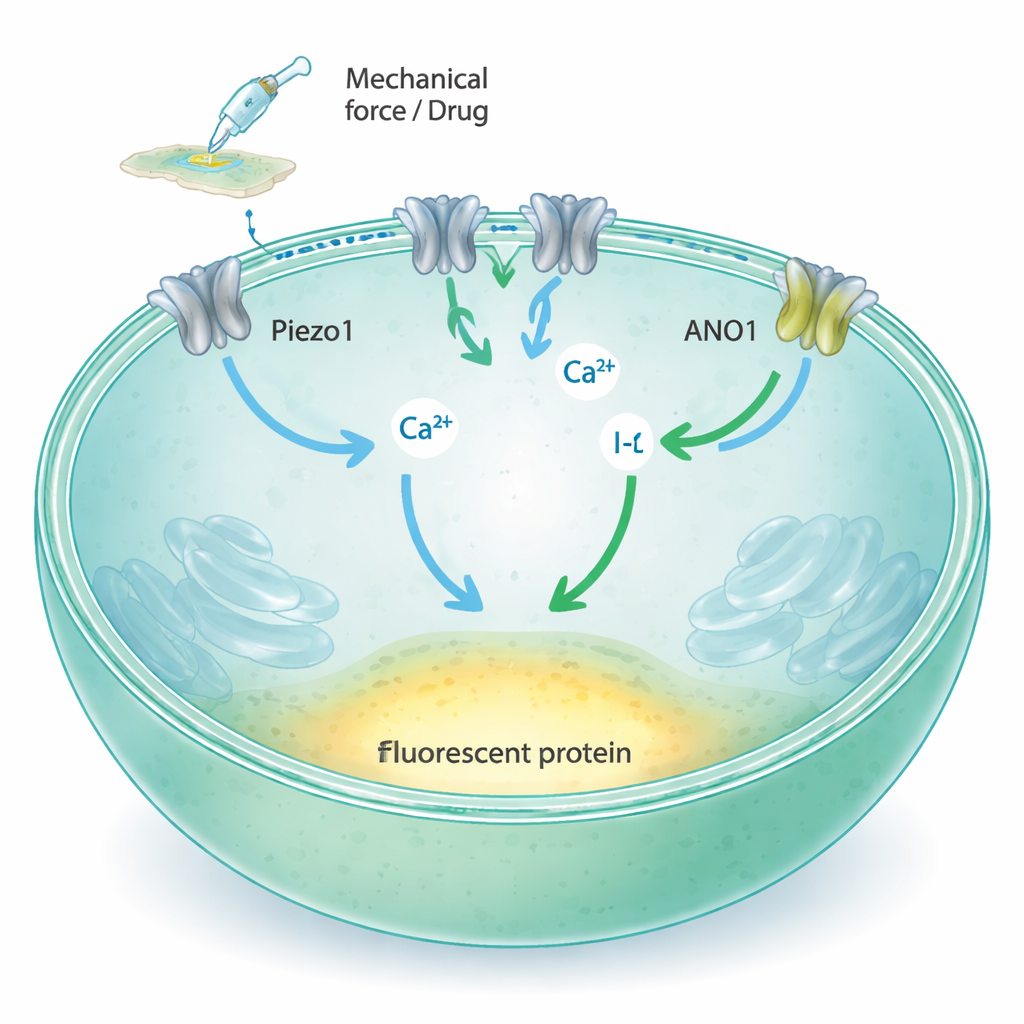
Piezo1 är en kanal i cellmembranet som öppnas när membranet sträcks eller trycks, vilket tillåter kalcium och andra laddade joner att flöda in i cellen. Traditionella metoder för att studera sådana kanaler förlitar sig på fina glaselektroder eller specialiserade fluorescerande rapportörer, vilka är kraftfulla men svåra att skala upp till de tiotusentals tester som moderna läkemedelsupptäckter kräver. Författarna ville därför omvandla Piezo1-aktivitet till en enkel ljusförändring som en platteläsare snabbt kan mäta över många prover samtidigt. Deras idé var att koppla Piezo1 till två ytterligare komponenter: ANO1, en annan jonkanal som svarar på kalcium, och ett modifierat gult fluorescerande protein som tappar ljusstyrka när det utsätts för jodidjoner.
Att bygga en responsiv testcell
Forskarna började med Fischer Rat Thyroid (FRT)-celler, som naturligt uttrycker Piezo1 och fäster väl på standardplastplattor. De bekräftade att dessa celler uttrycker Piezo1 men inte dess nära släkting Piezo2, och visade att Piezo1 i dessa celler svarar på vätskeflöde och mekanisk stimulans genom att släppa in kalcium. Nästa steg var att införa ANO1-kanalen och det jodidkänsliga fluorescerande proteinet (YFP-H148Q/I152L) i cellerna. När kalciumnivån stiger inuti cellen öppnas ANO1 och tillåter jodid att komma in; det fluorescerande proteinet blir då svagare när jodid bygger upp runt det. Mikroskopi, flödescytometri och elektriska inspelningar visade att både ANO1 och den fluorescerande sensorn fanns i höga nivåer och fungerade som avsett.
Från läkemedelsverkan till ett mätbart sken
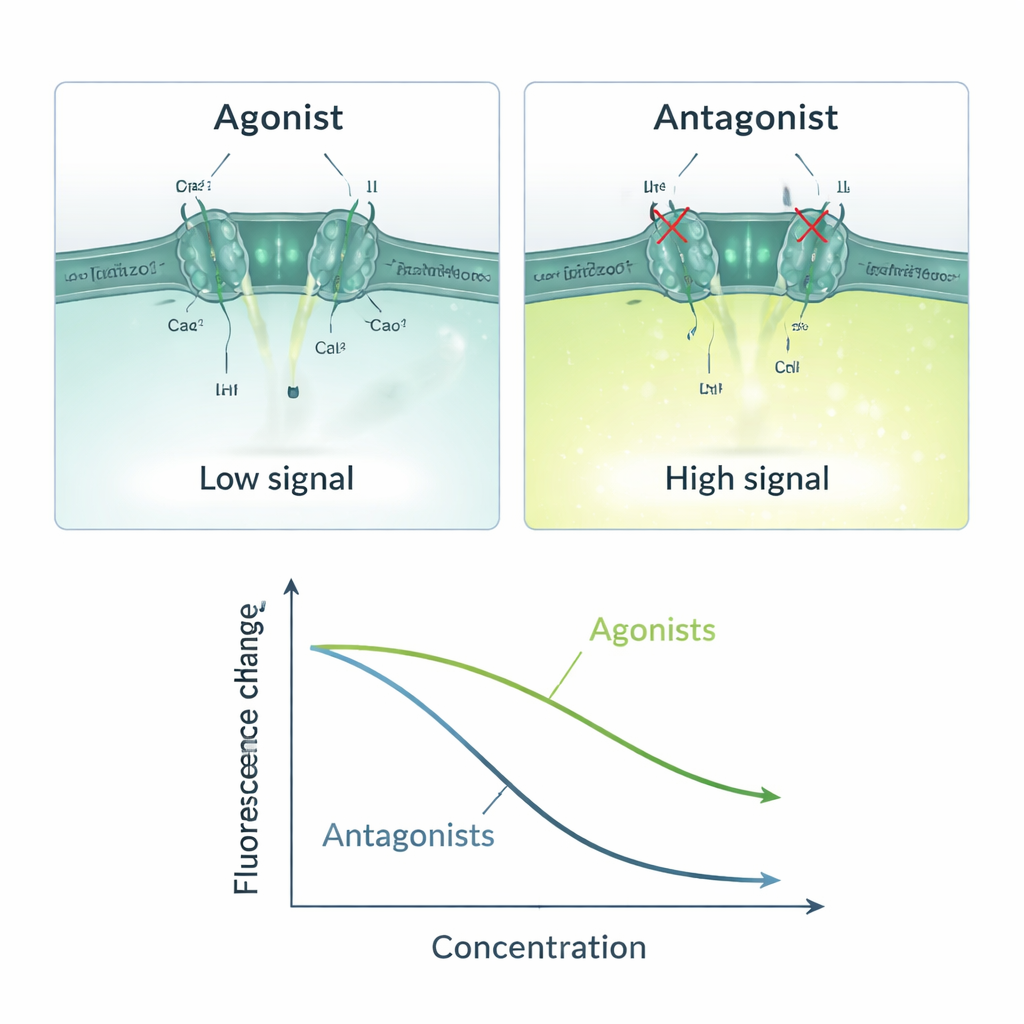
Med detta tredelade system på plats skapade teamet en enkel orsak‑och‑verkan-kedja: om en testmolekyl aktiverar Piezo1 strömmar kalcium in, ANO1 öppnas, jodid släpps in och fluorescensen sjunker; om en molekyl blockerar Piezo1 förblir signalen ljus. De validerade denna logik med välkända Piezo1-aktivatorer (Yoda1, Jedi1, Jedi2) och blockerare (Ruthenium Red, GsMTx4). Aktivatorer gav dosberoende minskningar i fluorescens, med känslighetsvärden som matchade tidigare rapporterade data. Blockerare gav motsatt mönster och minskade responsen i takt med att deras koncentration ökade. Assayet fungerade endast när både kalcium och jodid var närvarande, vilket betonar att signalen verkligen berodde på Piezo1-driven kalciuminströmning och efterföljande ANO1-medierad jodidinflöde. Statistiska mått som Z-faktor och signal‑till‑brus‑förhållande indikerade att metoden är stabil och tillförlitlig nog för industriell storskalig screening.
Snabb, skalbar testning med vissa förbehåll
Den nya cellmodellen kan genomföra en mätning per brunn på cirka 14 sekunder och skanna en hel 96‑brunnsplatta på ungefär 22 minuter, och den kan anpassas till instrument som läser hundratals brunnar samtidigt. De konstruerade cellerna förblir stabila över många generationer under antibiotikaselektion, vilket möjliggör upprepade experiment över tid. Eftersom avläsningen är optisk och använder standardmikroplattutrustning är tillvägagångssättet relativt kostnadseffektivt och tillgängligt. Författarna noterar dock att deras test är indirekt: vilken förening som helst som påverkar steg före eller efter Piezo1 i signalvägen — till exempel ANO1 självt eller andra kalciumhanterande proteiner — kan ge falskt positiva resultat. Av den anledningen måste träffar från denna screening fortfarande bekräftas med mer direkta metoder som elektrofysiologi.
Vad detta betyder för framtida behandlingar
I vardagliga termer har forskarna byggt ett laboratoriums "brandvarnare" som blinkar svagare när en förening puffar på Piezo1 och förblir stark när Piezo1 är blockerat. Denna varnare är känslig, snabb och enkel att köra i stora mängder, vilket gör den väl lämpad för första gallringen i sökandet efter läkemedel som finjusterar kroppens mekaniska sensorer. Även om den inte kommer att ersätta mer detaljerade uppföljningstester, ger denna cellmodell en kraftfull utgångspunkt för att upptäcka molekyler som en dag kan hjälpa till att behandla kärlsjukdomar, bensjukdomar, immunproblem och andra tillstånd kopplade till hur våra celler känner och reagerar på fysisk kraft.
Citering: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Nyckelord: Piezo1-kanal, mekanosensoriska jonkanaler, höggenomströmmande screening, cellbaserat assay, Läkemedelsupptäckt