Clear Sky Science · sv
Syntes, karakterisering, DFT-analys, molekylär dokning och antitumörutredningar vid kolorektalt karcinom av en ny pyrazol-hydrazon zink(II)-komplex
Varför ett metallbaserat läkemedel kan bekämpa tjocktarmscancer mer skonsamt
Många kraftfulla cancerläkemedel bygger på tunga metaller som platina. De kan vara effektiva men åtföljs ofta av kraftiga biverkningar och resistens över tid. Denna studie undersöker en annan väg: en ny läkemedelskandidat byggd kring zink, ett essentiellt näringsämne som redan finns i vår kropp, i kombination med en organisk stomme kallad pyrazol–hydrazon. Forskarna frågade om man genom att koppla zink till denna stomme kan skapa en förening som slår hårt mot tjocktarmscancerceller samtidigt som friska celler skonas.
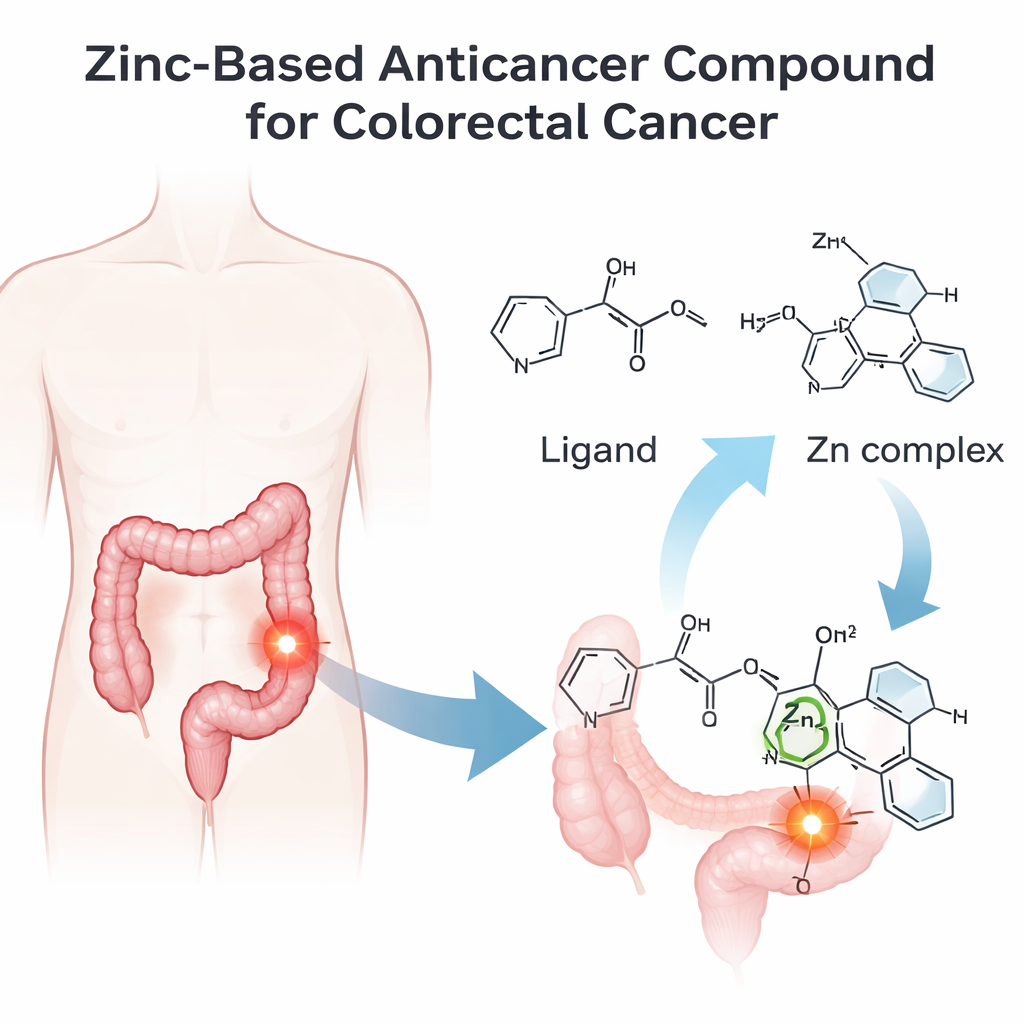
Att bygga en smartare zinkbaserad molekyl
Teamet designade och syntetiserade först en ny organisk molekyl, benämnd IMP, och bundet den sedan till en zinkjon för att bilda ett zinkkomplex kallat IMP-Zn. De bekräftade den exakta strukturen för båda med en rad tekniker som i praktiken ”fingeravtryckar” molekyler: infraröd spektroskopi för att se vilka kemiska bindningar som finns, kärnmagnetisk resonans för att kartlägga atompositioner, massespektrometri för att verifiera molekylvikten, och ultraviolett–synlig spektroskopi för att studera hur föreningarna interagerar med ljus. Dessa experiment, tillsammans med elektriska ledningsförsök, visade att zink är tätt koordinerat till tre nyckelatomer i IMP och två kloridjoner, vilket bildar ett väldefinierat komplex centrerat kring zink.
Att skåda in i molekylen med virtuell kemi
För att komplettera laboratoriemätningarna körde forskarna detaljerade datorsimuleringar med densitetsfunktionalteori (DFT). Dessa beräkningar gjorde det möjligt att förutsäga hur elektroner är fördelade inom IMP och IMP-Zn, hur stabil varje form är, och hur lätt molekylerna kan delta i kemiska reaktioner. Resultaten visade att när zink är bundet krymper energigapet mellan molekylens ”frontier”-orbitaler, vilket innebär att elektroner kan röra sig lättare inom strukturen. Detta brukar översättas till högre kemisk reaktivitet. Zinkkomplexet visade också ett högre så kallat elektrofilicitetsindex, vilket tyder på att det är bättre rustat att interagera med biologiska mål än den fria liganden IMP ensam.
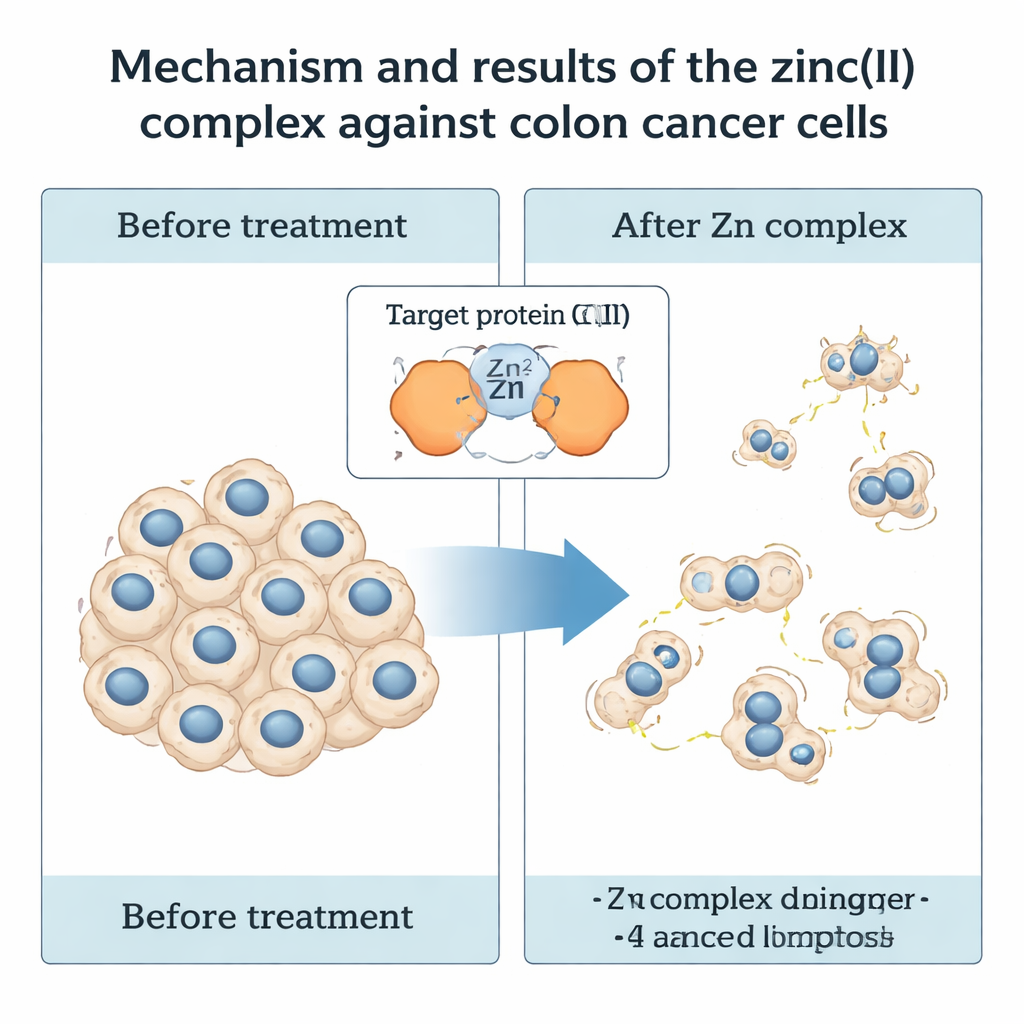
Hur zinkkomplexet angriper tjocktarmscancerceller
Det verkliga testet var biologiskt. Forskarna behandlade humana kolorektala cancerceller (HCT116) med IMP och IMP-Zn vid olika doser och tidpunkter och mätte hur många celler som överlevde. Båda föreningarna bromsade cancercellstillväxt, men zinkkomplexet var tydligt starkare: efter 48 timmar halverade IMP-Zn cellviabiliteten vid omkring 25 mikromolar, medan liganden ensam krävde en mycket högre dos. Lika viktigt var att samma koncentrationer av IMP-Zn inte visade någon påtaglig toxisk effekt på en normal human njurcellinje (HEK293), vilket pekar på en viss selektivitet för cancerceller. När teamet följde behandlade cancerceller över två veckor fann de att IMP-Zn kraftigt minskade både antalet och storleken på kolonier cellerna kunde bilda, vilket indikerar att det stör deras förmåga att proliferera långsiktigt.
Indikationer på att cellerna drivs mot programmerad celldöd
För att förstå hur zinkkomplexet skadar cancerceller undersökte forskarna cellcykeln — de stadier celler passerar när de växer och delar sig. Efter exponering för IMP-Zn flyttade en betydligt större andel av HCT116-cellerna in i en "SubG0"-fas, ett kännetecken för celler med fragmenterat DNA. Detta mönster är ofta förknippat med apoptos, en kontrollerad form av celldöd som ofta är måltavla för antitumörläkemedel. Molekylär dokningsimuleringar gav ytterligare en pusselbit: virtuella modeller föreslog att IMP-Zn binder starkare än IMP till flera cancerrelaterade proteiner, inklusive en tillväxtfaktorreceptorkinas, en cellcykelreglerande kinas och ett läkemedelsmetaboliserande enzym. Dessa tätare interaktioner stöder idén att zinkkoordination hjälper föreningen att fästa vid kritiska cellulära maskinerier och störa cancercellernas överlevnad.
Vad detta kan innebära för framtida behandlingar
Sammantaget visar studien att att ”dekorera” en pyrazol–hydrazonstomme med zink gör mer än att bara finjustera dess kemi: det förvandlar IMP till ett mer reaktivt, mer potent och till synes mer selektivt medel mot kolorektala cancerceller. Trots att IMP-Zn fortfarande är långt från ett färdigt läkemedel — det återstår att testa i djur eller människor — markerar dess förmåga att avsevärt bromsa tjocktarmscancertillväxt, driva celler mot apoptos och skona normala celler det som en lovande medlem i en växande klass av zinkbaserade metallläkemedel. Detta arbete antyder att noggrant designade zinkkomplex skulle kunna erbjuda skonsammare, riktade alternativ eller komplement till traditionell metallbaserad cytostatika i framtiden.
Citering: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Nyckelord: zinkbaserade antitumörmedel, kolorektalcancer, pyrazol-hydrazonkomplex, molekylär dokning, apoptos