Clear Sky Science · sv
Klorinerade bis-4-hydroxykumariner hämmar flavivirusreplikation genom att inhibera denguevirus typ 2:s proteinsyntes och replikation
Nya förhoppningar mot myggburna virus
Dengue- och Zikavirus smittar hundratals miljoner människor varje år, ofta i områden med begränsade medicinska resurser. Vacciner ger bara partiellt skydd och det finns fortfarande inget allmänt använt antiviralt läkemedel som läkare kan ordinera i ett tidigt sjukdomsskede. Denna studie undersöker en familj labbskapade kemikalier härledda från växtmolekyler och ställer en enkel men brådskande fråga: kan någon av dem pålitligt bromsa dessa virus i humana celler utan att skada cellerna själva?
Växtinspirerade molekyler som virusblockerare
Forskarlaget riktade in sig på kumariner, en klass naturliga föreningar som finns i många växter och länge varit kända för sina mikrobiella och antivirala egenskaper. De testade tolv “biskumarin”-derivat — två kumarin-enheter kopplade till varandra — mot denguevirus typ 2 och Zikavirus i cellkulturer. Genom att mäta hur många infektiva partikeler som producerades och hur friska cellerna förblev, upptäckte de att två klorerade varianter, benämnda förening 3 och förening 4, var särskilt lovande. Vid låga mikromolära koncentrationer minskade dessa klorerade bis-4-hydroxykumariner virusproduktionen med mer än 90 % samtidigt som de flesta celler förblev vid liv och fungerade.
Finjustera kemin för starkare skydd
Inte alla kemiska justeringar fungerade lika bra. Genom att systematiskt förändra atomer runt en ringsystemdel av molekylerna fann teamet att tillsats av klor i specifika positioner gav bäst antiviral aktivitet. Att byta ut klor mot andra halogener som fluor eller brom — eller att lägga till andra kemiska grupper — försvagade oftast effekten mot dengue och Zika. Med hjälp av datorbaserade modeller kopplade de antiviral styrka till enkla molekylära egenskaper, såsom hur laddning fördelas över molekylen och hur mycket yta den exponerar. Maskininlärningsmetoder fångade dessa samband betydligt bättre än äldre statistiska verktyg, vilket tyder på att artificiell intelligens kan hjälpa till att styra designen av förbättrade kandidatläkemedel mot dengue.
Hur föreningarna stör virusets livscykel
När de väl tagit sig in i en cell använder denguevirus sitt RNA-genom som mall för att tillverka ett långt polyprotein som klipps till fungerande delar, och sedan kopierar sitt RNA för att skapa nya virus. Studien visar att föreningarna 3 och 4 främst stör dessa translations- och replikationssteg. I infekterade celler sjönk nivåerna av ett centralt viruskapselprotein dramatiskt när föreningarna var närvarande, och ett rapportsystem som följer viral RNA-replikation dämpades också i en dosberoende takt. Biokemiska tester och dator-dockning pekade på ett viralt enzym, kallat NS5 metyltransferas, som ett direkt men relativt svagt mål: föreningarna kunde hämma dess RNA‑”capping”-funktion, om än inte alls lika kraftigt som en välkänd referenshämmare. De saktade även måttligt ner virusets proteas, ett annat enzym som behövs för att klyva det virala polyproteinet.
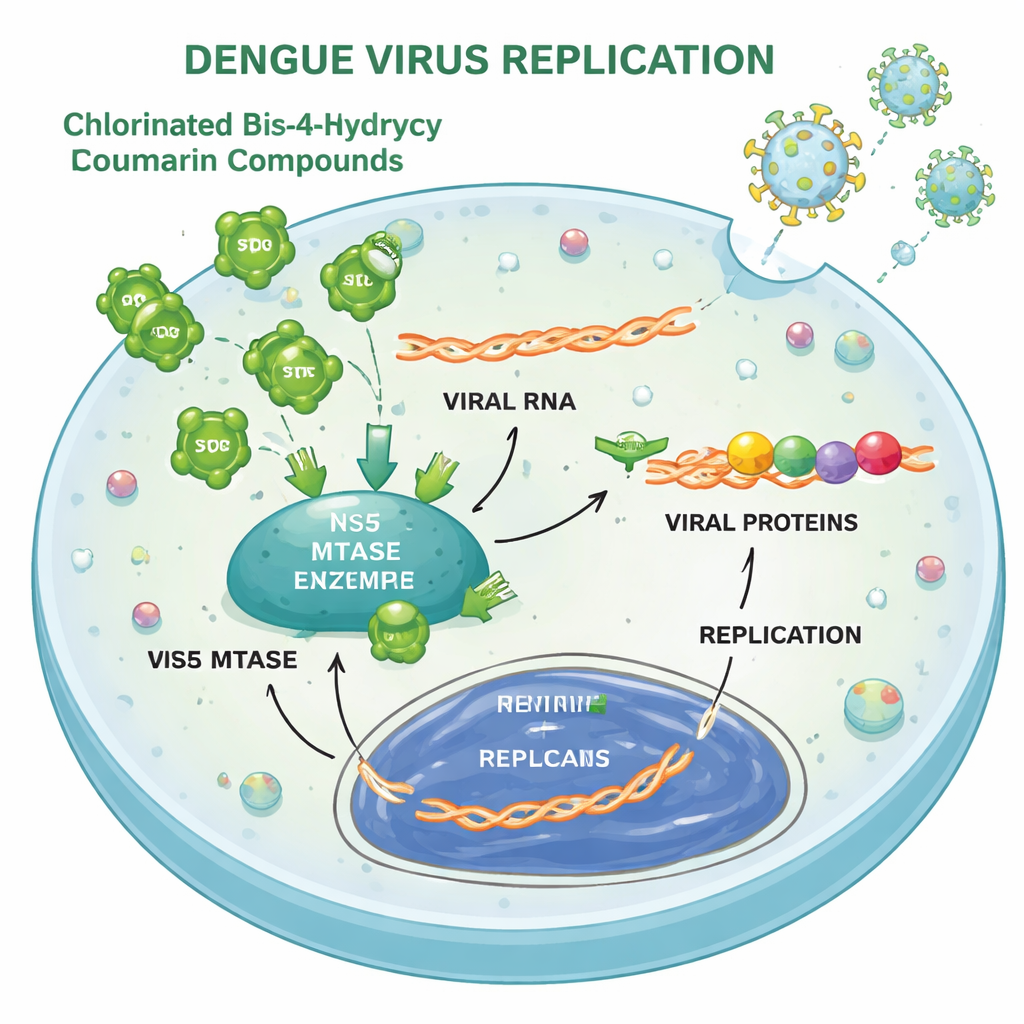
Virusen har svårt att anpassa sig till attacken
Virus undkommer ofta läkemedel genom mutationer. För att se om detta kunde inträffa här odlade teamet denguevirus upprepade gånger i celler badade i de nya föreningarna över många infektionscykler. Flera förändringar uppstod i ett annat virusprotein, NS4B, som hjälper till att böja cellmembran till små fickor där replikation sker. Överraskande nog var dessa muterade virus inte mindre känsliga för föreningarna än den ursprungliga stammen. Datorprediktioner av strukturer antydde att NS4B:s övergripande form förblev i stort sett oförändrad. Detta mönster tyder på att mutationerna var generella anpassningar till stress snarare än verklig resistens. Det stöder också idén att föreningarna verkar på flera delar av replikationsmaskineriet eller på värdcellfaktorer som viruset inte lätt kan ändra.
Varför dessa fynd är viktiga för framtida behandlingar
För icke‑specialister är huvudbudskapet att forskarna har identifierat ett nytt kemiskt ”stomme” som kan bromsa dengue- och Zikavirus vid flera punkter i deras livscykel, särskilt när virusen försöker översätta sina gener och kopiera sitt RNA inne i celler. Den mest lovande molekylen, förening 3, verkar vid låga doser, skadar celler relativt lite, träffar alla fyra huvudtyperna av dengue liksom Zika, och driver inte snabbt fram viral resistens i laboratoriet. Även om dessa klorerade bis-4-hydroxykumariner fortfarande är långt ifrån läkemedel, ger de en stark utgångspunkt för kemister och virologer att förfina, testa i djurmodeller och så småningom kombinera med andra läkemedel — steg som kan föra oss närmare en efterlängtad antiviral tablett mot myggburna infektioner.
Citering: Loeanurit, N., Phan, THT., Hengphasatporn, K. et al. Chlorinated bis-4-hydroxycoumarins suppress flavivirus replication by inhibiting dengue virus type 2 translation and replication. Sci Rep 16, 5300 (2026). https://doi.org/10.1038/s41598-026-35654-8
Nyckelord: denguevirus, Zikavirus, antivirala föreningar, kumarin-derivat, virusreplikation