Clear Sky Science · sv
Kemosensoriskt svar på Pt-baserade cytostatika via bittra smakreceptorer in vitro avslöjar en ny mekanism för smakstörningar
Varför cancerläkemedel plötsligt kan få allt att smaka fruktansvärt
Cancerpatienter rapporterar ofta att mat börjar smaka konstigt bittert eller metalliskt kort efter att kemoterapi inletts. Det gör mer än att förstöra måltider: det kan minska aptiten, främja viktminskning och urholka livskvaliteten just när patienterna behöver kraft som mest. Denna studie ställer en förenklat formulerad men praktiskt viktig fråga: hur stör vanliga platina-baserade cytostatika exakt vår smakuppfattning, och kan den effekten dämpas säkert utan att försvaga behandlingen?
Den dolda rollen för ”bittrareceptorer” i mun och tarm
Våra tungor och matsmältningskanal är täckta av bittra smakreceptorer, byggda för att varna oss för potentiellt skadliga ämnen. Dessa sensorer, kända som TAS2R, finns inte bara i smaklökarna; de återfinns också i celler i magsäcken. Forskarna använde en human gastrisk cellinje (HGT-1) som fungerar som en in vitro-detektor för bitterhet: när bittra receptorer aktiveras pumpas fler protoner (syra) ut av cellerna, vilket kan mätas som en förändring i ett mått kallat intracellular proton index. Genom att utsätta dessa celler för två vida använda platina-baserade cancerläkemedel — karboplatin och cisplatin — kunde teamet säkert undersöka hur ”bittra” dessa läkemedel framstår för humana celler utan att någonsin be en person smaka på ett giftigt ämne. 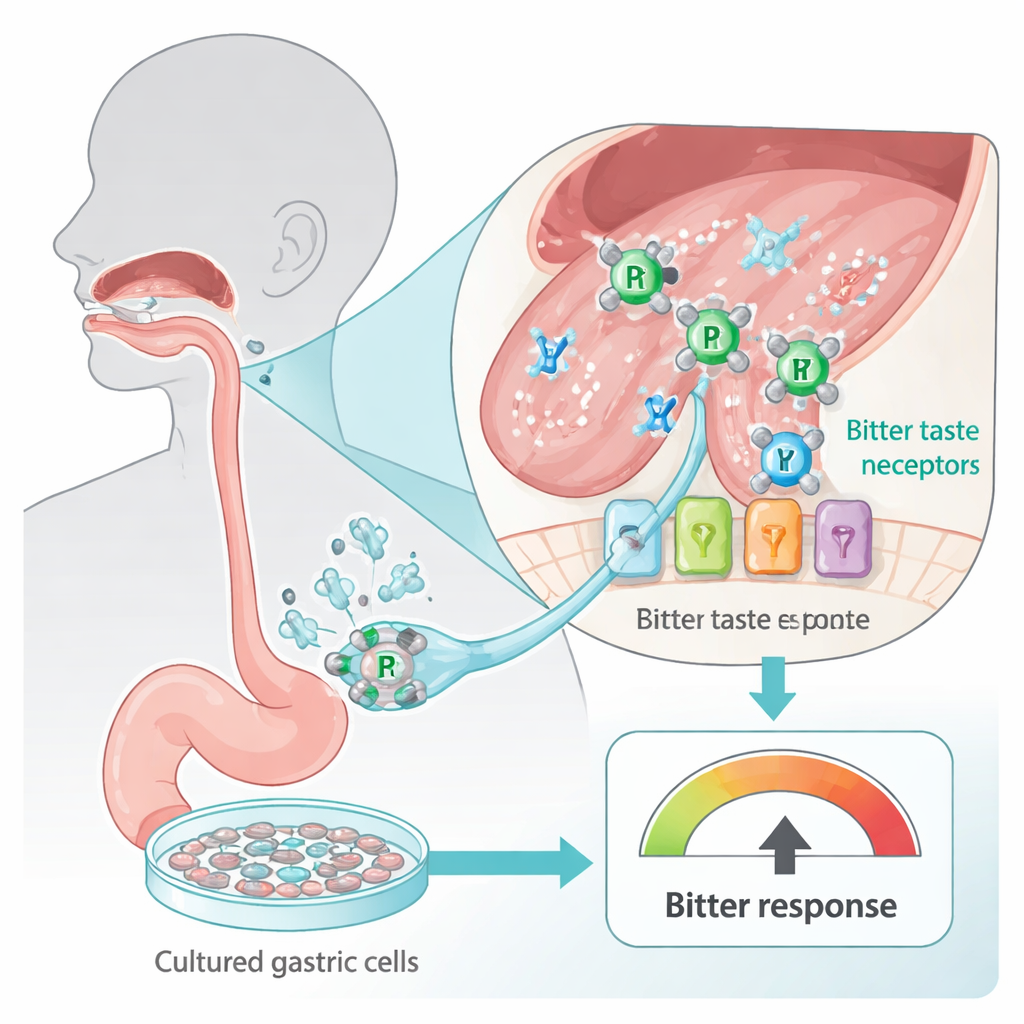
Cytostatika som smakar bittert för cellerna
När de gastriska cellerna behandlades med kliniskt relevanta koncentrationer av karboplatin och cisplatin utlöste båda läkemedlen ett tydligt, dosberoende bitterliknande svar: högre dos gav starkare cellulär reaktion. Cisplatin gav dock en mer intensiv respons än karboplatin när deras vanliga terapeutiska doskvot (ungefär 1:4) beaktades, vilket tyder på att det kan bidra starkare till bittra smakproblem hos patienter. På genetisk nivå förändrade exponering för dessa läkemedel aktiviteten hos flera gener för bittrareceptorer i cellerna, vilket visar att platina-läkemedel inte verkar på en enstaka ”bitterbrytare” utan i stället omformar bitterkänselsystemet brett. Bland dessa receptorer utmärkte sig TAS2R4 och TAS2R5 som både högt aktiva och starkt påverkade av behandlingen.
Stänga av bitsignaler och testa en naturlig bitterblockerare
För att avgöra vilka receptorer som är viktigast inaktiverade teamet selektivt specifika bittrareceptorer. Att slå ut TAS2R4 eller sänka uttrycket av TAS2R5 minskade vardera det bitterliknande svaret på karboplatin och cisplatin, vilket bekräftar att dessa receptorer bidrar till att känna av läkemedlen. Forskarna testade sedan en lovande motåtgärd: natriumsaltet av homoeriodictyol (Na-HED), en flavanon ursprungligen isolerad från den nordamerikanska växten Herba Santa, redan känd för att maskera bitterhet från andra föreningar. När Na-HED tillsattes tillsammans med platinaläkemedlen dämpade det det cellulära bittra svaret markant — med ungefär tre fjärdedelar för både karboplatin och cisplatin — utan att skada cellerna i sig. Detta visar att Na-HED kan verka direkt på bittrareceptorer för att dämpa signalen som utlöses av cytostatika.
När bitterkänning och läkemedelsupptag korsas
Utöver att förklara varför platina-kemoterapi kan smaka bittert visar studien en oväntad vändning: samma bittrareceptorer verkar också påverka hur mycket av dessa läkemedel som tas upp av celler. Med hjälp av mycket känslig massespektrometri mätte forskarna platinahalten inne i cellerna efter behandling. Celler som saknade vissa receptorer, såsom TAS2R4 eller TAS2R43, ackumulerade mer platina än normala celler, vilket tyder på att intakta receptorer hjälper till att begränsa cellulärt upptag eller retention av dessa toxiska ämnen. Na-HED förändrade inte upptaget av karboplatin, men det minskade hur mycket cisplatin som kom in i cellerna och visade direkt molekylär interaktion med cisplatin i lösning. Detta tyder på att ett bittermaskerande ämne i vissa fall också kan modulera hur starkt ett läkemedel påverkar lokala vävnader, såsom smakceller eller spottkörtlar. 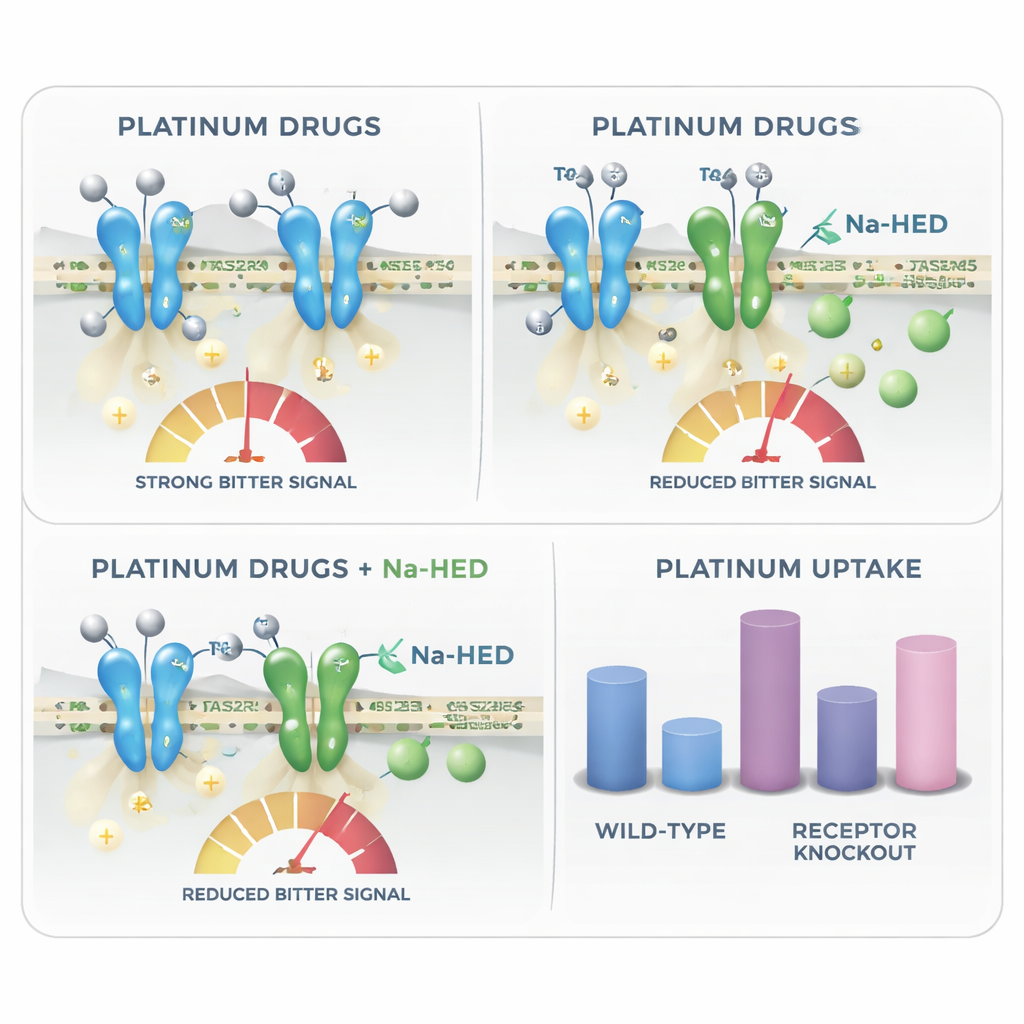
Mot mildare smakupplevelser under kemoterapi
För patienter är huvudbudskapet hoppfullt: platina-baserad kemoterapi verkar utlösa bittra smakproblem genom att direkt aktivera bittrareceptorer som finns inte bara på tungan utan också i tarmliknande celler. Cisplatin framstår som särskilt potent i detta avseende. Studin visar att Na-HED kan avsevärt dämpa denna bittra signal i ett kontrollerat cellsystem och kan också begränsa lokalt upptag av cisplatin. Även om dessa fynd behöver bekräftas hos människor pekar de mot framtida munskölj- eller spotta-ut-behandlingar innehållande Na-HED som skulle kunna mildra skarpa bittra och metalliska upplevelser utan att störa läkemedlets cancerbekämpande verkan i hela kroppen.
Citering: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Nyckelord: smakförändringar vid kemoterapi, bittra smakreceptorer, cisplatin och karboplatin, ämnen som maskerar bitterhet, näring för cancerpatienter