Clear Sky Science · sv
DFT‑beräkning av komplexbildning mellan Ac3+ och Bi3+ med hybridchelatorn 3p‑C‑DEPA för riktad alfaterapi
Varför denna forskning är viktig för cancerbehandling
Modern cancerbehandling förlitar sig i allt högre grad på radioaktiva läkemedel som kan söka upp tumörceller en och en. En kraftfull metod, kallad riktad alfaterapi, använder mycket energirika partiklar som kan döda enskilda cancerceller med anmärkningsvärd precision. Men för att leverera dessa partiklar säkert måste den radioaktiva metallen låsas i ett litet molekylärt ”bur” så att den inte vandrar till friska vävnader. Denna studie undersöker en ny burmolekyl, 3p‑C‑DEPA, utformad för att hålla särskilt svårhanterliga metaller som aktinium‑225 och bismut‑213, och ställer frågan: kan den binda dem mer säkert än dagens standardchelator, DOTA?
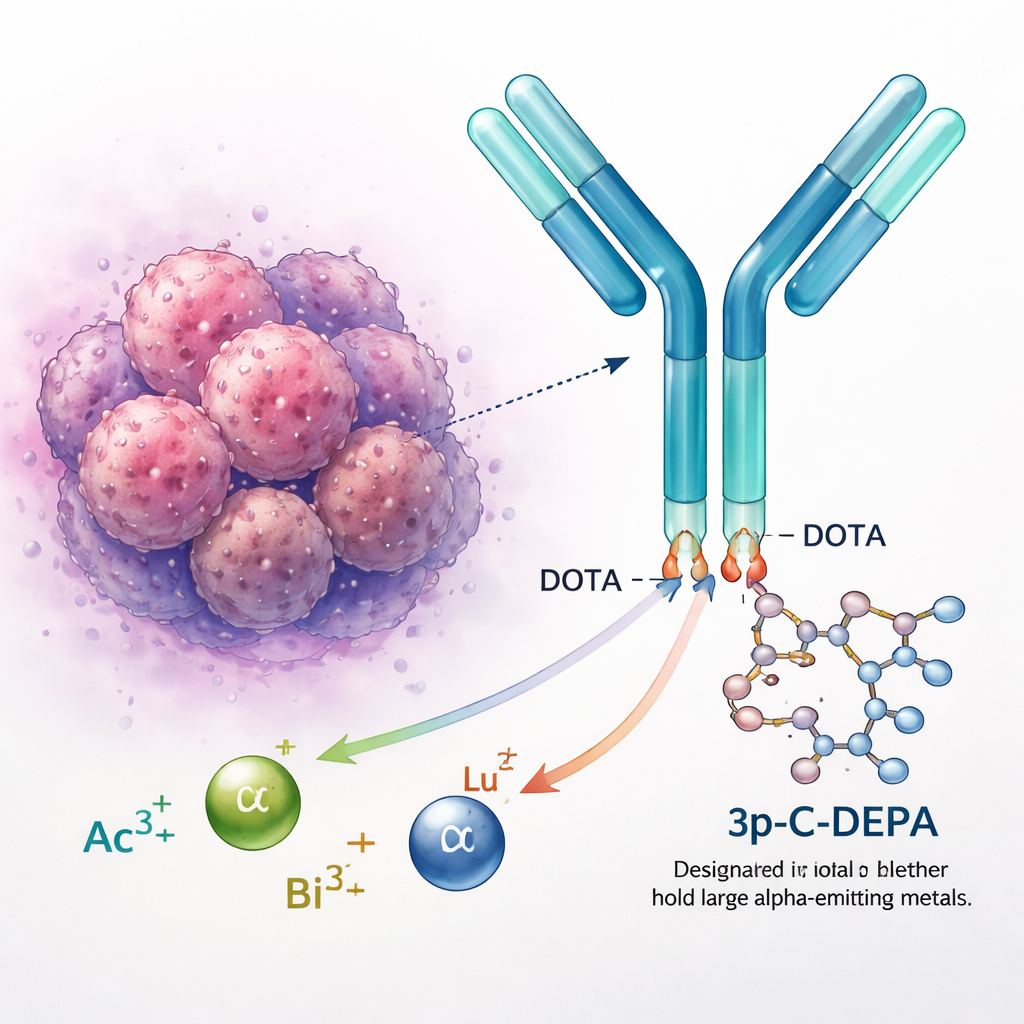
Att säkert låsa in radioaktiva metaller
Radioaktiva metaller som aktinium, bismut och lutetium används för att diagnostisera och behandla cancer. På egen hand skulle dessa positivt laddade metalljoner däremot reagera fritt i kroppen och potentiellt skada friska organ. Kemister fäster dem därför vid ”chelatorer”, ringformade molekyler som omsluter metallen och håller den på plats. DOTA, som är guldstandarden, används i flera godkända läkemedel, men den har svårt att hantera större, mer diffusa joner som aktinium‑225. Dessa metaller kan läcka ut över tid, vilket väcker oro för långsiktig säkerhet och begränsar hur brett riktad alfaterapi kan användas.
En hybridbur byggd för större atomer
Den nya chelatorn 3p‑C‑DEPA kombinerar egenskaper hos två etablerade konstruktioner: det styva, ringlika ramverket hos DOTA och den mer flexibla, öppnare strukturen hos en annan chelator, DTPA. Denna hybridarkitektur ger 3p‑C‑DEPA tio starka bindnings”händer” (kväve‑ och syreatomer) jämfört med DOTAs åtta, och ett rymligare hålrum som bättre kan rymma stora metalljoner. Tidigare laboratoriearbete antydde att 3p‑C‑DEPA kan märka antikroppar snabbt vid milda temperaturer och hålla bismutbaserade radionuklider stabilt i blodserum. Den aktuella studien tar nästa steg och använder kvantnivåberäkningar för att systematiskt jämföra hur väl 3p‑C‑DEPA och DOTA binder lutetium‑177, bismut‑213 och aktinium‑225.
En inblick i det molekylära handslaget
Då det är svårt att arbeta direkt med kortlivade alfa‑sändare vände sig forskarna till täthetsfunktionalteori (DFT), en kraftfull beräkningsmetod som uppskattar hur elektroner är fördelade i molekyler och hur starkt atomer attraherar varandra. De modellerade varje metalljon i vatten, sedan dess komplex med antingen DOTA eller 3p‑C‑DEPA, och beräknade förändringen i fri energi när metallen flyttar från vatten in i chelatorns bur. Denna energiförändring översätts till en ”stabilitetskonstant”: ju högre värde, desto hårdare håller chelatorn metallen. Två olika DFT‑metoder och två solvatationsmodeller användes för att efterlikna realistiska lösningsförhållanden och för att kontrollera att trenderna var robusta snarare än artefakter av en enskild beräkningsuppsättning.
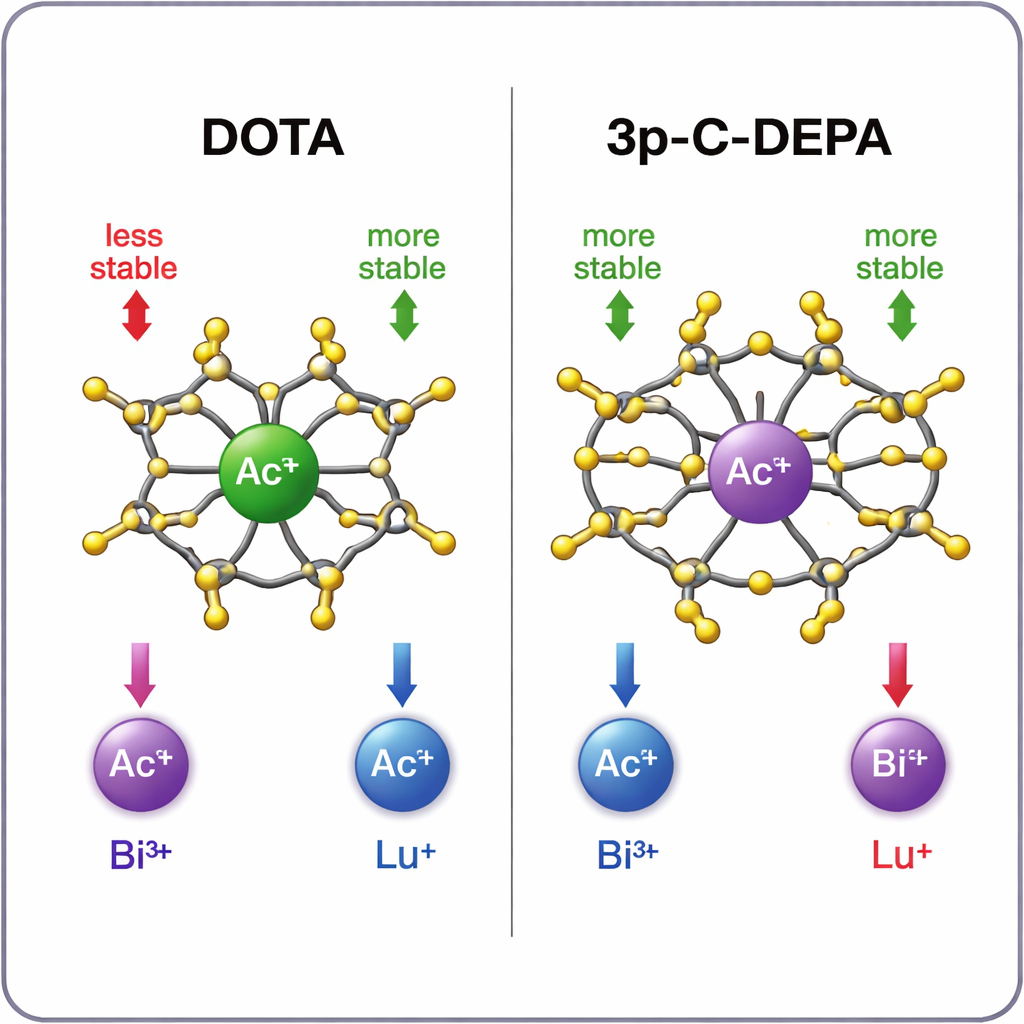
Vilken bur håller vilken metall bäst?
Simuleringarna visar ett tydligt mönster. För den stora aktiniumjonen bildar 3p‑C‑DEPA ett avsevärt mer stabilt komplex än DOTA, tack vare sitt större hålrum och fler syreredonatorer som kan greppa metallen. Även bismut‑213 rymms väl i 3p‑C‑DEPA och drar fördel av både sin storlek och sin elektrontagande karaktär, som passar med chelatorns elektrondonerande grupper. I kontrast passar den mindre lutetium‑177 bättre i DOTAs tajtare, åttaarmade omgivning. I 3p‑C‑DEPA trängs för många donatorgrupper runt den lilla jonen, vilket ger repulsiva interaktioner som verkar bromsa märkningen och något försvaga det slutliga komplexet. Beräknade stabilitetstrender överensstämmer väl med tillgängliga experimentella data och radiomärkningsutbyten, vilket stärker trovärdigheten i de teoretiska förutsägelserna.
Vad detta betyder för framtida cancerterapier
Enkelt uttryckt antyder studien att DOTA inte är en universallösning: den fungerar mycket bra för mindre metaller som lutetium, men är suboptimal för bulkigare alfautsläppare som aktinium‑225. 3p‑C‑DEPA, däremot, beter sig som en skräddarsydd hållare för dessa större joner, greppar dem hårdare och under mildare förhållanden som passar känsliga målmolekyler som antikroppar. Även om ytterligare experimentellt och kliniskt arbete krävs pekar beräkningarna på 3p‑C‑DEPA som en lovande stomme för säkrare, mer effektiva riktade alfaterapier—möjligtvis med förmåga att utöka tillgången till mycket potenta cancerbehandlingar som kan utplåna tumörer samtidigt som omkringliggande frisk vävnad skonas.
Citering: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Nyckelord: riktad alfaterapi, radioläkemedel, design av chelatorer, aktinium‑225, täthetsfunktionalteori