Clear Sky Science · sv
Strukturellt och beräkningsstött utveckling av 2,5-disubstituerade-1,3,4-oxadiazol-analoger som aktiva LOX-, ureas- och α-glukosidas-hämmare
Nya kemiska verktyg för att angripa vanliga sjukdomar
Många vardagliga hälsoproblem — från sår och njurstenar till diabetes och kronisk inflammation — drivs av överaktiva enzymer i våra kroppar. Denna studie undersöker en familj av nykonstruerade små molekyler som fungerar som små bromsar för tre sådana enzymer. Genom att finjustera deras strukturer och testa dem i laboratorium och med datorhjälp avser forskarna att lägga grunden för mer effektiva och säkrare läkemedel i framtiden. 
Varför dessa enzymer är viktiga
Teamet fokuserade på tre enzymmål som spelar mycket olika men likvärdigt viktiga roller för hälsan. Urease hjälper till att bryta ner urea; när det blir överaktivt i vissa bakterier eller vävnader kan det bidra till magsår och urinvägssår, njurstenar och till och med förhöjt blodtryck. Alpha‑glukosidas sitter på ytan av tarmceller och klyver komplexa kolhydrater till glukos; att blockera det är en väletablerad metod för att kontrollera blodsockret vid typ 2‑diabetes. Lipoxygenas (LOX) omvandlar fetter till signalmolekyler som driver inflammation, astma och vissa cancerrelaterade processer. Läkemedel som dämpar dessa enzymer utan att skada andra system är därför eftertraktade.
Bygga ett bibliotek av kandidatmolekyler
För att söka efter sådana läkemedel byggde forskarna en serie om 15 besläktade föreningar baserade på ett ringsystem kallat 1,3,4‑oxadiazol kopplat till en piperidin‑enhet. Detta kemiska stomme förekommer redan i flera moderna läkemedel och är känt för att interagera väl med biologiska mål. Teamet varierade de ”dekorationer” som fästs vid denna kärna — små grupper som metyl, etyl, metoxi, bensyl och cyklohexyl — på olika positioner och skapade ett litet bibliotek av kandidater märkta 7a till 7o. De bekräftade varje struktur med standardanalytiska metoder såsom infraröd och kärnmagnetisk resonansspektroskopi, för att säkerställa att det de syntetiserat stämde överens med designen.
Testning av hur väl molekylerna blockerar enzymer
Varje förening testades mot renade LOX, ureas och alpha‑glukosidas för att se hur effektivt den kunde bromsa enzymaktiviteten. Flera molekyler stack ut. Mot alpha‑glukosidas var föreningarna 7a och 7n särskilt effektiva och överträffade standardläkemedlet acarbose i laboratorietester genom att uppnå höga inhibitionsprocenter vid låga mikromolarkoncentrationer. För LOX visade 7a, 7h och 7n mycket stark aktivitet, i vissa fall bättre än den naturliga referenshämmaren quercetin. I ureas‑assayerna matchade eller överträffade föreningarna 7a och särskilt 7l standardhämmaren tiourea något, vilket antyder att de en dag skulle kunna fungera som ledande strukturer för anti‑sår eller anti‑sten‑terapier. 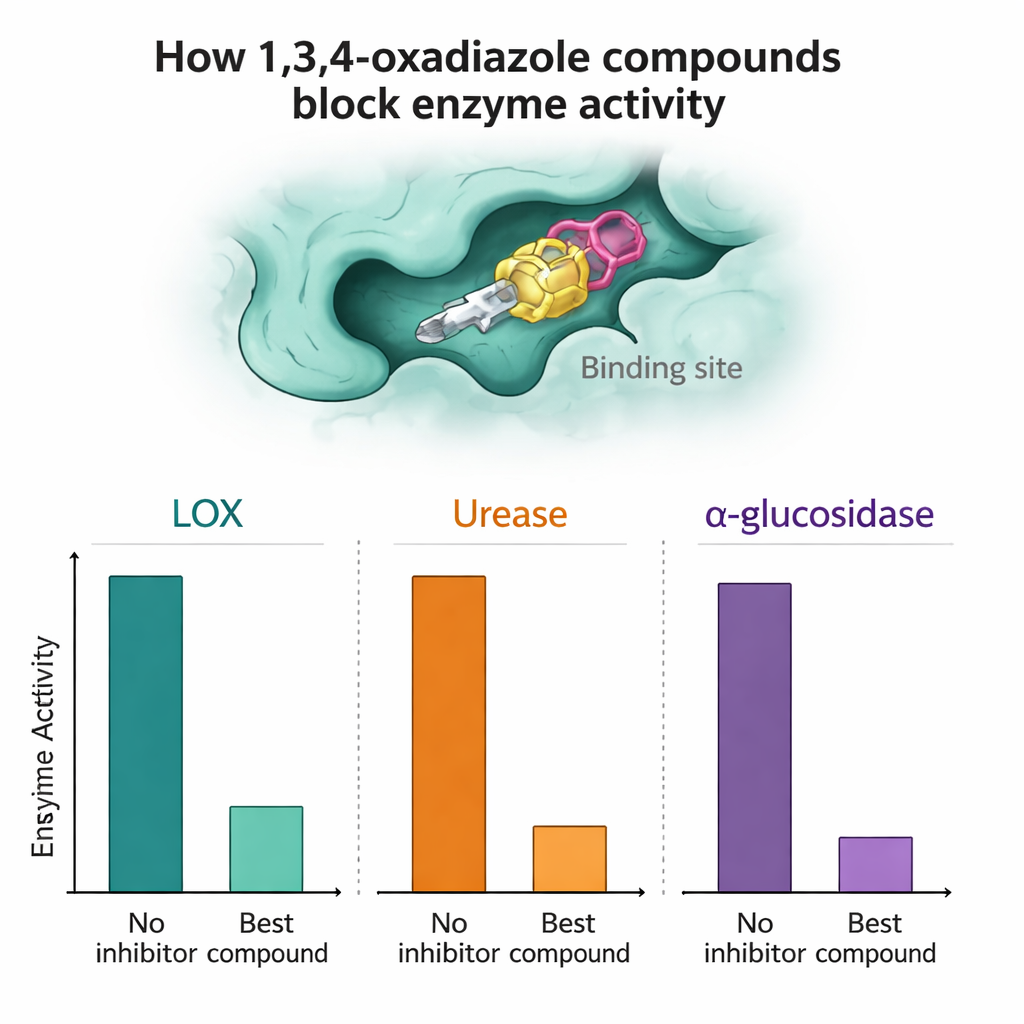
Koppla struktur till prestanda
Eftersom de enda skillnaderna mellan föreningarna 7a–7o är små förändringar kring kornringen kunde forskarna börja kartlägga enkla struktur‑aktivitetssamband. Till exempel förstärkte tillsats av små kolrika grupper på vissa ”orto”‑positioner på en bifogad ring ofta förmågan att blockera alpha‑glukosidas eller LOX. Andra substitutioner, såsom vissa metoxi‑ eller estergrupper placerade mindre gynnsamt, tenderade att försvaga aktiviteten. För att förstå varför använde teamet datorsituationer. Kvantkemiska beräkningar visade att alla molekyler var termodynamiskt stabila och tillräckligt flexibla för att anpassa sig till enzymfickor. Dockningsstudier — virtuell inpassning av varje molekyl i tredimensionella modeller av enzymerna — avslöjade att de mest aktiva föreningarna skapade tätare kontakter genom en blandning av vätebindningar och hydrofoba (oljiga) interaktioner vid nyckelställen i det aktiva sätet, medan svagare kandidater satt mindre tätt eller missade kritiska kontaktpunkter.
Vad detta betyder för framtida läkemedel
I vardagliga termer identifierar studien ett antal lovande ”nycklar” som passar väl i tre sjukdomsrelaterade ”lås” och börjar förklara, på atomnivå, varför vissa nycklar vrider bättre än andra. Ingen av dessa molekyler är ännu redo att bli ett läkemedel — de behöver fortfarande säkerhetstester, optimering för beteende i kroppen samt försök i djur och människor. Men arbetet visar att 1,3,4‑oxadiazol–piperidin‑ramverket är en fruktbar utgångspunkt för framtida behandlingar som riktar sig mot diabetes, inflammatoriska tillstånd och ureasrelaterade störningar. Kombinationen av noggranna laboratoriemätningar och detaljerad datormodellering ger en färdplan för att förfina dessa kandidater till mer precisa och effektiva läkemedel.
Citering: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Nyckelord: enzymhämmare, läkemedelsupptäckt, oxadiazol-föreningar, diabetes och inflammation, ureas och lipoxygenas