Clear Sky Science · sv
SHP2 främjar osteosarkom genom att reglera STAT3/TET3/HOXB2‑signalering
Varför denna studie om bencancer är viktig
Osteosarkom är den vanligaste primära benmaligniteten hos barn och tonåringar, och trots moderna kemoterapier och kirurgi har överlevnaden för patienter med avancerad eller recidiverande sjukdom knappt förbättrats under decennier. Denna studie undersöker den inre kopplingen i osteosarkomceller för att ta reda på vilka molekyler som fungerar som ”huvudströmbrytare” som hjälper tumörer att växa, sprida sig och motstå behandling. Genom att avslöja en nyckelregleringsväg centrerad kring ett protein kallat SHP2 pekar arbetet på nya drogmål som en dag skulle kunna göra osteosarkombehandlingar mer effektiva och mer precisa.
Följa spåren i tumörers genaktivitet
Forskarlaget började med att behandla osteosarkom som ett dataproblem. De analyserade offentliga genuttrycksdatabaser som jämför tumörprover med normalt benvävnad och använde statistiska verktyg för att identifiera gener som konsekvent var upp- eller nedreglerade i cancer. Hundratals gener skiljde sig åt, och många av dem grupperade sig i välkända cancerriktningar som driver celltillväxt, överlevnad och rörlighet. Bland dessa stack ett protein, SHP2, ut som en navpunkt starkt kopplad till flera andra: signalfaktorn STAT3, DNA‑modifierande enzymet TET3 och utvecklingsregulatorn HOXB2. Det föreslog att dessa molekyler kan bilda en sammanlänkad kedja som hjälper osteosarkomceller att uppträda aggressivt. 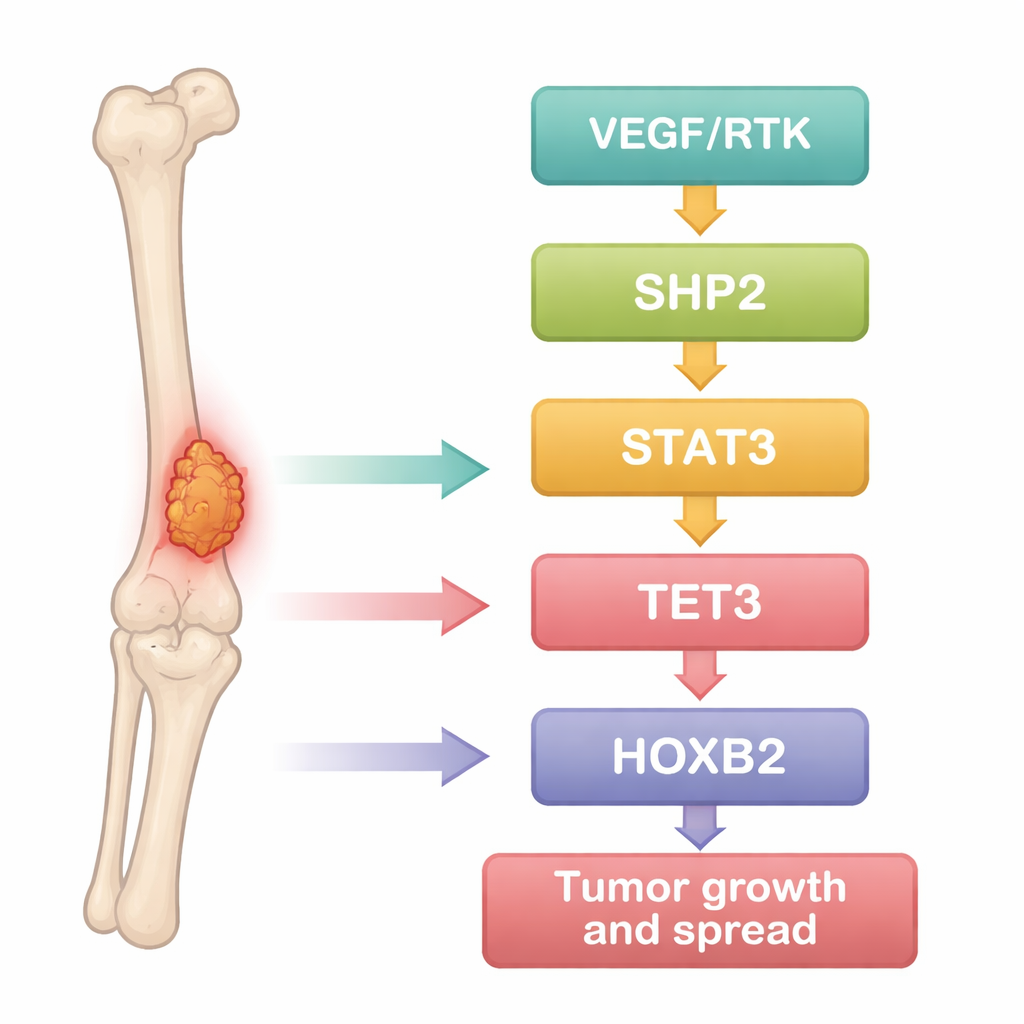
Testa SHP2:s roll i cancerceller
För att gå bortom korrelationer konstruerade teamet humana osteosarkomcellinjer (143B och MG63) för att antingen minska eller öka SHP2. När de slog ner SHP2 sjönk cellernas förmåga att föröka sig, migrera över en yta och invadera genom ett membran tydligt. Nivåerna av STAT3, TET3 och HOXB2‑proteiner, samt cancermarkörer som c‑Myc, NANOG och NUSAP1, minskade också. När de återaktiverade STAT3 eller överuttryckte HOXB2 reverserades många av dessa effekter, vilket visar att SHP2 ligger uppströms i en kedja som i slutändan påverkar gener som styr celldelning, stamcells‑lika egenskaper och cellens delningsmaskineri.
Bygga en steg‑för‑steg‑cancerväg
Genom att pussla ihop experimenten beskriver författarna en stegvis modell. I tumörmiljön stimulerar höga nivåer av vaskulär endotelial tillväxtfaktor (VEGF) receptor‑tyrosinkinaser (RTKs) på cellens yta. Dessa aktiverar i sin tur SHP2 inuti cellen. Aktivt SHP2 sätter igång STAT3, en transkriptionsfaktor som går in i kärnan och bidrar till ökad produktion av TET3. TET3 redigerar sedan kemiska taggar på DNA, specifikt genom att ta bort metylgrupper i HOXB2‑genens område. Denna demetylering fungerar som att släppa en broms och tillåter en starkare uttryckning av HOXB2. HOXB2, en gen som normalt styr utveckling, stärker nu aktiviteten hos c‑Myc, NANOG och NUSAP1, som tillsammans driver ihållande tumörtillväxt, ökar invasivt beteende och stödjer egenskaper kopplade till metastasering.
Från petriskål till levande djur
För att se om denna väg spelade roll i hela tumörer implanterade forskarna modifierade osteosarkomceller under huden på möss. Tumörer som bildades av celler som överproducerade SHP2 blev större och tyngre än kontrolltumörer. När TET3 tystades i dessa SHP2‑rika celler stannade tumörtillväxten av och nivåerna av HOXB2 sjönk, även om SHP2 och STAT3 förblev aktiva. Återinförande av HOXB2 återställde tumörens kraft. Mätningar av proteinnivåer i tumörvävnad speglade genomgående fynden från cellkulturerna, vilket stärker idén att SHP2, STAT3, TET3 och HOXB2 fungerar som en ihopkopplad axel som driver osteosarkom mot ett mer malignit beteende. 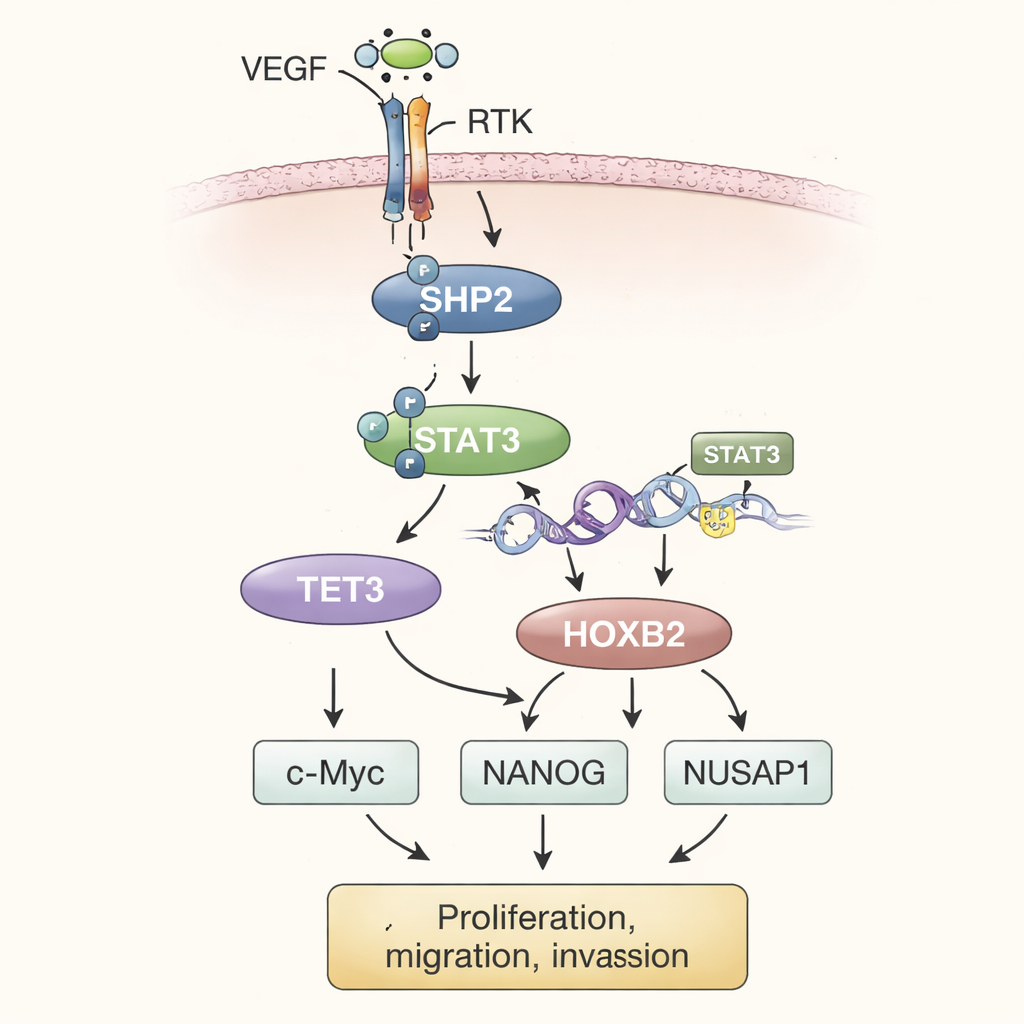
Vad detta betyder för framtida behandlingar
För en allmän läsare är huvudbudskapet att forskarna har kartlagt en tydlig signalväg — från VEGF och dess ytreceptorer, via SHP2 och STAT3, ned till TET3, HOXB2 och flera potenta tillväxtgener — som hjälper till att förklara varför osteosarkom kan växa snabbt och sprida sig tidigt. Eftersom SHP2 och STAT3 är enzymer som i princip kan blockeras med småmolekylära läkemedel, och TET3 och HOXB2 representerar senare steg i samma bana, erbjuder denna väg flera punkter där framtida terapier kan ingripa. Även om studien gjordes i cellinjer och möss ger den en detaljerad karta som läkemedelsutvecklare kan använda för att utforma kombinationsbehandlingar som syftar till att stänga av tumörens centrala styrspakar snarare än att endast angripa dess slutresultat.
Citering: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Nyckelord: osteosarkom, SHP2, STAT3‑väg, tumörsignalering, målinriktad terapi