Clear Sky Science · sv
Immunoinformatikbaserad design och utvärdering av ett multi-epitopvaccin mot Vibrio fluvialis
Varför ett nytt vaccin spelar roll för skaldjursälskare
Vibrio fluvialis är en mindre känd släkting till kolerabakterier som lever i varma kustvatten och kan förorena skaldjur och dricksvatten. Den orsakar svår diarré och tarminfektioner och blir vanligare i takt med att haven värms upp och antibiotikas effektivitet minskar. Det finns idag inget vaccin för människor. I denna studie används avancerade datorbaserade metoder för att ta fram ett nytt slags experimentellt vaccin, uppbyggt av noggrant utvalda små fragment från bakterien, med det långsiktiga målet att skydda personer som exponeras via mat, vatten eller klimatrelaterade översvämningar.

Från dold hotbild till tydligt mål
Vibrio fluvialis har ofta förväxlats med andra Vibrio-arter, vilket innebär att dess roll i matburna sjukdomar sannolikt underskattats. Utbrott har kopplats till förorenade skaldjur och förorenat vatten, och nyligen har stormar och översvämningar fört dessa bakterier inåt land och gjort människor sjuka långt från kusten. Många patienter behöver sjukhusvård, och en oroande andel stammar är nu resistenta mot flera antibiotika. Eftersom mikroorganismens yta liknar relaterade bakteriers kan läkare feldiagnostisera infektioner, vilket fördröjer rätt behandling. Allt detta skapar ett starkt behov av förebyggande åtgärder snarare än att enbart förlita sig på läkemedel.
Att designa ett vaccin i en dator
I stället för att odla hela bakterier i labbet använde forskarna "immunoinformatik" — programvara som förutsäger vilka små delar av Vibrio fluvialis som mest sannolikt upptäcks och angrips av det mänskliga immunsystemet. De fokuserade på två membranproteiner som sitter på bakteriens yta och är viktiga för dess överlevnad och förmåga att orsaka sjukdom. Från dessa proteiner extraherade teamet tio korta segment, kallade epitoper, som kan kännas igen av både T‑celler och B‑celler, immunsystemets huvudförsvarare. De fogade sedan ihop dessa delar till en enda kedja om 246 aminosyror, lade till korta spacers så att immunsystemet kan bearbeta varje del korrekt, samt ett adjuvantfragment för att förstärka det övergripande svaret.
Kontroll av styrka, säkerhet och global räckvidd
När det virtuella vaccinet byggts körde teamet en serie tester helt in silico, det vill säga på datorer snarare än i djur eller människor. Programmen förutspådde att den kombinerade konstrukten skulle vara starkt "synlig" för immunsystemet men osannolik att utlösa allergi eller toxicitet. De valda epitoperna matchade vanliga varianter av immungener runt om i världen, vilket tyder på att ungefär 99,97 procent av världens befolkning bör kunna svara, inklusive personer i hårt drabbade regioner som Syd- och Östasien. Vaccinproteinet verkade också stabilt, tillräckligt hydrofilt för att lösa sig bra och lämpligt för effektiv produktion i vanliga laboratoriebakterier, vilket gör framtida tillverkning mer praktisk.
Hur vaccinet kan väcka skydd
Forskarna undersökte därefter om det designade proteinet rimligtvis skulle kunna interagera med en verklig immunsensor. Genom moderna strukturförutsägelseverktyg byggde de en tredimensionell modell av vaccinet och simulerade sedan hur det skulle kunna fästa vid Toll‑like receptor 2 (TLR2), en molekyl på immunceller som känner igen bakteriekomponenter. Datordockning föreslog en tät passform mellan vaccinet och TLR2, understödd av många stabiliserande molekylära kontakter. Långa, detaljerade rörelsesimuleringar över 100 nanosekunder indikerade att vaccin‑receptorkomplexet förblev stabilt och kompakt över tid. Ytterligare simuleringar av immunsvaret förutspådde starka vågor av antikroppar och T‑cellsaktivitet, tillsammans med bildning av minnesceller som i princip skulle kunna ge bestående skydd mot Vibrio fluvialis.
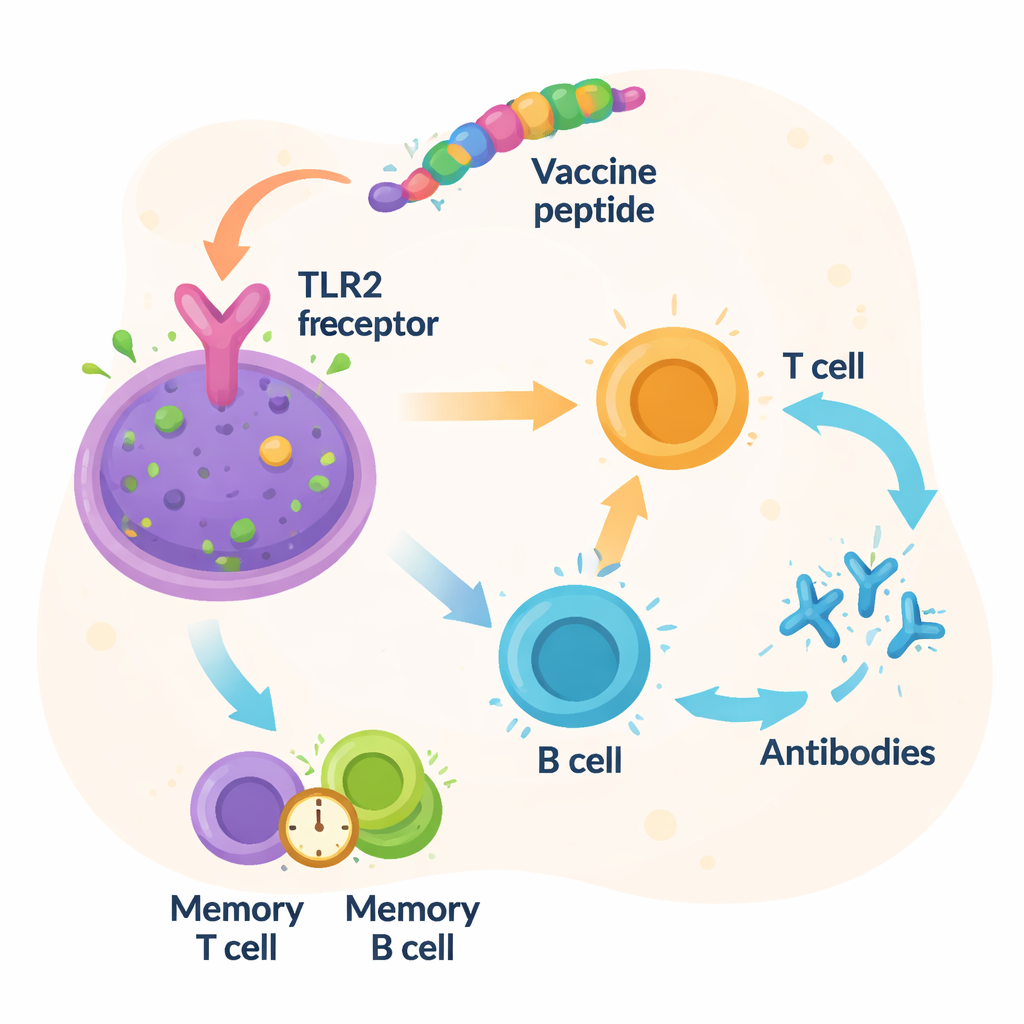
Från digital ritning till verkligt skydd
Förenklat erbjuder detta arbete en digital "ritning" för ett framtida Vibrio fluvialis‑vaccin uppbyggt av endast bakteriens viktigaste fragment, arrangerade för att vara brett effektiva och potentiellt säkrare än helcellsvacciner. Studien visar att denna konstruktion bör vara igenkännbar för de flesta människors immunsystem, binda väl till en nyckelimmunsensor och vara möjlig att tillverka med standardverktyg. Dock kommer alla dessa resultat från datorbaserade modeller. Nästa steg kräver att vaccinet produceras i labbet, testas i celler och djur, och så småningom i mänskliga prövningar för att bekräfta att det verkligen skyddar mot infektion utan att orsaka skada. Om dessa tester lyckas kan sådana multi‑epitopvacciner bli kraftfulla nya verktyg mot matburna bakterier i en varmare och tätare värld.
Citering: Naveed, M., Husnain, M., Aziz, T. et al. Immunoinformatics-based design and evaluation of a multi-epitope vaccine against Vibrio fluvialis. Sci Rep 16, 4100 (2026). https://doi.org/10.1038/s41598-026-35434-4
Nyckelord: Vibrio fluvialis, multi-epitopvaccin, matburen infektion, immunoinformatik, antibiotikaresistens