Clear Sky Science · sv
Utveckling av ett globalt screensystem för att upptäcka protein–protein-interaktioner med luminescenskomplementering i fissionsjäst
Ljussättning av proteinernas dolda liv
Varje hjärtslag, tanke och andetag i våra kroppar bygger på att proteiner samarbetar inne i cellerna. Dessa små partnerskap, kallade protein–protein-interaktioner, styr allt från hur gener avläses till hur celler svarar på stress. Många av dessa samarbeten är dock flyktiga eller känsliga, vilket gör dem svåra att upptäcka med befintliga verktyg. Denna studie beskriver ett nytt, mycket känsligt ”ljusbaserat” screensystem uppbyggt i en enkel modellorganism, fissionsjäst, för att samtidigt avslöja tusentals sådana dolda proteinförbindelser.
Varför proteinpartnerskap är så svåra att se
Proteiner arbetar sällan ensamma. De binder olika partners vid olika tillfällen, ibland bara för ögonblick, och deras beteende kan ändras av kemiska modifieringar eller av var de befinner sig i cellen. Traditionella metoder för att studera dessa interaktioner drar antingen ut proteiner ur deras naturliga miljö eller förlitar sig på genetiska knep som inte fångar alla bindningar. Som en följd är de nuvarande kartorna över vem som interagerar med vem ofullständiga. Författarna ville förbättra denna bild genom att skapa ett mer flexibelt, känsligt system som kunde undersöka praktiskt taget varje protein i fissionsjäst i levande celler.
Att förvandla beröring till ljus
Kärnan i den nya metoden är ett uppdelat enzym som avger ljus. En del, kallad LgBiT, fästs vid ett ”bete”-protein som forskarna vill studera. Den andra delen, SmBiT, fästs vid många möjliga ”byte”-partners, en per jästkultur. Var för sig interagerar dessa två enzymdelar knappt. Men när bete och byte binder varandra inne i cellen slår delarna samman och återskapar ett fungerande enzym som lyser i närvaro av ett kemiskt bränsle. Genom att mäta hur mycket ljus varje jästkultur producerar kan teamet avgöra vilka proteiner som faktiskt möts inne i cellen och hur starkt de interagerar. För att undvika att missa partners på grund av att taggen blockerar normal funktion görs beteproteinet i två versioner, med LgBiT fäst antingen i början eller slutet, vilket kraftigt ökar chansen att åtminstone en orientering fungerar. 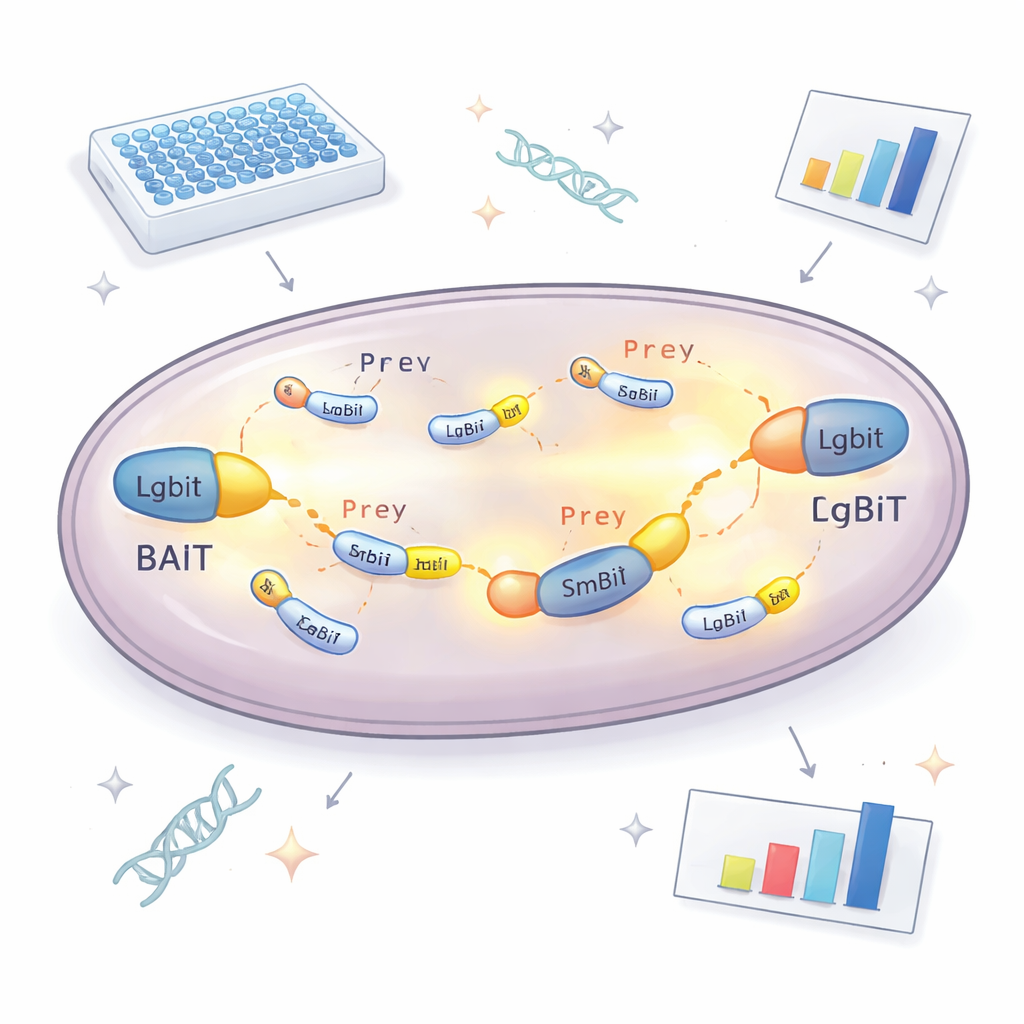
Konstruera ett jästbibliotek och strainsystem
Att bygga denna plattform krävde mer än ett smart enzym. Forskarna behövde också införa tusentals byteproteiner i jästen på ett kontrollerat sätt, i enkelkopior. De designade en speciell DNA-vektor för byteproteiner som integreras i en definierad plats i jästgenomet och bär en röd fluorescerande markör. Intensiteten i denna röda signal återspeglar hur många kopior som införts, vilket gör det enkelt för teamet att välja kolonier med exakt en kopia — avgörande för tillförlitliga jämförelser. De skapade också dedikerade betevektorer som placerar LgBiT i början eller slutet av beteproteinet, separerade av flexibla länkar så att proteinet fortfarande kan vika och röra sig normalt. Noggrant konstruerade jäststammar byggdes därefter för att samtidigt hysa två bete- konstruktioner och en byte-konstruktion, med näringsmarkörer för att säkerställa att endast korrekt kombinerade celler överlever.
Sätta systemet på prov
För att kontrollera om deras design verkligen förbättrade detektion undersökte forskarna först proteiner med välkända partners. De bekräftade att signalstyrkan i hög grad berodde på var den ljusproducerande taggen var fäst: vissa interaktioner syntes bara när LgBiT satt i ena änden av betet, och inte i den andra. Att uttrycka båda versionerna samtidigt ökade ljusutbytet, vilket visar att den dubbla-bete-strategin gör svaga eller orienteringskänsliga interaktioner lättare att fånga. Systemet upptäckte också kontakter som involverar membranbundna proteiner, en klass som är ökända för att vara svår för traditionella jäst två-hybridmetoder. Med denna validering i handen skalade teamet upp till en genomomfattande screen med ett transkriptionsrelaterat protein kallat Tfs1 som bete. Genom att screena mer än 4 600 byteproteiner hittade de 31 starka kandidater, inklusive flera redan kända partners och många nya, några belägna utanför kärnan i områden som mitokondrier och cellens yta. 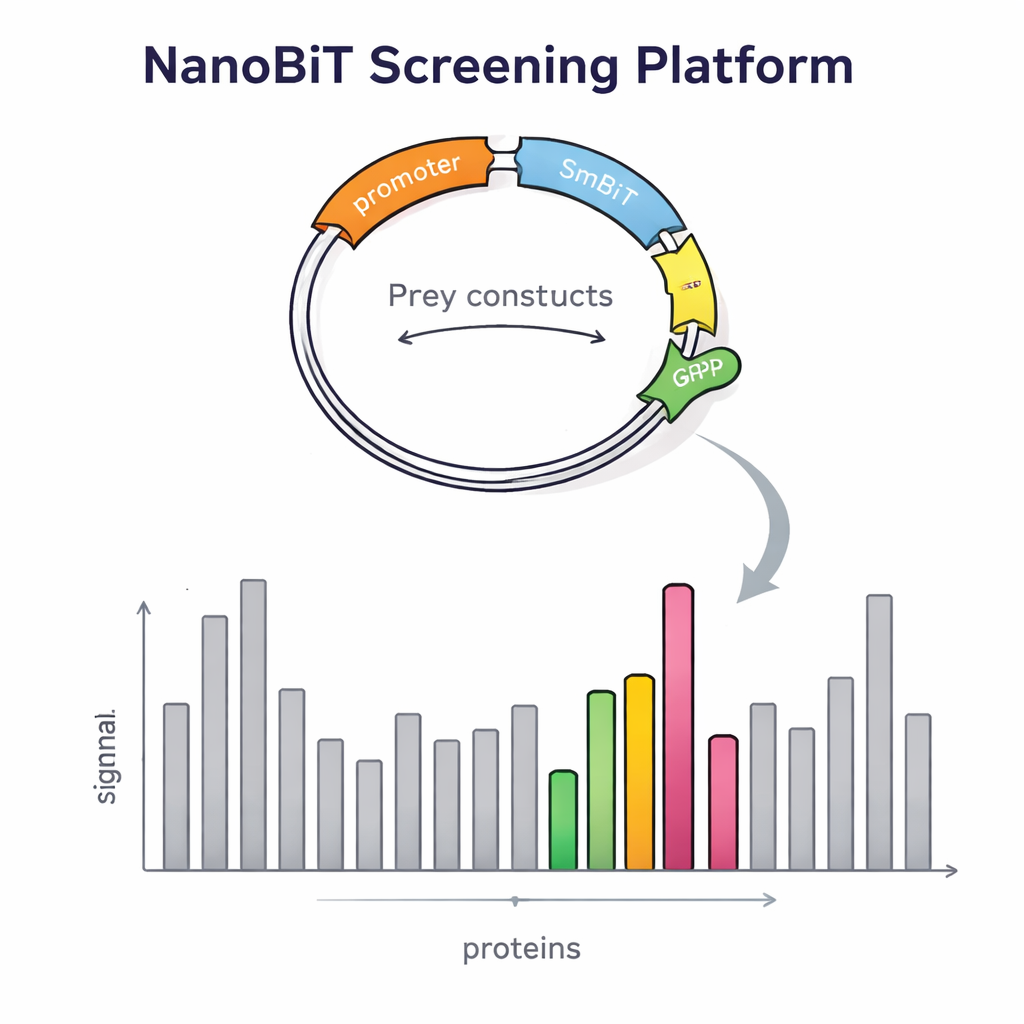
Vad detta innebär för biologi och läkemedelsupptäckt
För en lekman är huvudbudskapet att författarna byggt ett mer känsligt ”interaktionsradar” inne i jästceller. Genom att omvandla korta proteinhälsningar till mätbara ljusblixtar, och genom att smart ordna genetiken så att tre taggade proteiner kan uttryckas samtidigt, avslöjar deras system både kända och tidigare osynliga proteinpartners. Även om ytterligare kontroll med andra tekniker krävs för att bekräfta varje nytt par är denna plattform ett viktigt verktyg för att fylla luckor i våra kartor över cellulära nätverk. Eftersom stammarna också konstruerats för att vara mer känsliga för småmolekyler kan samma uppsättning anpassas för att söka efter läkemedel som antingen stör skadliga proteinpartnerskap eller stabiliserar gynnsamma sådana, vilket erbjuder ett kraftfullt nytt verktyg för både grundforskning och tidig läkemedelsupptäckt.
Citering: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Nyckelord: proteinintringar, fissionsjäst, luminescensanalys, höggenomströmningsscreening, verktyg för läkemedelsupptäckt