Clear Sky Science · sv
Signaligenkänningspartikelberoende sekretom hos människor
Hur celler avgör vilka proteiner som lämnar cellen
Våra celler skickar ständigt ut proteiner som bildar hormoner, antikroppar och det stödjande nätverket mellan vävnader. Men inte varje protein är tänkt att färdas utanför cellen. Denna studie ställer en grundläggande men obesvarad fråga: hur avgör mänskliga celler vilka proteiner som är beroende av en viktig hjälpare kallad signaligenkänningspartikel (SRP) för att nå cellens interna fraktcentral, och vilka som klarar sig utan den? Genom att kartlägga detta beslut över tusentals proteiner samtidigt visar författarna vilka som är beroende av SRP, vilka som inte är det, och vad som händer när detta system bryter samman — ett ämne som är relevant för många sjukdomar kopplade till felriktade eller saknade sekretoriska proteiner.
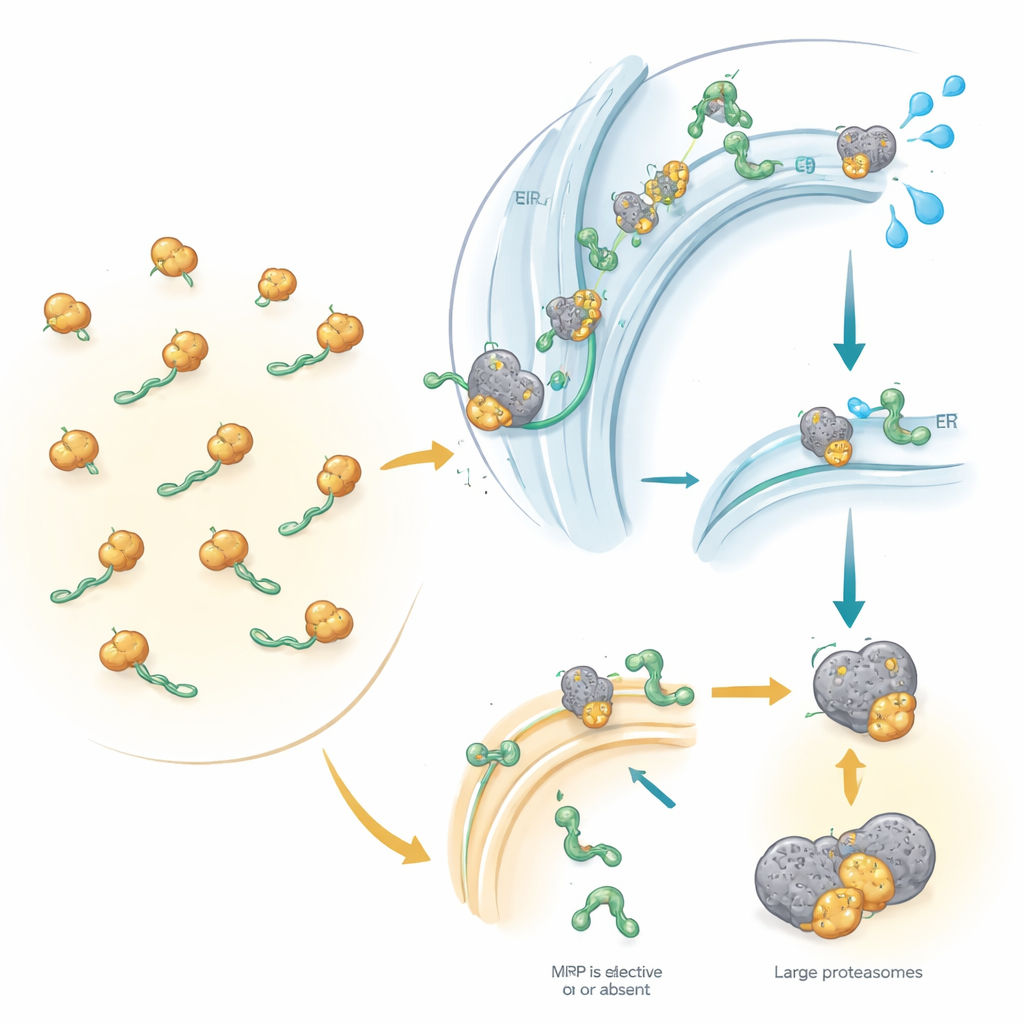
Cellens fraktdocka och dess huvudsakliga guide
Cirka en av tre mänskliga proteiner är avsedd antingen för cellens yta, cellmembran eller för utsöndring utanför cellen. För att nå rätt plats måste de flesta av dessa proteiner först gå in i ett nätverk av interna membran kallat det endoplasmatiska retiklet, cellens fraktdocka. SRP fungerar som en guide: den känner igen en liten ”adresslapp” i början av nydanade proteiner och pausar tillfälligt deras produktion. Denna paus ger ribosomen — proteinproduktionsmaskinen — tid att docka vid det endoplasmatiska retiklet, där produktionen återupptas och det växande proteinet träddes in i eller genom membranet. Vissa proteiner använder dock alternativa vägar som inte kräver SRP, särskilt mycket små proteiner eller de som är förankrade i sitt svansände. Fram tills nu visste forskare inte, i global skala, vilka mänskliga proteiner som verkligen kräver SRP och vilka som kan kringgå det.
Nedreglering av SRP för att se vad som går sönder
För att besvara detta minskade forskarna selektivt nivån av en väsentlig SRP-komponent, SRP54, i mänskliga HeLa-celler. De använde därefter en känslig teknik kallad masspektrometri för att mäta över 6 000 proteiner inne i cellerna och nästan 2 000 proteiner i vätskan runt cellerna, så kallat conditioned medium. Genom att jämföra celler med normal SRP54-nivå med celler där SRP54 var utarmad kunde de se vilka proteiner som blev mindre förekommande, vilka som ökade och vilka som förblev oförändrade. Ett starkt fall i en proteins nivå — särskilt både inne i cellen och i mediet — tolkades som ett tecken på att detta protein är beroende av SRP för att bli korrekt syntetiserat och riktat.
Vilka är beroende av SRP och vilka klarar sig utan
Analysen visade att majoriteten av de proteiner som normalt utsöndras till mediet tydligt är beroende av SRP. När SRP54 minskades föll de flesta av dessa sekretoriska proteiner kraftigt, särskilt de som bär en klassisk signal ”adresslapp”. Många membranproteiner inne i cellen minskade också, vilket identifierar dem som SRP-klienter. En mindre grupp proteiner med liknande adresslappar påverkades i stor utsträckning inte, vilket markerar dem som SRP-oberoende; dessa använder sannolikt alternativa vägar för att nå det endoplasmatiska retiklet. Forskarna upptäckte också att särskilda egenskaper hos adresslappen — till exempel ett positivt laddat område i dess början — var vanligare bland SRP-beroende proteiner, vilket antyder subtila regler som hjälper SRP att välja sitt last. Samtidigt ökade vissa proteiner involverade i märkning av skadade proteiner för nedbrytning och i mitokondriell funktion, vilket tyder på att cellerna aktiverar reservsystem och energiproduktion när deras huvudsakliga fraktguide är komprometterad.
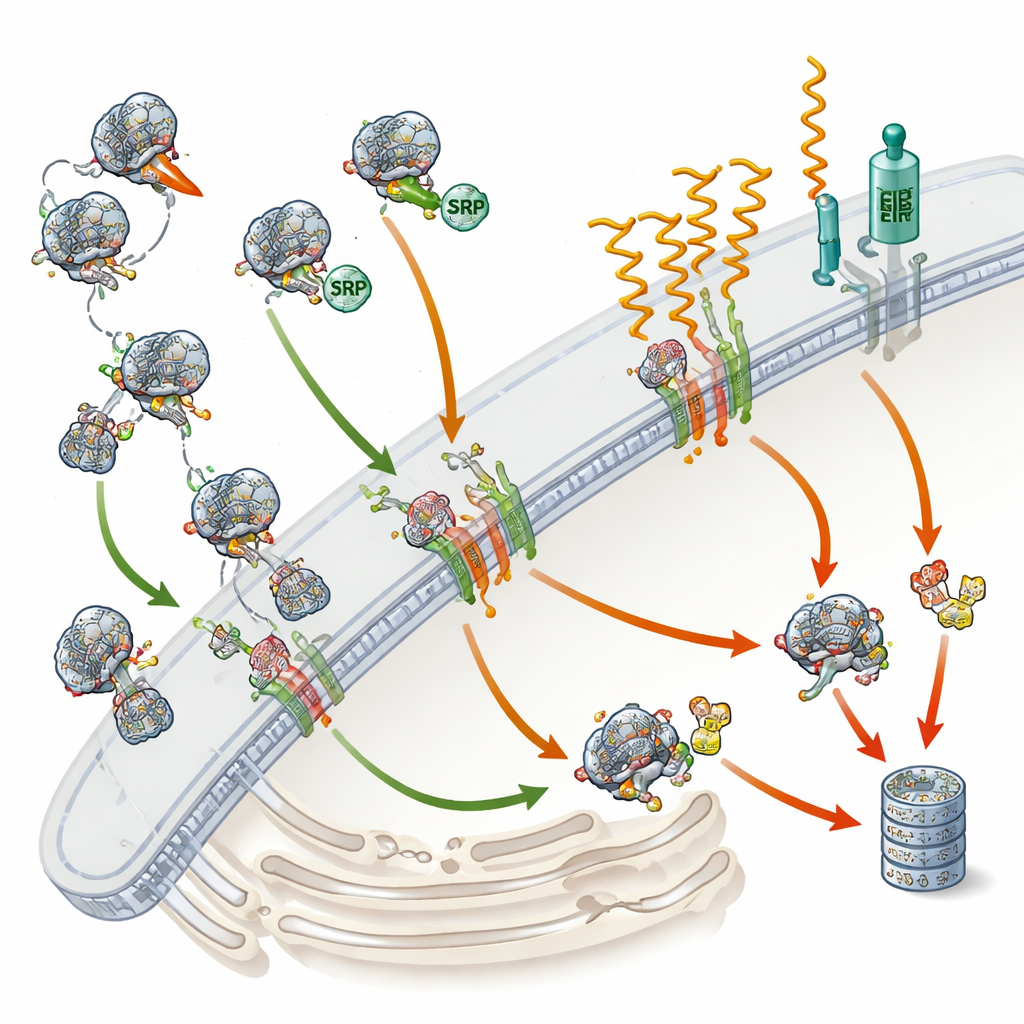
Kvalitetskontroll när riktningen misslyckas
Studien gick bortom att bara räkna proteiner: den jämförde dessa förändringar med skiften i budbärar-RNA, de ritningar som används för att skapa proteiner. Många SRP-beroende proteiner förlorade inte bara protein utan även sina RNA-ritningar, vilket inbegriper en kvalitetskontrollväg känd som RAPP. När SRP inte kan engagera ett framväxande sekretoriskt eller membranprotein verkar denna väg trigga nedbrytningen av motsvarande RNA, vilket förhindrar fortsatt produktion av ett felriktat protein. Samtidigt märks ofullständigt tillverkade proteiner som misslyckas med att nå det endoplasmatiska retiklet sannolikt med små molekylflaggor och matas till cellens ”malningsmaskiner” kallade proteasomer. Intressant nog aktiverades inte de klassiska stressvägarna i det endoplasmatiska retiklet starkt, vilket antyder att defekt SRP framkallar en distinkt typ av cellulär stressreaktion.
Vad detta betyder för hälsa och sjukdom
Genom att för första gången i mänskliga celler kartlägga vilka utsöndrade och membranbundna proteiner som är SRP-beroende respektive SRP-oberoende, tillhandahåller detta arbete en referenskarta över cellens fraktregler. Resultaten visar att de flesta exporterade proteiner verkligen är beroende av SRP och att, när SRP brister, svarar cellerna genom att nedbryta både proteinerna och deras ritningar samtidigt som alternativa hanteringsmekanismer slås på. Eftersom många sjukdomsframkallande mutationer påverkar signalernas ”adresslappar” på sekretoriska proteiner kan förståelsen av exakt hur SRP känner igen sina klienter och hur RAPP avlägsnar felaktiga sådana hjälpa till att förklara varför vissa mutationer leder till hormonbrister, immunproblem eller neurodegeneration — och så småningom peka mot nya sätt att finjustera proteinroutning i mänsklig hälsa.
Citering: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Nyckelord: proteinutskiljning, signaligenkänningspartikel, sekretom, proteinkvalitetskontroll, endoplasmatiskt retikulum