Clear Sky Science · sv
Sekventiell platina- och PARP-hämning ökar PD1-immunterapins effektivitet i murint Brca2‑muterat pankreascancer
Varför denna forskning är viktig för patienter
Pankreascancer är en av de mest dödliga cancerformerna, och även när läkare vet att en tumör har ett potentiellt sårbart drag—till exempel en mutation i BRCA2‑genen—håller dagens behandlingar sällan sjukdomen under kontroll länge. Denna studie använder en realistisk musmodell för att ställa en praktisk fråga som många patienter och onkologer nu står inför: efter intensiv kemoterapi och en PARP‑hämmare, kan tillsats av modern immunterapi påtagligt förlänga överlevnaden, och varför återkommer tumörerna så ofta?
En seglivad cancer med ett genetiskt svagt ställe
Pankreasduktalt adenokarcinom är ökänd för att vara svårt att behandla, med femårsöverlevnad som fortfarande ligger i ensiffriga procent. En liten andel patienter bär ärftliga eller tumörspecifika defekter i BRCA2, en gen som behövs för att reparera brutet DNA. Dessa tumörer är ovanligt känsliga för läkemedel som skadar DNA, såsom platina‑baserad kemoterapi, och för PARP‑hämmare som ytterligare försvårar cancercellernas förmåga att reparera DNA. Dagens standardvård för avancerad BRCA‑muterad pankreascancer är månader av platinabaserad kemoterapi följt av underhållsbehandling med en PARP‑hämmare. I den viktiga POLO‑studien förlängde dock inte denna strategi den totala överlevnaden, vilket understryker behovet av att förstå resistens och utforma bättre underhållsstrategier.
Att bygga en mer verklighetstrogen musmodell
Många befintliga laboratoriemodeller avlägsnar immunceller och stromaceller som omger verkliga tumörer hos patienter. För att övervinna detta konstruerade författarna möss som utvecklar BRCA2‑defekta pankreastumörer i en miljö med ett fullt fungerande immunsystem. Från dessa spontana tumörer härledde de klonala cellinjer som kunde implanteras i genetiskt matchade möss. Dessa Brca2‑mutanta tumörer liknade och betedde sig mycket som humana pankreastumörer: de var tätt fibrotiska, uteslöt till stor del T‑celler och visade höga nivåer av spontan DNA‑skada. Avgörande var att tumörerna var mycket känsliga för en vanlig platina‑kombination (gemcitabin plus cisplatin), medan behandling med PARP‑hämmare ensam endast gav måttliga och kortvariga effekter hos djuren, trots stark aktivitet mot samma celler i odling. 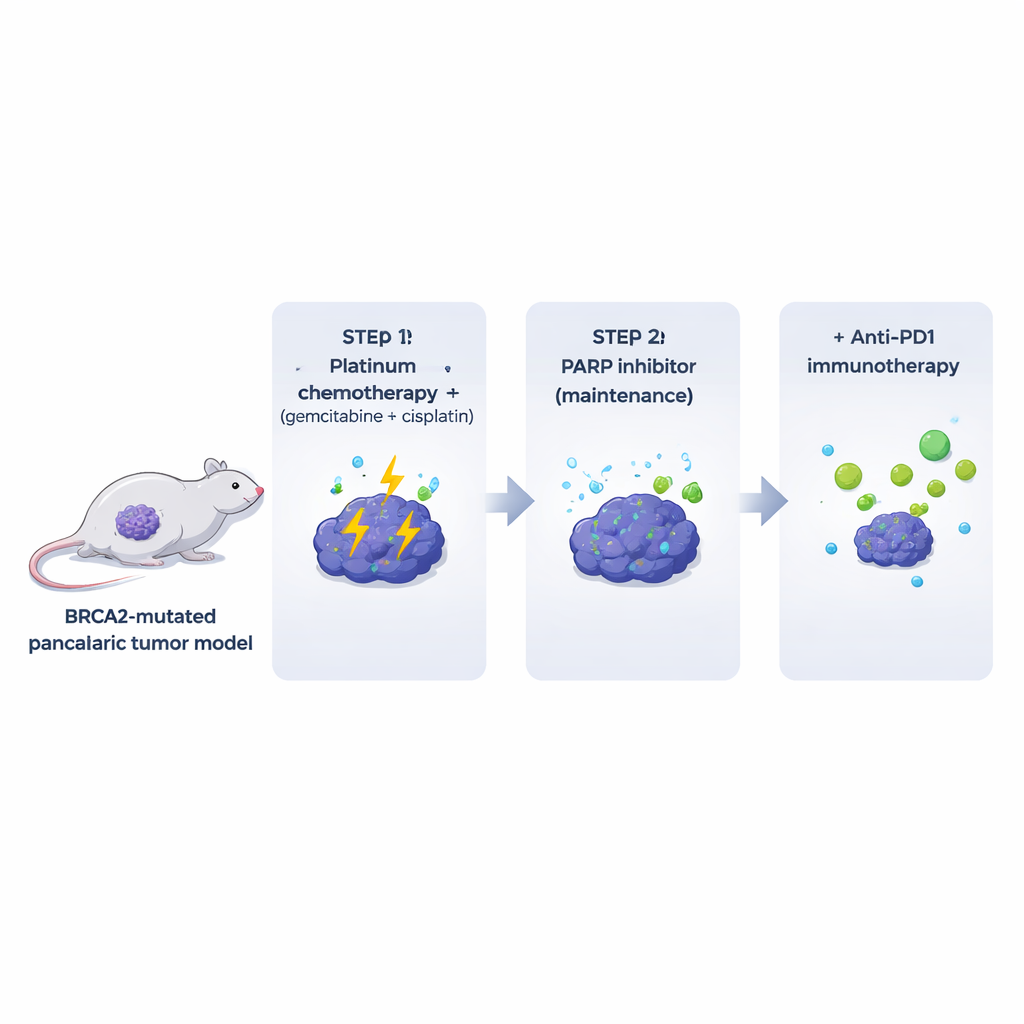
Kemoterapi omformar tumörens närområde
Teamet undersökte sedan vad som händer inne i tumören efter platinakemoterapi. Tio dagar efter behandling hade tumörerna krympt men inte utplånats. Genuttrycksanalys visade ett påtagligt skifte mot immunrelaterad aktivitet: vägar kopplade till T‑cellsaktivering och adaptiv immunitet var påslagna. Fler T‑celler hittades i behandlade tumörer, och många av dessa T‑celler bar tecken på utmattning—indikationer på att de aktiverats men blivit ineffektiva. Liknande mönster med ökad T‑cellspresens observerades i humana pankreastumörer med BRCA‑ eller relaterade PALB2‑mutationer efter att patienter erhållit platinabaserad kemoterapi före operation. Samtidigt ökade tumörcellerna nivåerna av PD‑L1, ett ytprotein som kan stänga av T‑celler genom att binda PD‑1‑receptorn, vilket tyder på att tumörerna försvarade sig mot detta nya immunologiska tryck.
Varför PARP ensam inte räcker—och var resistens uppstår
I likhet med patientvård gav forskarna mössen en initial kur med gemcitabin och cisplatin, följt av underhåll med PARP‑hämmaren olaparib. Denna sekvens förbättrade tumörkontroll och överlevnad jämfört med bara kemoterapi, vilket bekräftar att föregående kemoterapi kan göra tumörer mer mottagliga för PARP‑hämning. Dock botades inga möss: tumörerna växte så småningom tillbaka under PARP‑underhåll. Resistenta tumörer uppvisade ett mer differentierat utseende och kraftigt ökade nivåer av utvecklingsregulatorn CDX2. Detta tyder på att resistens, åtminstone i denna modell, inte enbart uppstår genom återställande av den ursprungliga DNA‑reparationsdefekten, utan kan involvera ett skifte i tumörens cellulära identitet. CDX2 skulle potentiellt kunna fungera som en biomarkör för framväxande resistens hos patienter.
Att låsa upp immunterapi med rätt sekvens
Immunkontrollpunktläkemedel som anti‑PD1‑antikroppar har förändrat behandlingen för flera cancerformer, men pankreascancer har förblivit i stort sett okänslig. Föga förvånande gav anti‑PD1 (med eller utan en annan kontrollpunktfaktor, anti‑CTLA4) inget genomslag när det gavs till behandlingsnaiva BRCA2‑mutanta tumörer, och gjorde heller liten nytta när det bara lades till PARP‑hämmarbehandling. Bilden ändrades när hela sekvensen användes: platinakemoterapi först, därefter PARP‑hämning plus anti‑PD1 som underhåll. I detta scenario krympte tumörerna mer uttalat och mössen levde längre än vid kemoterapi plus PARP‑hämmare eller anti‑PD1 ensam. Tillägg av anti‑CTLA4 till PARP‑underhåll gav inte liknande fördelar, vilket tyder på att det kemoterapi‑primade tumörmiljön är speciellt mottagligt för PD‑1‑blockad. 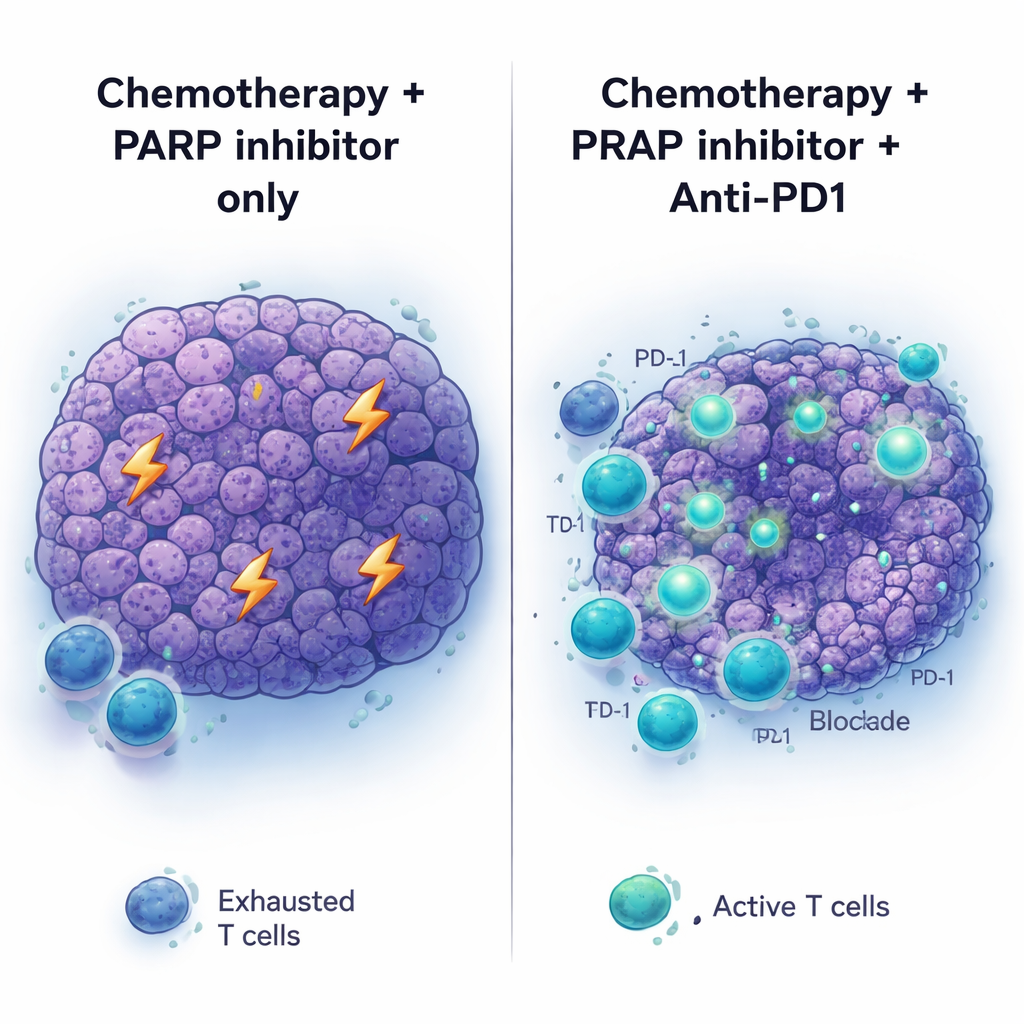
Vad detta kan innebära för framtida vård
Sammantaget hävdar studien att för BRCA‑muterad pankreascancer spelar ordningen och kombinationen av behandlingar stor roll. Stark DNA‑skadande kemoterapi angriper inte bara tumörceller direkt utan väcker också en immunrespons, även om den responsen initialt dämpas av utmattning och PD‑L1‑försvar. PARP‑hämmare kan förlänga nyttan men är osannolikt kurativa på egen hand och kan driva tumörer mot ett resistent, CDX2‑högt tillstånd. Genom att lägga anti‑PD1‑immunterapi ovanpå PARP‑underhåll efter platinakemoterapi kan det vara möjligt att omvandla detta kortvarigt inflammerade, utmattade immunscenario till en mer effektiv och varaktig antitumoral attack. Pågående kliniska prövningar som kombinerar PARP‑hämmare med immunterapi vid BRCA‑relaterad pankreascancer blir avgörande för att avgöra om denna omsorgsfullt tajmade strategi kan ge längre, bättre liv för patienter.
Citering: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Nyckelord: pankreascancer, BRCA2‑mutation, platinakemoterapi, PARP-hämmare, PD‑1-immunterapi