Clear Sky Science · sv
Indirubinbehandling förknippades med modulering av PI3K/AKT- och MAPK-vägarna samt induktion av apoptos och autofagi
En ny vinkel på behandling av livmoderhalscancer
Livmoderhalscancer är fortfarande en av de ledande orsakerna till cancerrelaterad dödlighet hos kvinnor globalt, och nuvarande behandlingar som kirurgi, kemoterapi och strålning kan vara påfrestande och ibland ineffektiva i avancerad sjukdom. Denna studie undersöker om indirubin, en naturlig förening härledd från en traditionell kinesisk medicin, kan bromsa tillväxten av livmoderhalscancer och döda cancerceller samtidigt som den verkar via välkända cellulära överlevnadsbrytare inne i tumörer. För läsaren ger den en inblick i hur ett gammalt botemedel kan omformas till en modern, mer riktad cancerbehandling.
Varför ett växtpigment fångade forskarnas intresse
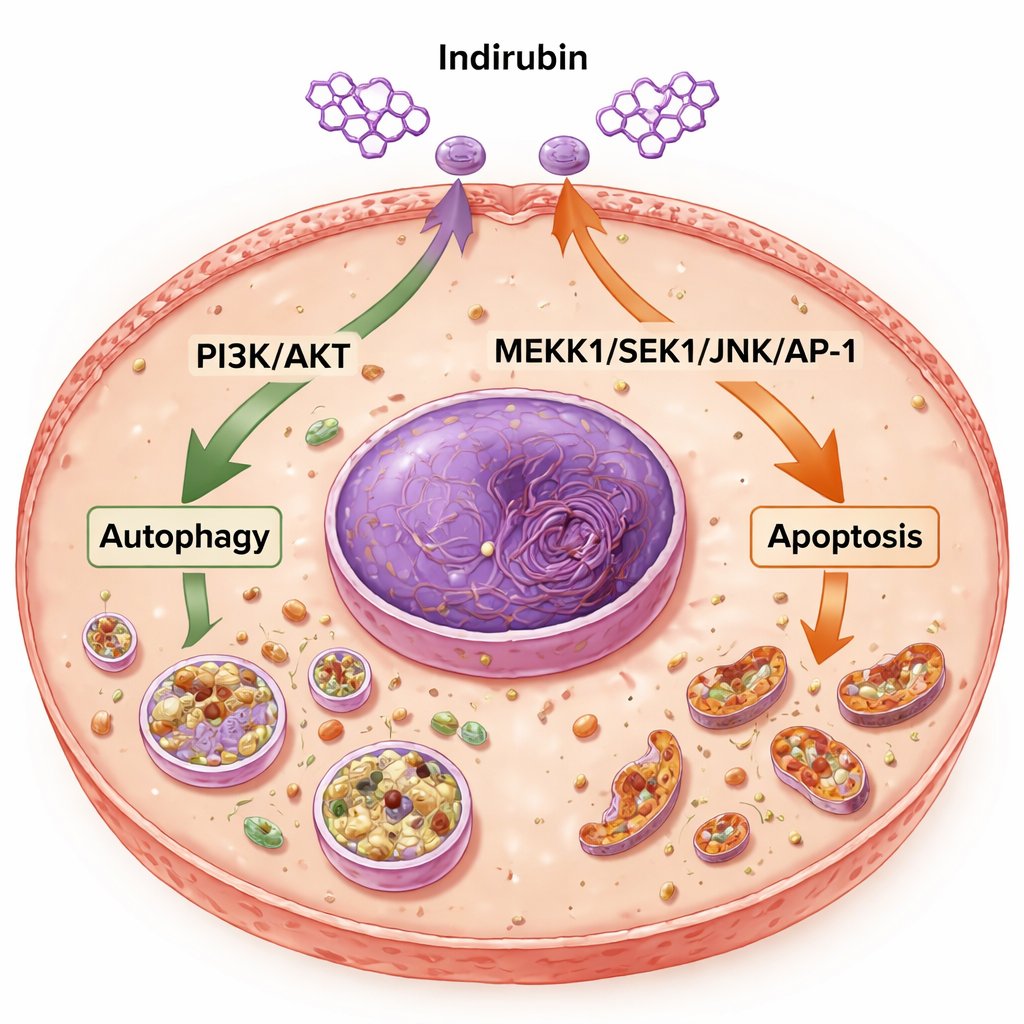
Indirubin är ett pigment som finns i indigo naturalis, ett preparat som länge använts inom traditionell kinesisk medicin. Tidigare forskning har visat att det kan hämma tillväxten av flera typer av cancerceller, men hur det fungerar i livmoderhalscancer var inte väl förstått. Författarna fokuserade på två stora kontrollsystem inne i cellerna. Det ena är PI3K/AKT-vägen, ofta beskriven som en tillväxt- och överlevnads"på-knapp" i många tumörer. Det andra är en del av MAPK-familjen av vägar, specifikt en kedja kallad MEKK1/SEK1/JNK/AP-1, som hjälper celler att avgöra om de ska anpassa sig till stress eller dö. Genom att undersöka dessa brytare hoppades teamet se om indirubin kunde styra livmoderhalscancerceller bort från överlevnad och mot självförstörelse.
Test av indirubin i möss och mänskliga cancerceller
För att undersöka indirubins effekter genomförde forskarna två huvudsakliga experimentserier. I möss implanterade de livmoderhalscancerceller under huden och behandlade djuren med olika doser indirubin eller med standardkemoterapiläkemedel. I laboratoriet behandlade de HeLa-celler — en väletablerad cellinje från livmoderhalscancer — med ökande koncentrationer av indirubin och mätte hur många celler som överlevde, hur många som gick in i programmerad celldöd (apoptos) och hur väl cellerna aktiverade sin interna "självrensnings"-process, känd som autofagi. De följde också musens vikt och följde noggrant djurvälfärdsregler för att säkerställa att eventuella antitumöreffekter inte enbart berodde på generell toxicitet.
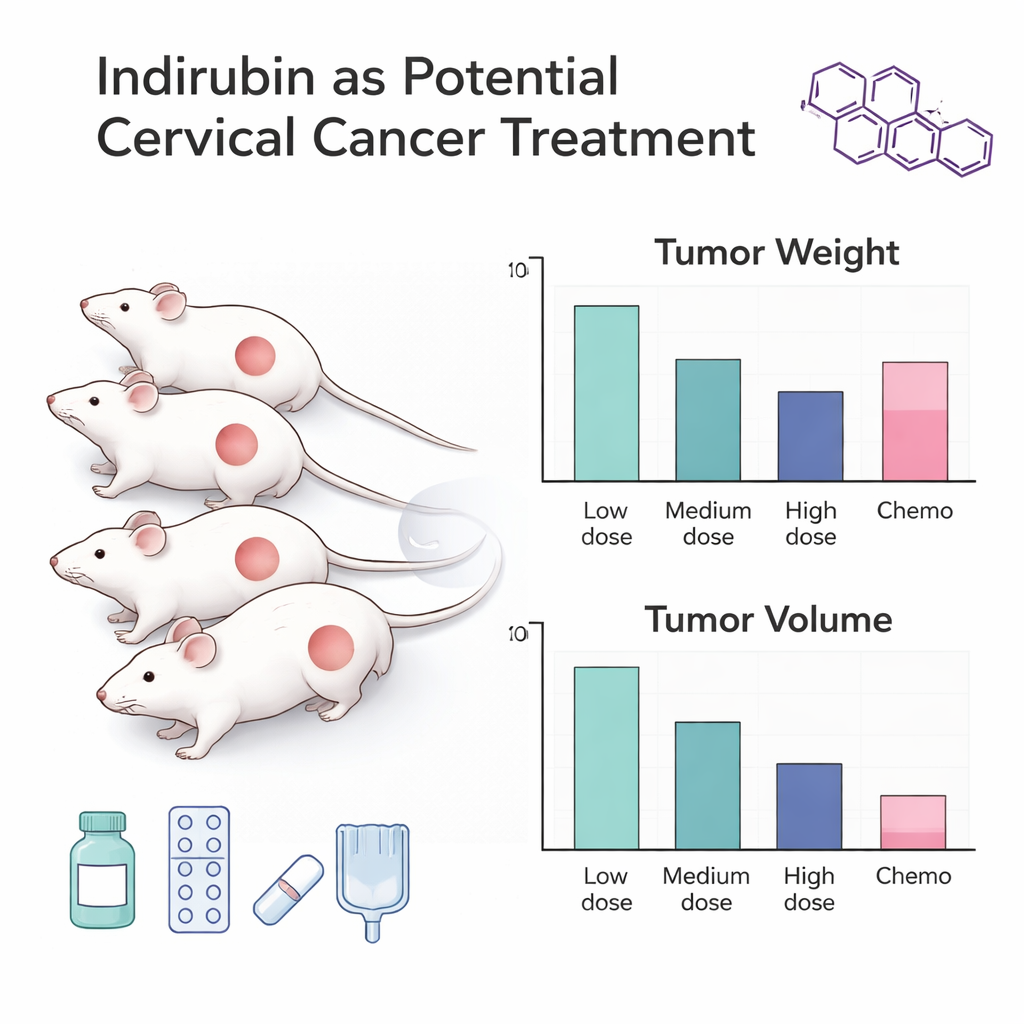
Bromsade tumörer och utlöste cellsjälvmord
I möss krympte tumörerna tydligt i en dosberoende utsträckning: högre doser gav mycket lättare och mindre tumörer, samtidigt som djuren bibehöll normal kroppsvikt, vilket tyder på att läkemedlet inte orsakade allvarlig systemisk skada. I cellkultur minskade indirubin antalet levande HeLa-celler över tid och vid stigande doser. Vid de högsta testade nivåerna dödade indirubin fler livmoderhalscancerceller än standardkemoterapiläkemedel såsom cisplatin och ifosfamid. Flödescytometri, en teknik som sorterar och räknar celler, visade att indirubinbehandlade celler var betydligt mer benägna att befinna sig i tidiga eller sena stadier av apoptos, vilket innebär att föreningen kraftigt uppmuntrade cancerceller att genomgå kontrollerad självförstörelse istället för att fortsätta dela sig.
Omkoppling av cellens överlevnadskretsar
Genom att gräva djupare visade teamet att indirubin ändrade balansen av nyckelproteiner som styr cellens öde. Det ökade markörer för autofagi, vilket indikerar att cellernas återvinningsmaskineri var mer aktivt, samtidigt som nivåerna av p62 minskade, ett protein som vanligtvis sjunker när denna process ökar. Samtidigt dämpade indirubin aktiviteten i PI3K/AKT-vägen — både på nivån av genbudskap och genom minskad fosforylering, den kemiska "på"-signalen på dessa proteiner. Läkemedlet sänkte också nivåerna av BCL2, ett protein som blockerar celldöd, och ökade nivåerna av Bax, en dödsfrämjande partner, vilket tippar vågskålen mot apoptos. I tumörvävnader från möss undertryckte indirubin på liknande sätt MEKK1/SEK1/JNK/AP-1-vägen, vilket tyder på att det dämpade ytterligare en stressresponssignal som tumörer utnyttjar för att överleva och sprida sig.
Vad detta kan betyda för framtida patienter
För icke-specialister är huvudbudskapet att indirubin, en förening med rötter i traditionell medicin, kunde bromsa tillväxten av livmoderhalscancer och driva cancerceller mot självrensning och självförstörelse genom att stänga av kraftfulla interna överlevnadsbrytare. Den visade dessa effekter både i djurmodeller och i odlade celler, och gjorde det utan uppenbar skada på mössen. Även om dessa fynd fortfarande är prekliniska och långt ifrån rutinmässig användning i kliniken, ger de en vetenskaplig grund för vidare studier och så småningom humana prövningar. Om framtida forskning bekräftar dess säkerhet och effektivitet kan indirubin eller relaterade föreningar en dag bli en del av verktygslådan för riktade behandlingar som gör livmoderhalscancerbehandling mer precis och mindre påfrestande.
Citering: Xie, X., Liu, C., Liu, X. et al. Indirubin treatment was associated with modulation of the PI3K/AKT and MAPK pathways and induction of apoptosis and autophagy. Sci Rep 16, 5155 (2026). https://doi.org/10.1038/s41598-026-35382-z
Nyckelord: livmoderhalscancer, indirubin, traditionell kinesisk medicin, cellsignaleringsvägar, apoptos och autofagi