Clear Sky Science · sv
Störning av intracellulär järnhomeostas genom mitokondriell dysfunktion associerad med hämning av ATP13A2‑uttryck
Varför järn inne i hjärncellerna är viktigt
Parkinsons sjukdom är mest känd för tremor och stelhet, men djupt inne i de påverkade hjärncellerna utspelar sig en annan dramatik: järn, en nödvändig metall, börjar ansamlas där det inte bör göra det. Denna studie ställer en enkel men viktig fråga: hur uppstår denna järnansamling, och hur kan den skada nervcellernas små kraftverk och återvinningscentraler? Genom att besvara den ger arbetet ledtrådar till varför vissa hjärnregioner degenererar vid Parkinsons och närliggande sjukdomar, och pekar mot nya behandlingsvägar som går bortom att bara ersätta dopamin.
Närmare om en sällsynt genetisk ledtråd
Forskarna fokuserar på en sällsynt ärftlig form av Parkinsons sjukdom, kallad PARK9, orsakad av defekter i genen ATP13A2. Denna gen kodar för ett protein som sitter i lysosomer, cellens avfalls- och återvinningskompartiment. Personer med ATP13A2‑mutationer kan också utveckla ett tillstånd med järnavlagringar i hjärnan. Den kopplingen gjorde ATP13A2 till en idealisk ingång för att studera hur järnbalansen rubbas. Med en human neuronlik cellinje som överproducerar Parkinsonsproteinet alfa‑synuklein använde teamet små RNA‑fragment för att sänka ATP13A2 och följde sedan hur järn, energiproduktion och cellhälsa förändrades.
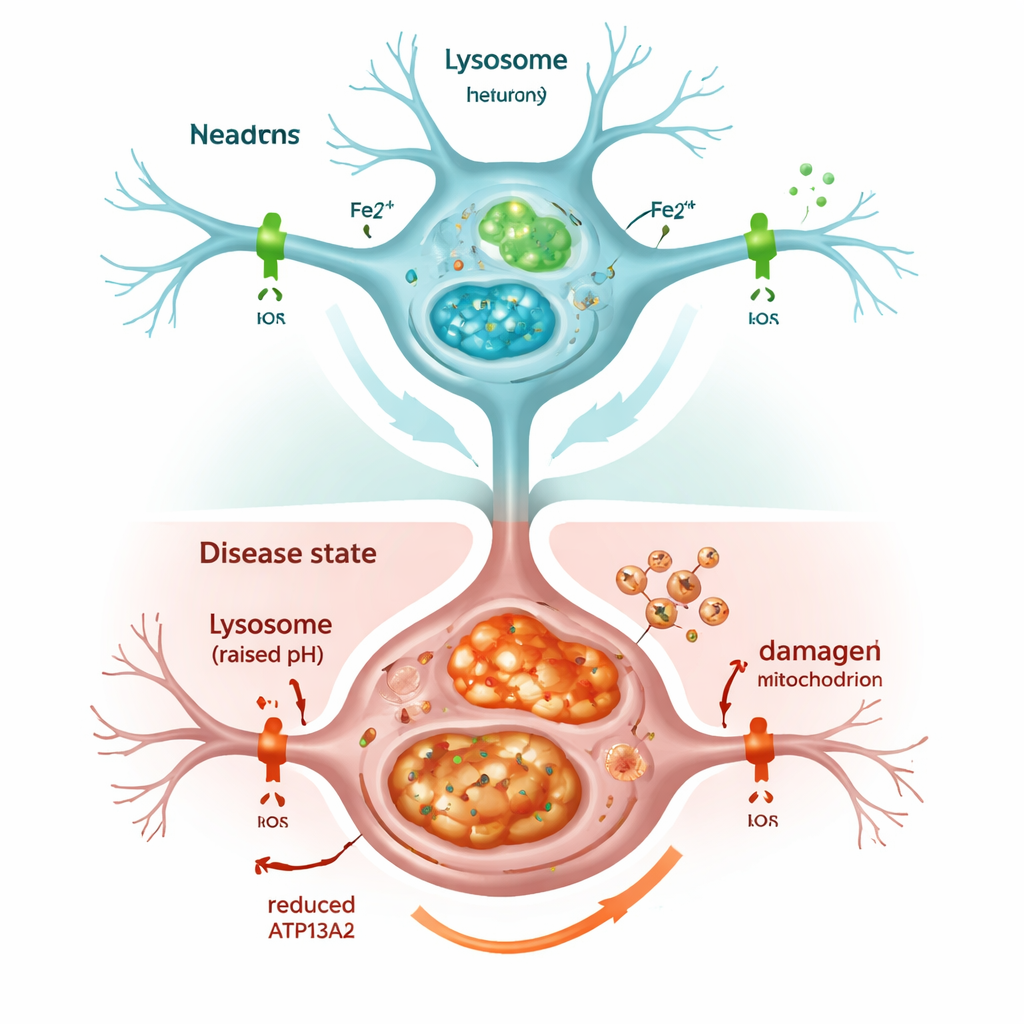
När cellens återvinningssystem stannar av
Att stänga av ATP13A2 försvagade snabbt lysosomerna. Deras inre surhetsgrad, som är avgörande för nedbrytning av oönskat material, sjönk, och markörer för cellens nedbrytningsprocess, autophagi, ackumulerades istället för att rensas bort. Som ett resultat byggdes alfa‑synuklein upp, vilket speglar det som ses i Parkinsons hjärnor. Cellerna visade också mer järn totalt, och särskilt mer av den kemiskt aktiva formen, kallad Fe2+, inne i både lysosomer och mitokondrier. Cellen svarade genom att tillverka mer ferritin, ett järnlagrande protein, men detta räckte inte för att förhindra skada: de överbelastade mitokondrierna producerade överskott av reaktiva syremolekyler och cellöverlevnaden minskade. Behandling av cellerna med ett järnbindande läkemedel, liknande sådana som används kliniskt, minskade denna oxidativa stress och räddade delvis cellernas livskraft, vilket understryker att överskott av järn i sig var en central orsak till skadan.
Järnsensorer slutar lyssna på metallen
Vanligtvis har celler ett återkopplingssystem som märker när järnnivåerna stiger och svarar genom att dämpa järnimporten. Ett protein kallat IRP2 känner av järn, delvis genom en hem‑beroende signal från mitokondrierna, och reglerar sedan produktionen av järntransportörer på cellytan. I ATP13A2‑bristfälliga celler misslyckades detta skydd. Transportörer som för in järn i cellen förblev höga trots att järn redan var förhöjt. Nivåerna av IRP2‑protein förändrades knappt, och att tillsätta extra järn utifrån utlöste inte dess normala nedbrytning. Teamet spårade detta fel tillbaka till mitokondrierna: skadade mitokondrier andades mindre effektivt, visade tecken på bristfällig kvalitetskontroll (mitofagi) och, avgörande, förlorade förmågan att bilda hem, den järninnehållande molekyl som hjälper IRP2 att känna av järn. Utan tillräckligt med hem mottog inte IRP2 budskapet om ”för mycket järn” och tillät fortsatt järnflöde in i cellen.
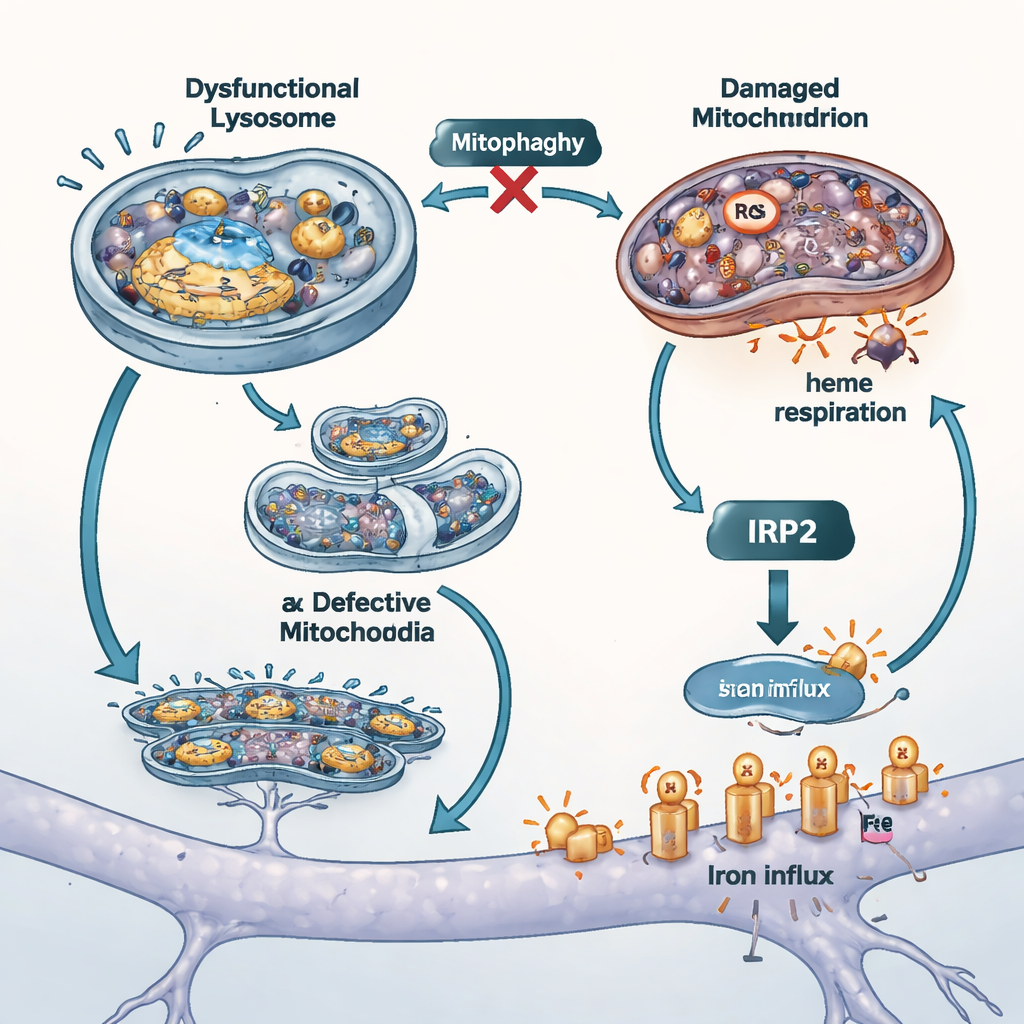
Blockera järnkranen och testa andra modeller
För att undersöka hur mycket denna okontrollerade järnentry bidrog till cellskada blockerade forskarna två huvudvägar för järnupptag. De använde en järnfri version av blodproteinet transferrin för att konkurrera om en importör, och ett litet läkemedel för att dämpa aktiviteten hos en annan transportör kallad DMT1. Båda ingreppen sänkte det totala och fria järnet inne i cellerna, minskade mitokondriell oxidativ stress och förbättrade överlevnaden, vilket tyder på att ytreceptorer för järn är viktiga förstärkare av skada när ATP13A2 går förlorat. Forskarna upprepade också nyckelexperiment i celler som saknade en annan Parkinsonsassocierad gen, PINK1, som är känd för att försämra mitofagi. Dessa celler visade samma kombination av järnansamling och försvagad hemproduktion, vilket stöder idén att mitokondriell kvalitetskontroll och järnbalans är tätt sammankopplade i olika former av sjukdomen.
Vad detta betyder för Parkinsons och framtida behandlingar
Enkelt uttryckt beskriver studien en ond cirkel. När ATP13A2 hämmas lyckas inte lysosomer rensa bort skadade komponenter, inklusive defekta mitokondrier. Dessa försvagade mitokondrier producerar då mindre energi och mindre hem, vilket försvagar cellens järn‑sensorik. Järn fortsätter strömma in via ytreceptorer, samlas i sårbara kompartiment och driver igång toxiska reaktioner som ytterligare skadar mitokondrier. Med tiden kan denna loop hjälpa till att förklara varför vissa neuroner dör vid Parkinsons och relaterade hjärnsjukdomar med järnansamling. Resultaten tyder på att framtida terapier kanske inte bara bör försöka avlägsna överskott av järn, utan också återställa korrekt lysosomfunktion, mitokondriell kvalitetskontroll och hemproduktion — angripa problemet vid dess källa snarare än att bara torka upp metallen i efterhand.
Citering: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
Nyckelord: Parkinsons sjukdom, hjärnans järn, mitokondrier, lysosomer, hem‑syntes