Clear Sky Science · sv
Undersökning av enzymets funktionella hotspot‑rester genom realtidsövervakning av den enzymatiska reaktionen med NMR och beräkningsmetoder
Varför detta är viktigt för framtida antivirala läkemedel
Favipiravir är en tablett som redan används mot influensa och testats för COVID‑19, men den bekämpar inte virus i den form vi sväljer. Våra egna celler måste först omvandla den till en aktiv molekyl som blockerar virus. Denna studie dissekerar, nästan atom för atom, hur ett mänskligt enzym utför ett avgörande aktiveringssteg och vilka små delar av enzymet som fungerar som ”hotspots” som styr hur snabbt och hur effektivt läkemedlet aktiveras. Att förstå dessa detaljer kan vägleda utformningen av nästa generation antivirala medel som både är mer potenta och mer förutsägbara i patienter.
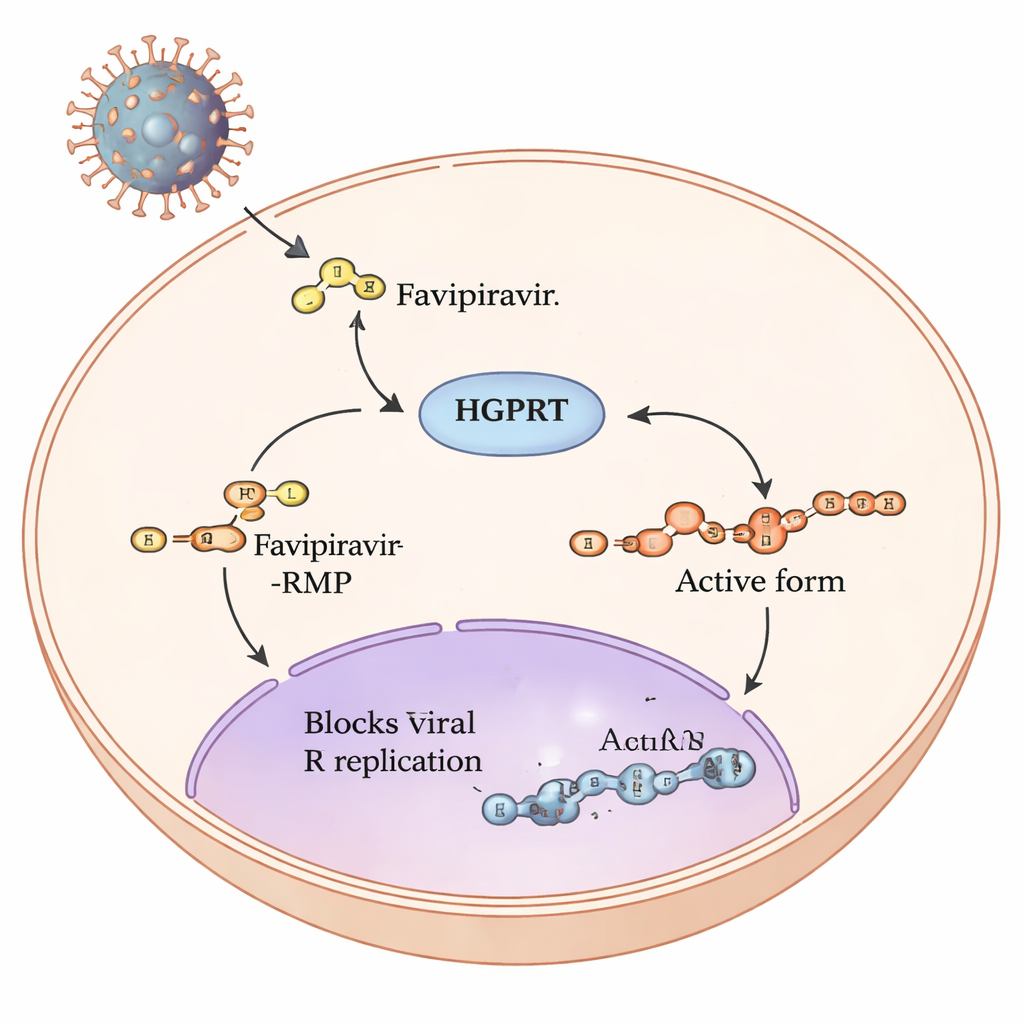
Prodrugens resa inne i våra celler
Favipiravir är en så kallad prodrug: när den väl kommer in i humana celler omvandlas den genom en serie kemiska steg till en form som kan störa kopieringsmaskineriet hos RNA‑virus som influensa och SARS‑CoV‑2. Det första och långsammaste steget i denna bana utförs av ett mänskligt enzym som kallas hypoxantin‑guanin fosforibosyltransferas, eller HGPRT. HGPRT lägger till en liten socker‑fosfatgrupp på favipiravir och bildar favipiravir‑RMP. Först efter detta steg kan andra enzymer bygga den fullt aktiva trifosfatformen som direkt stör virusets RNA‑polymeras. Eftersom detta första HGPRT‑drivna steg fungerar som en flaskhals för hur mycket aktivt läkemedel som bildas, syftade författarna till att fastställa vilka delar av HGPRT som är viktigast för att hantera favipiravir.
Att iaktta kemi i realtid med NMR
Unikt nog innehåller favipiravir en fluoratom som beter sig som en liten radiosändare i ett magnetfält. Forskargruppen utnyttjade detta genom att använda fluor‑19‑nukleär magnetisk resonans (NMR)‑spektroskopi för att i realtid följa hur mycket favipiravir respektive favipiravir‑RMP som fanns i ett provrör medan reaktionen fortskred. Eftersom endast läkemedlet bär fluor är NMR‑signalerna rena och lätta att följa. Genom att upprepade gånger spela in spektra över 12 timmar kunde forskarna följa försvinnandet av utgångsläkemedlet och ökningen av den modifierade produkten, och sedan extrahera standardkinetiska mått som hur snabbt reaktionen går och hur tätt enzymet verkar binda läkemedlet.
Finjustering av nyckelpositioner i enzymet
Tidigare röntgenbilder av HGPRT bundet till favipiravir‑RMP hade föreslagit ett fåtal aminosyror som omsluter läkemedlet i en ficka. Det nya arbetet testar tre av dessa positioner genom att göra precisa enstaka bokstavsändringar i proteinet och jämföra varje mutantenzym med det naturliga. En förändring, kallad T138A, gjorde oväntat enzymet ungefär fyra till sex gånger snabbare på att omvandla favipiravir, trots att den avlägsnade en kemisk grupp som tidigare troddes hjälpa till att hålla läkemedlet. En andra förändring, K140M, bromsade reaktionen måttligt och försvagade något den uppenbara bindningen. En tredje förändring, D193N, avskaffade helt enzymets förmåga att bilda favipiravir‑RMP, även om det förändrade proteinet fortfarande kunde produceras och binda produkten. Tillsammans visar dessa resultat att inte alla kontaktpunkter är likvärdiga: vissa fungerar som subtila hastighetsregulatorer, medan andra är nödvändiga strömbrytare.
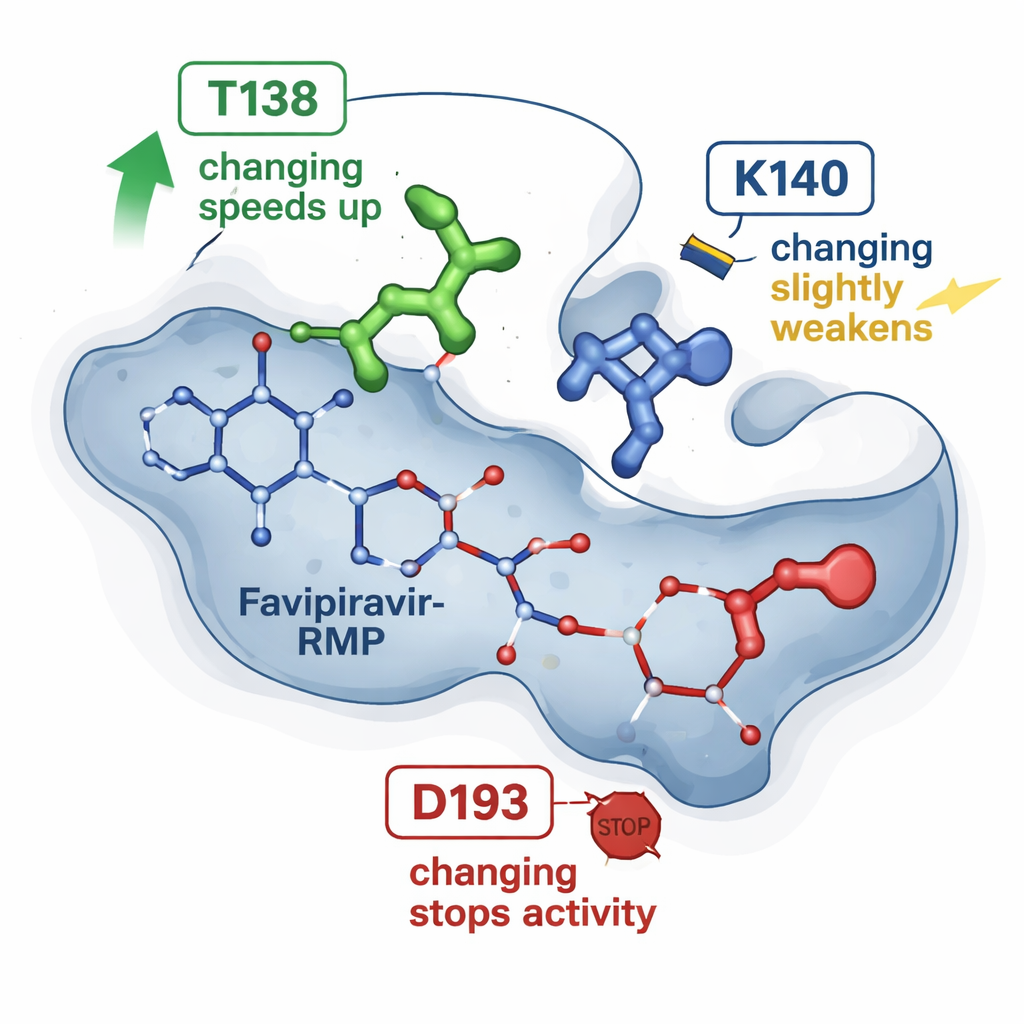
Att simulera rörliga delar i datorn
För att se bortom statiska strukturer vände sig forskarna till molekylära simuleringar. Utgående från den kända tredimensionella strukturen av HGPRT med favipiravir‑RMP använde de väletablerade beräkningsverktyg för att uppskatta hur starkt läkemedlet binder i varje mutant och för att köra många korta molekylärdynamiska simuleringar. Dessa simuleringar följer hur atomerna skakar och interagerar över tiotals nanosekunder. Beräkningarna överensstämde med trenderna från NMR: T138A‑varianten tenderade att hålla favipiravir‑RMP mer gynnsamt men visade också episoder där läkemedlet rörde sig mot en ”flykt”‑bana, styrd av en annan rest (K140) som kort förankrar fosfatgruppen före frisättning. Däremot grep D193N‑varianten fortfarande produkten, men misslyckades sannolikt i ett tidigare katalytiskt steg som kräver en magnesiumjon, vilket förklarar varför den förlorade aktivitet trots stabil bindning.
En färdplan för smartare antiviralsdesign
Genom att kombinera realtidsmässiga NMR‑mätningar med detaljerade datorbaserade modeller kartlägger denna studie de funktionella hotspots i HGPRT som avgör hur effektivt favipiravir aktiveras. För icke‑specialister är slutsatsen att våra egna enzymer starkt kan påverka hur mycket aktivt antiviralt läkemedel som byggs upp inne i celler, och att justeringar av antingen läkemedlets form eller enzymfickan kan förändra detta resultat dramatiskt. Författarnas hybrida strategi erbjuder en generell plan för att undersöka hur andra läkemedel interagerar med sina målproteiner, vilket potentiellt kan snabba på utvecklingen av nya antivirala föreningar som bättre matchas kroppens aktiveringsmaskineri.
Citering: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Nyckelord: favipiravir, aktivering av antivirala medel, HGPRT‑enzym, NMR‑spektroskopi, läkemedelsdesign