Clear Sky Science · sv
Ett lysinfritt REC-tagssystem för närhets-biotinyleringsapplikationer
Varför små taggar på proteiner spelar roll
Inuti varje cell arbetar sällan proteinerna ensamma — de samarbetar i föränderliga partnerskap som driver såväl hälsa som sjukdom. För att studera dessa partnerskap fäster forskare ofta små ”namnbrickor” på proteiner så att de kan spåras, isoleras ur en blandning eller visualiseras i mikroskop. En populär metod kallad närhets-biotinylering gör det möjligt att kartlägga vem som står nära vem inne i cellen, men den har en dold svaghet: många av dessa namntaggar blir kemiskt modifierade och försvinner just när de behövs som mest. Denna studie presenterar en ny typ av tagg, kallad REC-taggen, utformad för att förbli synlig under dessa krävande förhållanden.
En kemisk markör för proteiners grannar
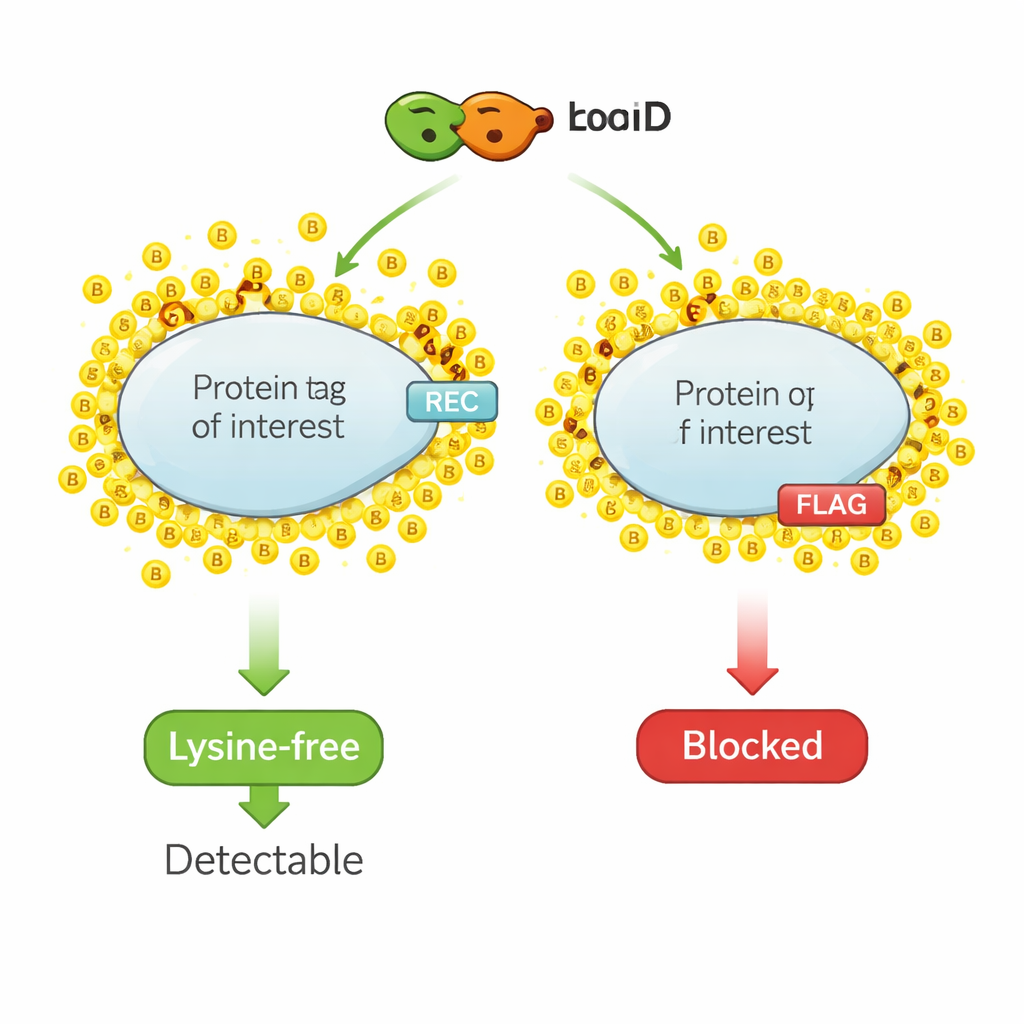
Närhets-biotinylering fungerar som en molekylär markeringspenna. Ett konstruerat enzym, exempelvis TurboID, är fuserat till ett protein av intresse. När biotin — en liten vitamin — tillsätts fäster TurboID snabbt biotinmolekyler på närliggande proteiner. Forskarna fiskar sedan upp alla biotinmarkerade proteiner och identifierar dem, vilket ger en ögonblicksbild av proteinets lokala grannskap. Men samma kemi som märker intilliggande proteiner riktar sig också mot de små epitoptaggar som ofta används för detektion, eftersom dessa taggar vanligen innehåller lysin, en aminosyra som är huvudmål för biotin. När lysiner i taggen täcks av biotin kan antikroppar inte längre känna igen taggen, och signalen i standardmetoder sjunker eller försvinner.
Att designa en tagg som vägrar modifiering
För att lösa detta gav sig författarna i kast med att skapa en ny tagg helt fri från lysin. De utgick från ett fragment av ett malaria-parasitprotein kallat PfRipr5, som har liten likhet med mänskliga proteiner, vilket minskar risken för oönskade korsreaktioner. Genom en mikrochipbaserad screeningsmetod i kaniner genererade de 22 monoklonala antikroppar mot PfRipr5 och identifierade en, döpt till klon nr. 6, med särskilt stark och specifik bindning. Genom systematisk trimning och mutation av PfRipr5-fragmentet avgränsade de antikroppens mål till en 11-aminosyrasträcka. Denna minimala sekvens innehöll bara ett lysin, som de ersatte med en liknande aminosyra, arginin. Anmärkningsvärt nog bibehöll antikroppen samma goda bindning. Denna optimerade, lysinfria sekvens namngavs REC-taggen, och den matchande antikroppen REC-antikropp.
Att pröva REC-taggen i praktiken
Forskargruppen testade sedan om REC-taggen kunde ersätta vanliga taggar som FLAG i vanliga laboratorietekniker. När den fuserades till fluorescerande eller signalproteiner och uttrycktes i cellfria system och i däggdjursceller detekterades REC-märkta proteiner lätt med immunoblotting, en högkänslig ljusbaserad plattformsanalys kallad AlphaScreen och immunfärgning i celler. Detektionsstyrkan var liknande den för FLAG-taggen och för ett annat lysinfritt tagsystem (AGIA), och REC-antikroppen visade mycket lite bakgrundssignal i en rad mänskliga och apa-cellinjer. Viktigt är att taggen fungerade oavsett om den placerades i början eller slutet av ett protein, och på proteiner lokaliserade i olika cellulära områden, inklusive kärnan, mitokondrier, endoplasmatiska retiklet och cellmembranet.
Att förbli synlig under intensiv märkning
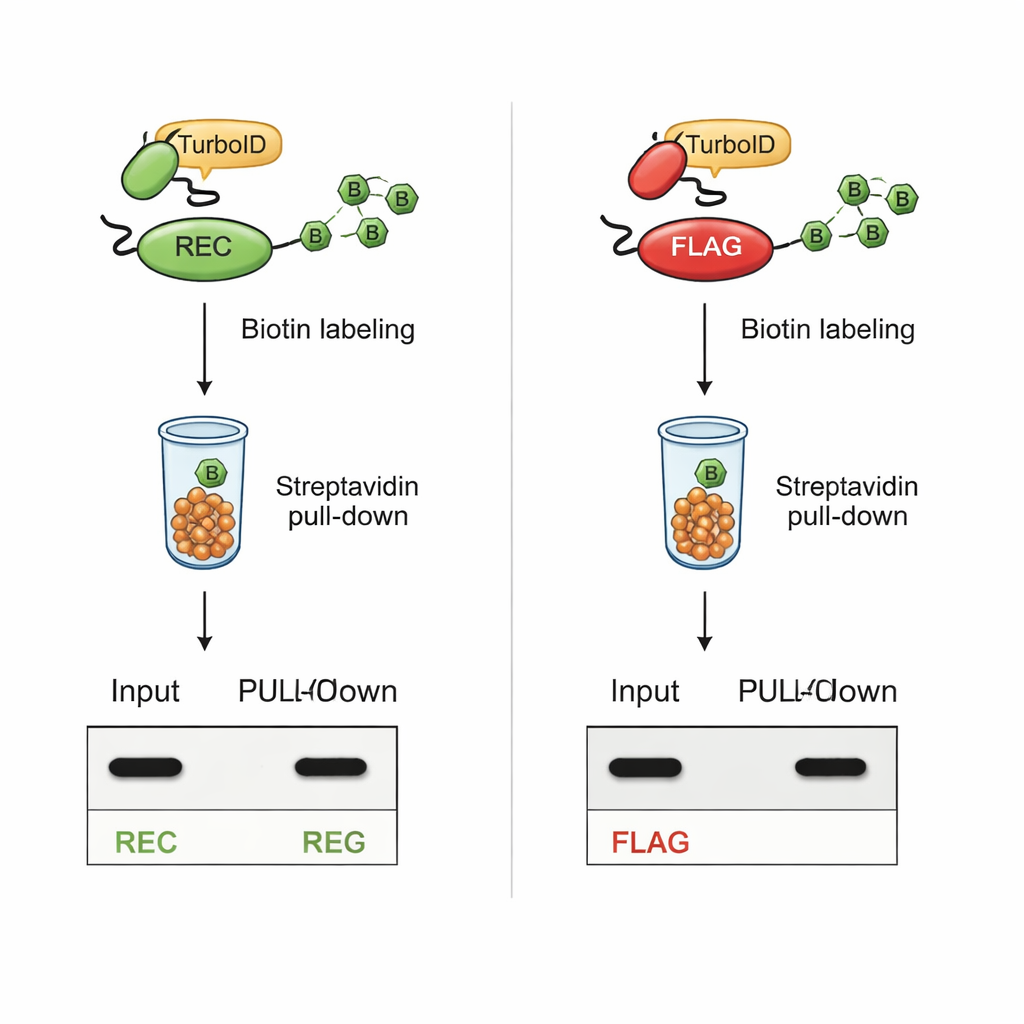
Det avgörande testet var om REC skulle förbli detekterbar efter TurboID-baserad biotinylation. I celler där TurboID var fuserat till kända interaktionspartners förblev proteiner som bar REC-taggen tydligt synliga både i helcellsextrakt och i den renade, biotinmärkta fraktionen. Däremot förlorade proteiner med den klassiska FLAG-taggen sin FLAG-signal när TurboID var aktivt, även om proteinerna i sig fortfarande var närvarande. Ytterligare experiment med syntetiska peptider visade att TurboID direkt biotinylierar lysinerna i FLAG-sekvensen och fysiskt blockerar antikroppstillgång. REC-taggen, som helt saknar lysin, påverkades inte av TurboID och förblev lätt att detektera.
Vad detta betyder för framtida experiment
För forskare som utforskar protein-nätverk inuti levande celler erbjuder REC-taggen ett praktiskt nytt verktyg: den beter sig som välkända taggar i vardagliga analyser men fortsätter fungera även när kraftfulla närhetsmärkningsenzym är aktiva. Det innebär att forskare mer tillförlitligt kan bekräfta att deras taggade proteiner är närvarande och korrekt fångade, och kan studera andra lysinbaserade modifieringar — såsom ubiquitinering och acetylering — utan att taggen själv stör. Kort sagt är REC en liten designändring med stor påverkan som hjälper till att göra komplexa protein-kartläggningsexperiment tydligare och mer trovärdiga.
Citering: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Nyckelord: proteinmärkning, närhets-biotinylering, TurboID, proteininteraktioner, epitop-taggar