Clear Sky Science · sv
EEG-baserad klassificering av Alzheimers sjukdom och frontotemporal demens med hjälp av funktionell konnektivitet
Varför hjärnvågsmönster spelar roll
Demens drabbar miljontals familjer, men även läkare kan ha svårt att skilja olika former åt. Alzheimers sjukdom och frontotemporal demens kan ofta se lika ut i kliniken, samtidigt som de kräver olika vårdplaner och forskningsstudier. Denna studie ställer en enkel men kraftfull fråga: kan vi använda ett snabbt, icke-invasivt hjärntest — elektroencefalografi, eller EEG — för att läsa av hjärnans kommunikationsmönster i vila och hjälpa till att skilja dessa tillstånd från normalt åldrande, och från varandra?
Att titta på hjärnsamtal, inte bara hjärnaktivitet
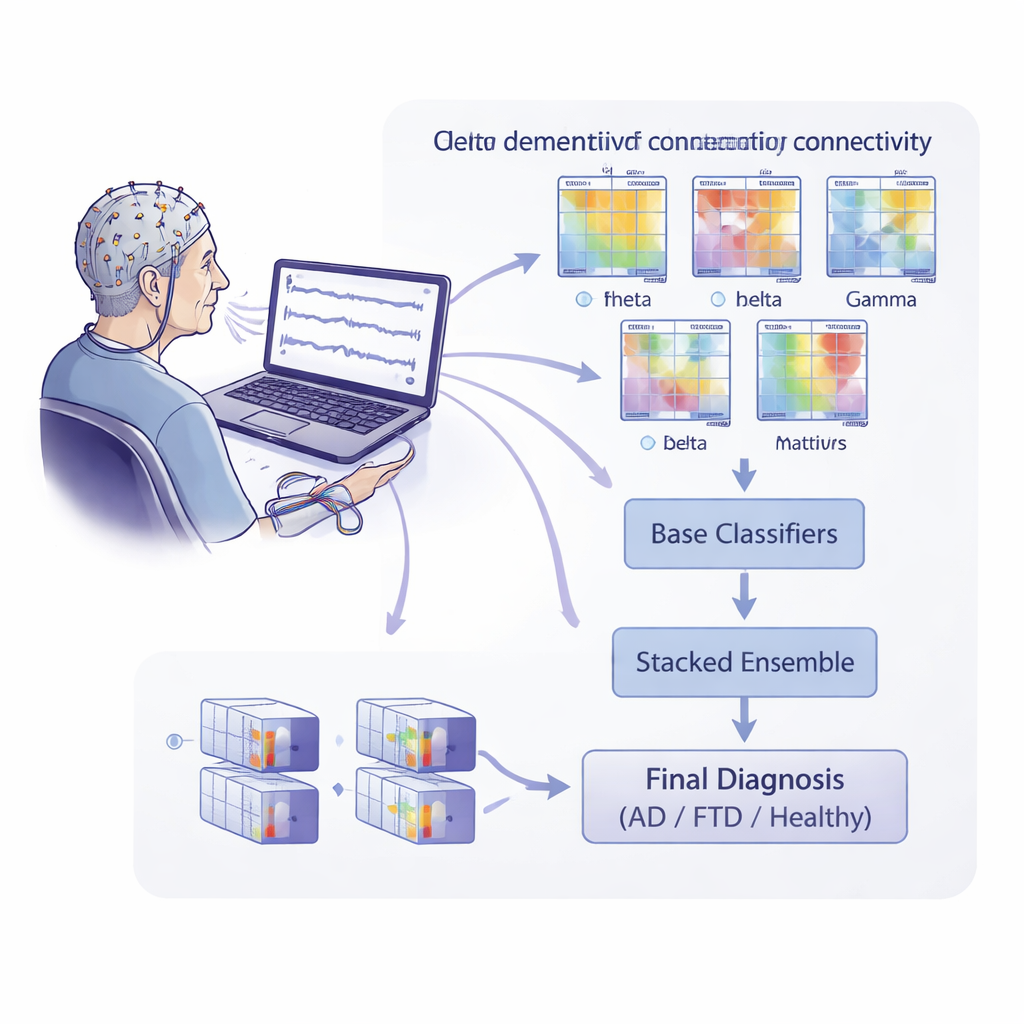
EEG mäter vanligtvis hur starka hjärnvågorna är i olika frekvensband, såsom långsamma delta‑vågor eller snabbare alfa‑vågor. Här gick forskarna ett steg längre och undersökte hur olika delar av hjärnan "pratar" med varandra. De använde inspelningar från 88 personer: 36 med Alzheimers sjukdom, 23 med frontotemporal demens och 29 friska äldre vuxna. Med 19 skalpelektroder spelade de in hjärnaktivitet i vila med slutna ögon och delade varje inspelning i många korta tidssegment. För varje segment och för flera frekvensband beräknade de en serie konnektivitetsmått — matematiska beskrivningar av hur tätt olika EEG‑kanaler är kopplade i tid, frekvens och fas.
Att lära algoritmer känna igen demensmönster
För att omvandla dessa konnektivitetskartor till förutsägelser tränade teamet ett stort antal grundläggande maskininlärningsmodeller, där varje modell fokuserade på en kombination av frekvensband och konnektivitetsmått. Dessa basmodeller använde specialiserade matematiska verktyg för att jämföra konnektivitetsmönster mellan individer. Utdata från alla basmodeller matades sedan in i en högre nivå, en så kallad "stackad" modell, som försökte lära sig vilka kombinationer av funktioner som var mest informativa. Viktigt är att forskarna utvärderade prestanda på den nivå som betyder något kliniskt: en enskild diagnos per person. De använde en strikt testuppläggning som alltid höll en persons data helt separata från träningsdata, vilket minskar risken för överoptimistiska resultat på grund av subtil dataläckage.
Vad hjärnvågorna avslöjade — och vad de inte gjorde
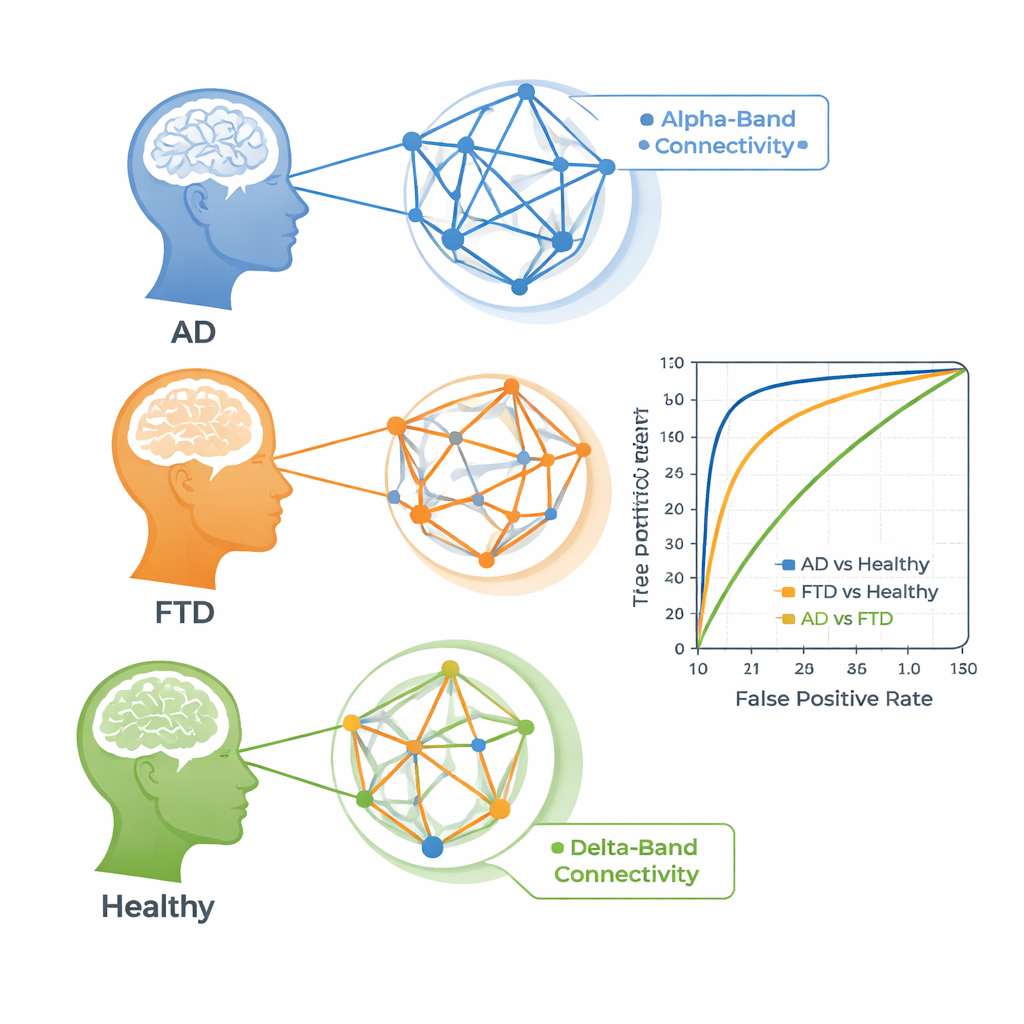
Konnektivitetsmönstren hjälpte till att skilja personer med demens från friska försökspersoner. För Alzheimers jämfört med friska kontroller nådde vissa enskilda konnektivitetsfunktioner area-under-curve‑värden över 85 %, vilket innebär att de var ganska bra på att rangordna vem som hade sjukdomen. Detsamma gällde, om än något svagare, för frontotemporal demens jämfört med normalt åldrande. De mest informativa signalerna i båda fallen kom från alfa‑bandet, en rytm kopplad till avslappnat vakenhetstillstånd som ofta störs vid demens. Att skilja Alzheimers från frontotemporal demens var däremot mycket svårare. De bästa måtten för denna uppgift kom från det långsamma delta‑bandet och nådde endast måttlig träffsäkerhet, vilket antyder att de två sjukdomarna delar många av samma storskaliga nätverksstörningar i dessa EEG‑inspelningar.
När större komplexitet inte ger bättre svar
En förhoppning med ensemblemetoder är att kombinera många svaga prediktorer kan ge en starkare, mer pålitlig modell. I denna studie överträffade emellertid inte den stackade ensemblemodellen de bästa enskilda konnektivitetsfunktionerna. Faktum är att de bästa fristående modellerna ofta var något bättre. Ytterligare analyser visade att många basmodeller gjorde liknande typer av fel, så ensemblen hade begränsad verkligt ny information att utnyttja. Författarna testade också olika sätt att mäta avstånd mellan konnektivitetsmatriser, inklusive avancerade "manifold"‑geometrimetoder, men fann liten fördel jämfört med enklare tillvägagångssätt för detta diagnostiska problem mellan individer.
Vad detta betyder för patienter och kliniker
För personer som upplever minnes‑ eller beteendeförändringar erbjuder dessa resultat försiktig optimism. Vila‑EEG, ett snabbt, billigt och allmänt tillgängligt test, fångar meningsfulla signaturer av demens i hur hjärnregioner kopplar till varandra. Samtidigt understryker arbetet att smart matematik inte ensam kan fullt ut reda ut nära besläktade sjukdomar när data är begränsade och hjärnförändringarna överlappar. Författarna menar att noggrant utvalda, tolkbara EEG‑funktioner, utvärderade med strikt testning på subjekt‑nivå, kan vara mer pålitliga än mycket komplexa modeller. Framtida framsteg, föreslår de, kommer sannolikt från att kombinera EEG‑konnektivitet med andra biomarkörer såsom hjärnavbildning, blodprover och kognitiva profiler, för att bygga mer precisa och tillförlitliga verktyg för att diagnostisera olika former av demens.
Citering: Mlinarič, T., Van Den Kerchove, A., Barinaga, Z.I. et al. EEG-based classification of alzheimer’s disease and frontotemporal dementia using functional connectivity. Sci Rep 16, 4903 (2026). https://doi.org/10.1038/s41598-026-35316-9
Nyckelord: EEG, funktionell konnektivitet, Alzheimers sjukdom, frontotemporal demens, maskininlärning