Clear Sky Science · sv
Interaktion mellan ELMO1 DNA‑metylering och Med31 främjar H. pylori‑inducerad gastrisk cancer EMT och intestinal metaplasi via M2‑polarisering
Varför magsyrabakterier spelar roll för cancer‑risk
De flesta av oss bär på miljarder bakterier i matsmältningskanalen, och en av dem — Helicobacter pylori — kan tyst leva i magsäcken i årtionden. För vissa personer är infektionen ofarlig, men för andra blir den första steget på vägen mot magcancer, en av världens dödligaste cancerformer. Denna studie undersöker hur en liten kemisk förändring i DNA i magsäcksceller bidrar till att omvandla en långvarig infektion till precancerös skada och slutligen till en miljö där cancer kan växa.
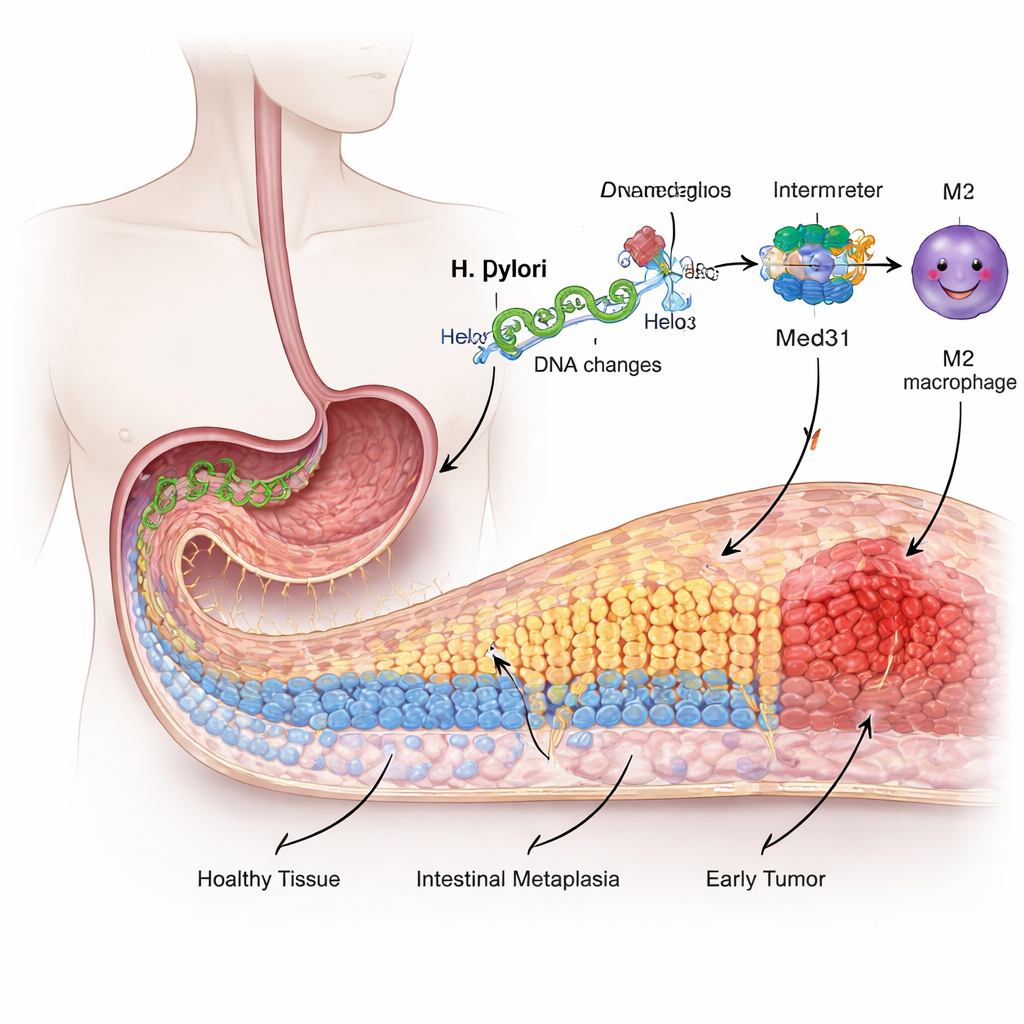
Från vänlig slemhinna till riskfylld omgestaltning
Magsäckens inre yta är täckt av specialiserade celler som är anpassade för att hantera stark syra, inte födognedbrytning som i tarmen. Under år av irritation och inflammation från H. pylori börjar några av dessa magsäcksceller ”göra om” sig och anta drag av tarmceller i en process som kallas intestinal metaplasi. Denna förändring betraktas som ett precanceröst stadium. Forskarna använde en human gastrisk cellinje för att efterlikna infektion och fann att exponering för H. pylori fick dessa celler att dela sig snabbare, röra sig lättare och aktivera tarmtypiska markörer — alla tecken på att slemhinnan förlorade sin normala identitet.
Små kemiska etiketter med stora konsekvenser
Vårt DNA kan märkas med små kemiska grupper kallade metylgrupper som fungerar som av‑ och på‑brytare för gener utan att förändra den genetiska koden. Teamet fokuserade på en gen kallad ELMO1, redan känd för att vara involverad i cellrörelse och cancerspridning. De visade att H. pylori‑infektion ökade metyleringen av ELMO1‑genen och, något motintuitivt, ökade dess aktivitet och proteinnivåer i gastriska celler. När de använde ett läkemedel som avlägsnar dessa metylmärken förlorade cellerna många av de infektiondrivna förändringarna: de delade sig mindre, rörde sig mindre och visade färre tecken på intestinal metaplasi. Detta pekade på ELMO1‑metylering som en avgörande brytare som bakterien slår om.
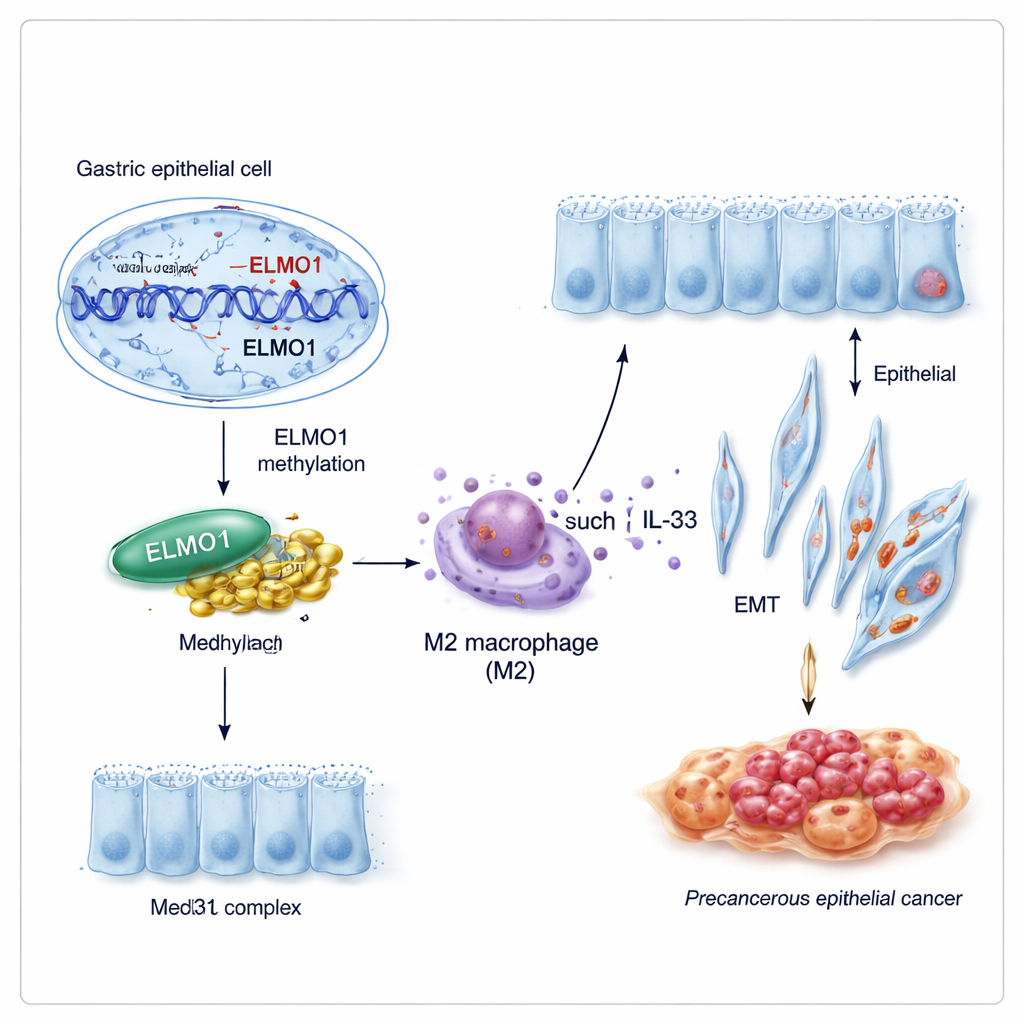
En ny samverkan som omlägger cellbeteende
Gener agerar sällan ensamma. Forskarna upptäckte att metylerat ELMO1 gynnade ett partnerskap med ett annat protein, Med31, som är en del av en stor ”kontrollpanel” som hjälper till att bestämma vilka gener en cell slår på. Under förhållanden som främjar DNA‑metylering steg ELMO1‑nivåerna, Med31 ökade, och de två band fysiskt till varandra, medan en tidigare känd partner till ELMO1, DOCK10, fick stå åt sidan. Detta nya ELMO1–Med31‑team verkar omprogrammera genuttrycket i magsäcksceller på sätt som uppmuntrar dem att anta intestinala drag och att bete sig mer aggressivt.
Hur immunceller pressas att gynna tumören
Cancer utvecklas inte i isolation; den växer i ett komplext grannskap av immunceller och stödjeceller. Studien visar att infekterade gastriska celler med metylerat ELMO1 frisätter högre nivåer av IL‑33, en signal som knuffar närliggande immunceller kallade makrofager mot ett tumörvänligt ”M2”‑tillstånd. Med hjälp av ett samsystem i odling fann författarna att makrofager exponerade för dessa signaler starkt lutade åt M2‑typen och i sin tur utsöndrade faktorer som fick nya gastriska celler att bli mer rörliga, mer invasiva och mer lika tarmceller. Markörer för epitelial‑mesenkymal övergång — när stationära slemhinnesceller omvandlas till vandrare med invasiv kapacitet — ökade markant under påverkan av dessa M2‑makrofager.
Vad detta innebär för att förebygga magcancer
Sammantaget skisserar arbetet en händelsekedja: H. pylori‑infektion ändrar DNA‑metyleringen av ELMO1, detta modifierade ELMO1 slår sig ihop med Med31, infekterade celler sänder ut signaler som omvandlar närliggande immunceller till M2‑hjälpare, och dessa hjälpare driver både intestinal metaplasi och ett mer invasivt celltillstånd. För icke‑specialister är kärniden att en vanlig magsäcksbakterie kan omforma både magslemhinnan och det lokala immunsvaret genom reversibla kemiska märken på DNA. Att förstå denna bana kan öppna vägar till nya blodbaserade tester som upptäcker riskfyllda metyleringsmönster tidigt, samt läkemedel som stör ELMO1–Med31–M2‑axeln innan en kronisk infektion utvecklas till magcancer.
Citering: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Nyckelord: magcancer, Helicobacter pylori, DNA‑metylering, intestinal metaplasi, tumörmikromiljö