Clear Sky Science · sv
Djupinlärningsbaserad automatisk segmentering och klassificering för cervixcancerdetektion med förbättrad U‑Net och ensemblemetoder
Varför Pap‑test fortfarande behöver en digital hjälpande hand
Cervixcancer är en av de få cancerformer som är starkt förebyggbara om den upptäcks i tid, ändå dör många kvinnor eftersom farliga cellförändringar missas eller upptäcks för sent. Det välkända Pap‑testet räddar redan liv, men att läsa tusentals cellbilder för hand är långsamt, tröttande arbete och även experter kan vara oense. Denna artikel undersöker hur modern artificiell intelligens kan fungera som en outtröttlig assistent, automatiskt hitta och sortera cervixceller på Pap‑smear‑bilder för att hjälpa läkare upptäcka tidiga varningstecken snabbare och mer pålitligt.
Lära datorer att se problematiska celler
Forskarna satte upp målet att bygga ett datorsystem som kan utföra två nyckeluppgifter: för det första identifiera varje cervixcell mot bakgrunden i en Pap‑smear‑bild, och för det andra avgöra om cellen ser normal ut eller uppvisar tecken kopplade till cancer. För att göra detta använde de djupinlärning, en form av AI som lär sig mönster direkt från stora mängder exempelbilder istället för från handskrivna regler. Systemet fokuserar på hela cellen—både den mörka kärnan (nukleus) och det omgivande materialet (cytoplasma)—eftersom förändringar i storlek, form och textur över hela cellen kan signalera sjukdom.
Ett smartare sätt att rita upp cellerna
I centrum av systemet finns en förbättrad version av en populär modell för medicinsk bildbehandling kallad U‑Net, som är särskilt bra på att rita precisa konturer runt objekt i bilder. Författarna modifierade U‑Net så att den kan betrakta bilddetaljer i flera skalor samtidigt och vara stabil även när den tränas på små datapartier, en vanlig begränsning inom medicin. Detta uppgraderade nätverk lär sig att måla en enkel mask över varje bild: vitt där en cell finns, svart för bakgrunden. Genom att isolera endast cellområden kan senare steg i kedjan fokusera på det som är viktigast istället för att distraheras av färgningar, skräp eller tom yta.
Skapa fler träningsexempel ur tomma intet
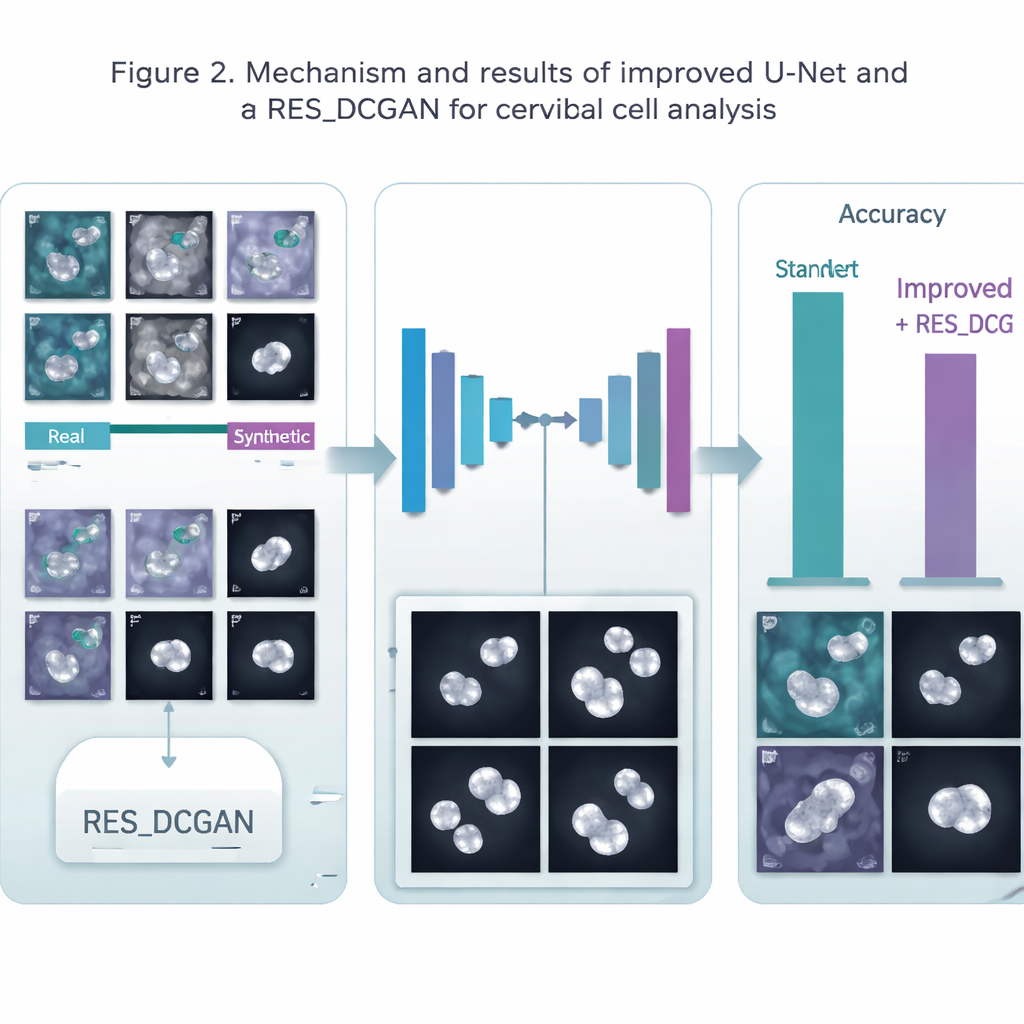
En stor utmaning inom medicin är att högkvalitativa, annoterade bilder är sällsynta och dyra att ta fram. För att tackla detta använde teamet en generativ modell kallad RES_DCGAN, som lär sig att skapa realistiska syntetiska Pap‑smear‑bilder baserat på de verkliga. Dessa extra ”påhittade men övertygande” bilder blandas in i träningsprocessen, både före cellsegmenteringssteget och efteråt i klassificeringssteget. Genom att exponeras för många fler variationer av celler—inklusive sällsynta och subtila mönster—blir AI:n mer robust och mindre benägen att överanpassa sig till ett litet urval av patienter eller avbildningsförhållanden.
Från konturer till tidiga varningar
När cellerna är segmenterade tar en andra grupp av djupinlärningsmodeller över för att klassificera varje cell som normal eller tillhöra olika abnorma kategorier. Författarna använde en kraftfull bildigenkänningsmodell kallad ResNet50V2 och kombinerade den med flera andra välkända nätverk i ett ”ensemble”, där flera modeller röstar tillsammans om det slutliga beslutet. De testade sex olika bearbetningskedjor på tre dataset från Polen (Pomeranian), Danmark (Herlev) och Grekland (SIPaKMeD), som täcker både enkla normal‑mot‑abnorma fall och mer detaljerade flerkategoriproblem. I dessa tester förbättrade segmentering av cellerna konsekvent klassificeringsnoggrannheten, och tillförseln av syntetiska bilder sköt i allmänhet prestationen något högre, särskilt för cellkontureringen.
Hur bra presterade den digitala assistenten?
Systemet uppnådde mycket höga poäng. För cellkonturering nådde noggrannheten upp till cirka 99,5% på ett dataset och omkring 98% på ett annat, vilket klart överträffade en standard‑U‑Net. För att avgöra celltyp korrekt etiketterade ensembles av modeller runt 95–96% av cellerna i de mer komplexa uppgifterna och upp till 99% i enklare ja/nej‑bedömningar av cancerisk risk. Dessa resultat matchar eller överträffar många tidigare studier, samtidigt som de visar att en enhetlig pipeline kan fungera över olika laboratorier och datakällor. Vinsterna var mer måttliga på ett särskilt varierat dataset, vilket understryker att verklig mångfald i data fortfarande utgör utmaningar.
Vad detta betyder för patienter och läkare
I praktiska termer visar detta arbete att en AI‑assistent kan lära sig att omsorgsfullt spåra cervixceller och sortera dem i riskgrupper med anmärkningsvärd konsekvens. Den ersätter inte patologen, men den kan förscreenas preparat, markera misstänkta celler och minska risken att tidiga tecken förbises i stressade kliniker eller i regioner med få specialister. Med vidare testning på större, mer komplexa prover och maskar validerade av experter kan system som detta bidra till att göra pålitlig cervixcancerscreening tillgänglig för fler kvinnor världen över, upptäcka farliga förändringar tidigare och öka chanserna för framgångsrik behandling.
Citering: Wubineh, B.Z., Rusiecki, A. & Halawa, K. Deep learning-based automatic segmentation and classification for cervical cancer detection using an improved U-Net and ensemble methods. Sci Rep 16, 5184 (2026). https://doi.org/10.1038/s41598-026-35299-7
Nyckelord: cervixcancerscreening, Pap‑provbilder, djupinlärning, medicinsk bildsegmentering, datorstödd diagnostik