Clear Sky Science · sv
Bedömning av den biokemiska grunden för resistens mot systemisk amyloidos
När små proteinförändringar blockerar en dödlig ansamling
Många kroniska inflammatoriska sjukdomar, från reumatoid artrit till tuberkulos, kan utlösa en sällsynt men ofta dödlig komplikation som kallas systemisk AA-amyloidos. Vid detta tillstånd byggs ett normalt blodprotein upp som styva fibrer som täpper igen organ. Denna studie ställer en oväntat hoppfull fråga: kan små, naturliga förändringar i det proteinet göra vissa djur i stort sett immuna mot sjukdomen – och i så fall hur?
Det dolda hotet från proteinansamlingar
AA-amyloidos börjar med en inflammatorisk varningssignal i blodet kallad serum amyloid A (SAA). Under svår eller långvarig inflammation kan SAA-nivåerna stiga tusentals gånger över det normala. Hos vissa människor och djur veckas en del av detta protein fel och staplas till långa fibrer, kända som amyloida fibriller, som sprider sig genom organ som mjälten och njurarna. Med tiden försämrar dessa fibrer organfunktionen. Men inte alla individer med höga SAA-nivåer utvecklar amyloidos, och vissa musstammar förblir förvånansvärt motståndskraftiga även när de pressas mot sjukdom i laboratorium. Att förstå varför kan peka på nya strategier för att förebygga amyloidansamling hos människor.
Motståndskraftiga möss och deras speciella proteinvarianter
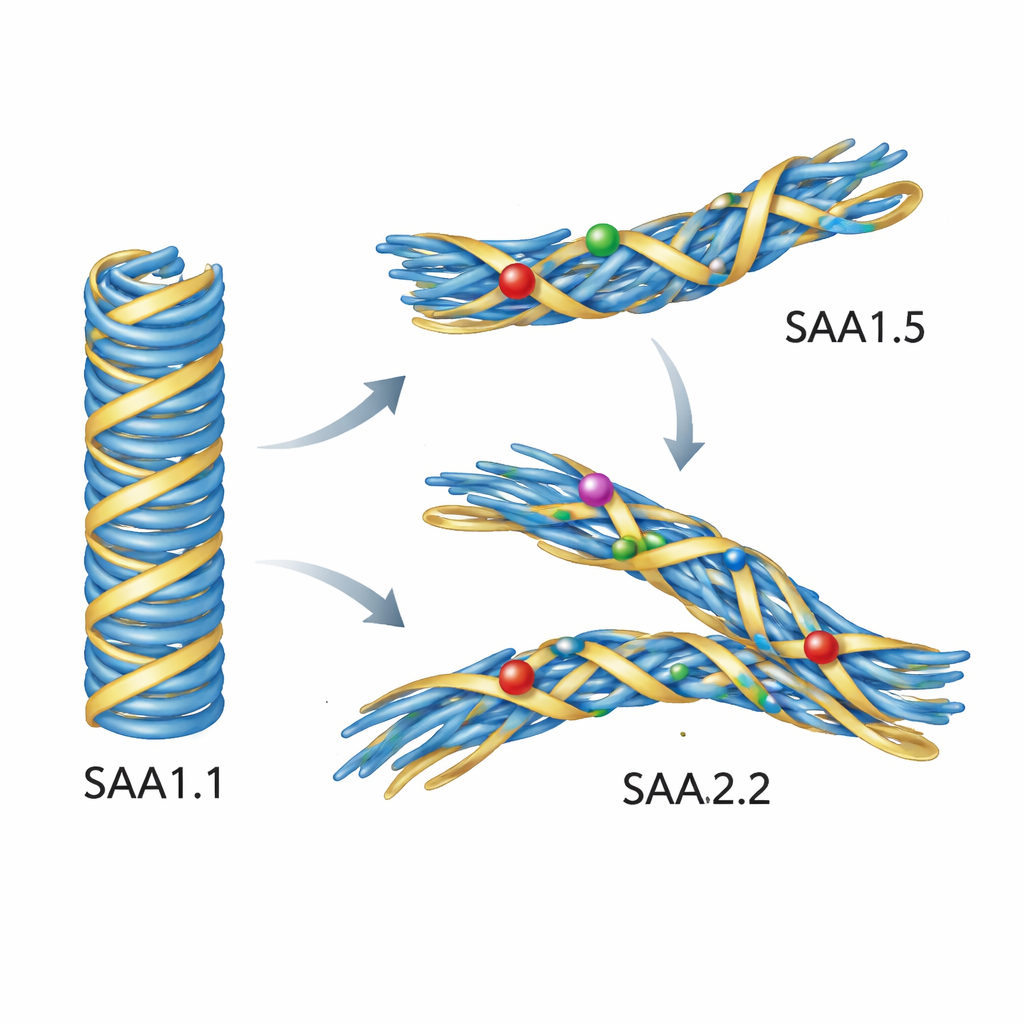
I möss uppstår de flesta AA-amyloida fibriller från en variant av SAA kallad SAA1.1, som är starkt kopplad till sjukdom. Men vissa musstammar producerar främst något förändrade varianter, benämnda SAA1.5 och SAA2.2, och dessa stammar utvecklar sällan systemisk AA-amyloidos. Proteinerna skiljer sig bara i ett fåtal byggstenar (aminosyror), men dessa förändringar klustrar sig i ett tätt packat område som bildar fibrillernas inre kärna. Forskarna föreslog att dessa små skillnader inte hindrar proteinerna från att klumpa sig helt, utan istället förhindrar dem från att anta just den specifika fibrilformen som är skadlig.
Sätta proteinerna på prov i laboratoriet
För att undersöka denna idé framställde teamet alla tre mus-SAA-varianterna i bakterier och följde hur de betedde sig i provrörsexperiment. De övervakade fibrillbildning med ett fluorescerande färgämne som lyser upp när amyloid bildas, och verifierade strukturer med elektronmikroskop. Den sjukdomsassocierade SAA1.1 bildade lätt långa, raka fibriller. SAA2.2 kunde också bilda fibriller, men de var tjockare, mer snurrade och strukturellt mer varierade, och de gav inte samma starka färgsignal. SAA1.5, däremot, misslyckades med att bilda fibriller under de testade förhållandena. När forskarna tillsatte små prover av verkliga sjukdomsfibriller tagna från sjuka musmjöltar som ”frön”, växte SAA1.1 snabbt nya fibriller som nära kopierade den ursprungliga strukturen, precis som ett prion. Slående nog växte inte SAA1.5 och SAA2.2 alls på dessa frön; de ex vivo-fibrillerna kunde inte rekrytera dem till den patogena formen.
Simuleringar visar varför mutanta proteiner vägrar den skadliga formen
Experimenten kunde inte ensamma visa exakt vad som går fel på atomnivå, så författarna vände sig till detaljerade datorbaserade simuleringar. De började från en högupplöst struktur av en patogen mouse AA-fibrill byggd av SAA1.1 och ersatte sedan beräkningsmässigt sekvenserna med SAA1.5 och SAA2.2. När de simulerade dessa fibriller i vatten vid kroppstemperatur förblev SAA1.1-baserade modellen anmärkningsvärt stabil. I kontrast skiftade och deformeras fibriller byggda av SAA1.5 eller SAA2.2. En nyckelloop i kärnan rörde sig utåt och lossnade från kontakten med proteinets N-terminala segment, och flera sidokedjor vred sig till nya orienteringar. Dessa subtila omarrangemang störde den täta packning som definierar den sjukdomsassocierade vikningen. Med andra ord, variantsekvenserna hade inget emot att bilda fibriller i allmänhet – men de kunde inte bekvämt passa in i ritningen för den patogena AA-fibrillen.
Hur naturens design pekar mot framtida terapier
Tillsammans visar arbetet att ”amyloidresistenta” musstammar inte skyddas för att deras SAA inte kan aggregera alls. Snarare är deras SAA-versioner strukturellt oförenliga med just den fibrilform som orsakar systemisk AA-amyloidos. Proteinerna kan fortfarande klumpa ihop sig, men de gör det i alternativa, till synes ofarliga former. Liknande skyddande mutationer är kända i andra proteinfelveckningssjukdomar, inklusive vissa prion- och Alzheimersfall. Detta antyder en bredare princip: att justera ett sjukdomsbenäget protein så att det inte kan anta sin toxiska arkitektur – samtidigt som det fortfarande fungerar normalt – kan vara nog för att förebygga sjukdom. På sikt skulle terapier inspirerade av dessa naturliga ”resistenta” varianter, eller av korta fragment härledda från dem, kunna hjälpa till att styra proteiner bort från skadliga veckningar och mot ofarliga.
Citering: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Nyckelord: AA-amyloidos, serumt Amyloid A, proteinfelveckning, amyloidresistens, musmodeller