Clear Sky Science · sv
Modellering och experimentell verifiering av utfällning av polykaprolakton-nanopartiklar
Varför små plastkulor spelar roll för medicinen
Föreställ dig att packa ett potent läkemedel inuti en prick så liten att den kan glida genom blodkärl och leverera sitt innehåll precis där det behövs. Sådana partiklar, kallade polymernanopartiklar, ligger i centrum för många nya behandlingar och avbildningsmetoder. Men att tillverka dem med rätt och reproducerbar storlek är förvånansvärt svårt. Denna studie visar hur en enkel fysikbaserad datormodell kan förutsäga och justera storleken på en mycket användbar biologiskt nedbrytbar nanopartikel, vilket potentiellt kan kapa år av försök‑och‑fel i utvecklingen av nya nanomediciner.
Från köksblandning till laboratorieprecision
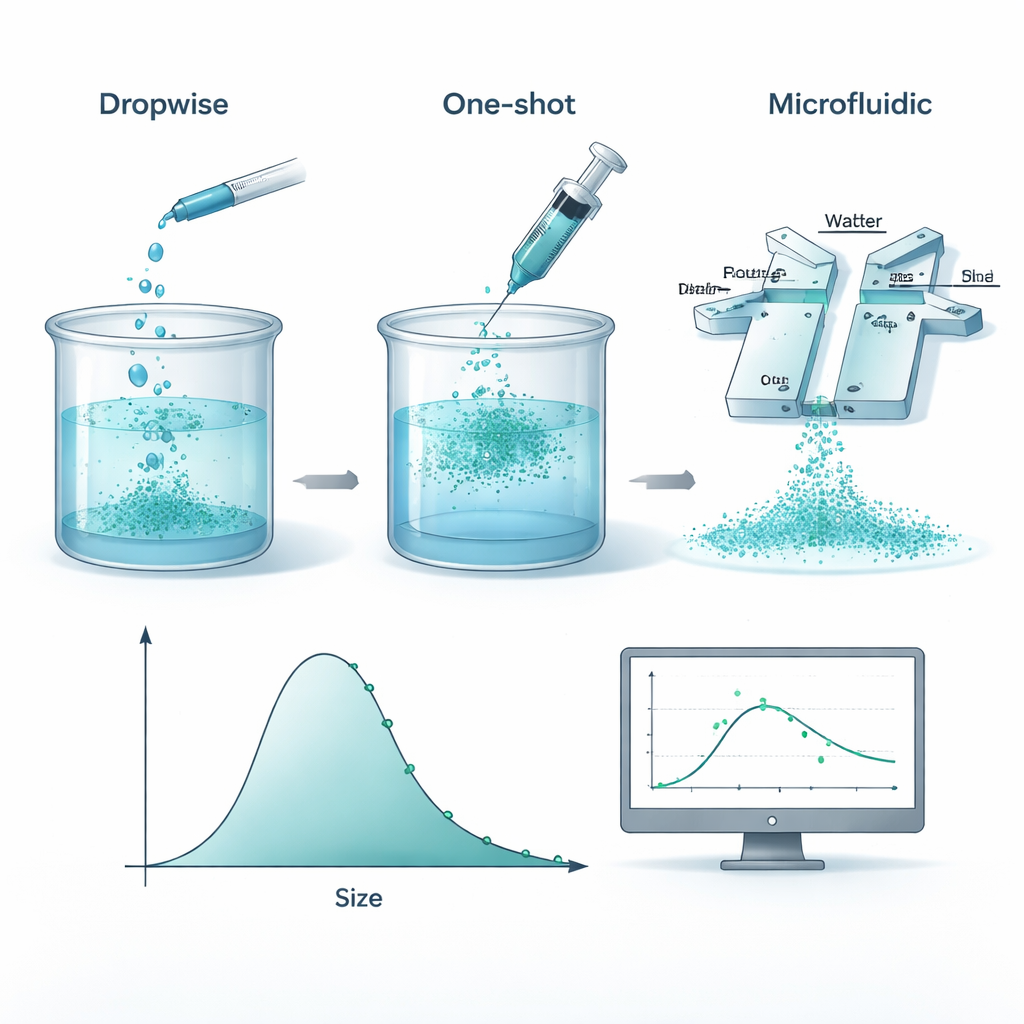
För att skapa dessa nanopartiklar löser forskarna upp en biologiskt nedbrytbar plast kallad polykaprolakton (PCL) i ett organiskt lösningsmedel och blandar det sedan med vatten så att polymeren ”fäller ut” ur lösningen och bildar små kulor. Gruppen jämförde tre praktiska sätt att göra detta: att tillsätta polymerslösningen droppvis, att hälla i allt på en gång, och att pressa båda vätskorna genom en liten mikrofluidisk chip där de möts i smala kanaler. Under noggrant kontrollerade förhållanden gav alla tre metoderna partiklar med mycket liknande genomsnittsstorlekar och spridning. Det betyder att, åtminstone inom de undersökta områdena, spelar ingredienserna — mängden polymer och stabilisator — större roll än exakt vilken blandningsanordning som används.
Hur viskositet och hjälpmolekyler formar partiklarna
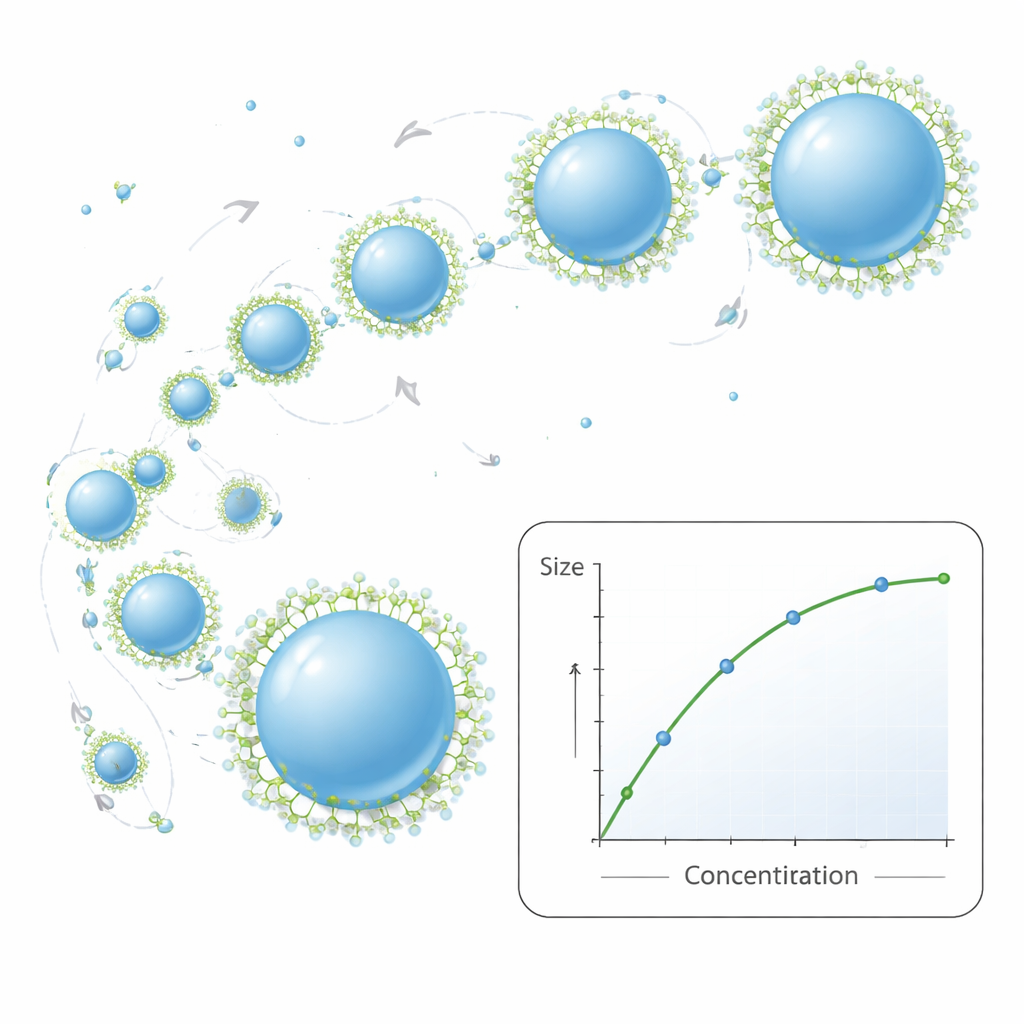
Forskarna undersökte sedan hur receptets ingredienser styr den slutliga partikelstorleken. Att öka mängden PCL i den organiska fasen gör den vätskan tjockare, det vill säga mer viskös. Tänk dig att blanda sirap i vatten istället för juice: tjockare sirap sönderdelas till större droppar. Här ledde tjockare polymerslösningar till större nanopartiklar och något bredare storleksfördelningar. Att tillsätta ett andra lösningsmedel, etanol, hjälpte till att hålla processen stabil även vid mycket höga polymerhalter, men på bekostnad av att partiklarna blev större i det övre koncentrationsområdet. En annan ingrediens, en tensid kallad Pluronic F‑127, fungerar som en molekylär anti‑klumpagent. Vid låga tensidnivåer tenderar partiklarna att stöta ihop och klibba ihop, växa större och bli mindre enhetliga. När tensidkoncentrationen ökar, täcker den partiklarnas ytor, förhindrar sammanflytning och ger mindre, mer stabila nanopartiklar — upp till en gräns där ytterligare ökningar ger måttliga förbättringar och storleksfördelningen kan bli mer blandad.
En enkel växregel som stämmer med verkligheten
I arbetets kärna finns en kompakt matematisk modell som beskriver hur nanopartiklar växer efter att de först framträder. Den behandlar deras rörelse som slumpmässigt skakande i vätskan, där kollisioner ibland leder till att två partiklar förenas till en större. Tidigare modeller antog att partiklar smälter samman omedelbart när de möts och blir perfekta sfärer. Den nya modellen lägger till två realistiska inslag: för det första tillåter den en ändlig tid för två berörande partiklar att slappna av från en förlängd form till en enda sfär; för det andra låter den tensidmolekyler gradvis ”blockera” ytan, vilket saktar ner eller stoppar fortsatt sammansmältning. Med bara några mätbara indata — såsom temperatur, vätskans viskositet och initial polymerkoncentration — förutsäger modellen hur genomsnittlig partikelstorlek förändras med receptförhållanden. I många experiment matchade de förutsagda storlekarna väl de som mättes med ljusspridning, samtidigt som modellen fångade allmänna trender i hur bred storleksfördelningen blir.
Använda modellen som ett designverktyg
För att testa om detta tillvägagångssätt verkligen är användbart vände gruppen på problemet: istället för att be modellen förklara tidigare data bad de den föreslå recept som borde ge tre specifika partikelstorlekar och grad av enhetlighet. De förberedde sedan dessa ”designade” formuleringar i labbet. De uppmätta partikeldiametrarna skiljde sig från målen med endast 1–7 procent — väl inom typisk experimentell variation — vilket visar att modellen kan styra formuleringval på ett tillförlitligt sätt. Förutsägelser om hur smal eller bred storleksfördelningen skulle bli var mindre exakta, men fortfarande tillräckligt bra för att skilja relativt jämna från mer spridda populationer. Jämfört med tungrodda simuleringsmetoder som spårar varje molekyl eller varje virvel i flödet, kör denna strömlinjeformade modell snabbt på måttliga datorer och är enkel att anpassa till andra polymerer och processupplägg.
Vad detta betyder för framtidens nanomedicin
För icke‑specialister är huvudbudskapet att tillverkning av användbara nanopartiklar inte längre behöver förlita sig enbart på mödosamma försök‑och‑fel i labbet. Genom att fånga den väsentliga fysiken för hur små plastdroppar rör sig, kolliderar och skyddas av tensider levererar detta arbete en praktisk ”karta” från formuleringval — hur mycket polymer, vilken lösningsmedelsblandning, hur mycket stabilisator — till slutlig partikelstorlek. Eftersom PCL är ett vanligt biologiskt nedbrytbart material som används i läkemedelsleverans, implantat och avbildningsmedel, kan denna modell hjälpa forskare att snabbare och med mindre materialspill designa säkrare och mer effektiva nanomediciner. Samma principer kan överföras till andra polymerer och ge mer förutsägbarhet och effektivitet inom nanoskaliga terapier.
Citering: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Nyckelord: polymerkapslade nanopartiklar, nanoprecipitation, läkemedelsleverans, numerisk modellering, polykaprolakton