Clear Sky Science · sv
Störning av zinkhomeostas minskar nivåerna av histonacetylering i normala och tumörceller
När en hjälpsam metall blir skadlig
Zink är mest känt som näringsämnet i multivitaminer som stödjer vårt immunförsvar och sårläkning. Men inne i våra celler måste zink hållas inom ett mycket snävt "lagom" intervall. Denna studie visar att när zinknivåerna i celler blir för höga kan de tyst stänga av viktiga gener genom att förtäta hur DNA paketeras, och till och med driva celler mot en självstädande process som kallas autofagi. Eftersom zinktillskott, ämnen i mjällschampon och experimentella cancerläkemedel alla kan förändra zinknivåer, är förståelsen av detta dolda kontrollsystem viktig för vardagshälsa och för framtida terapier.
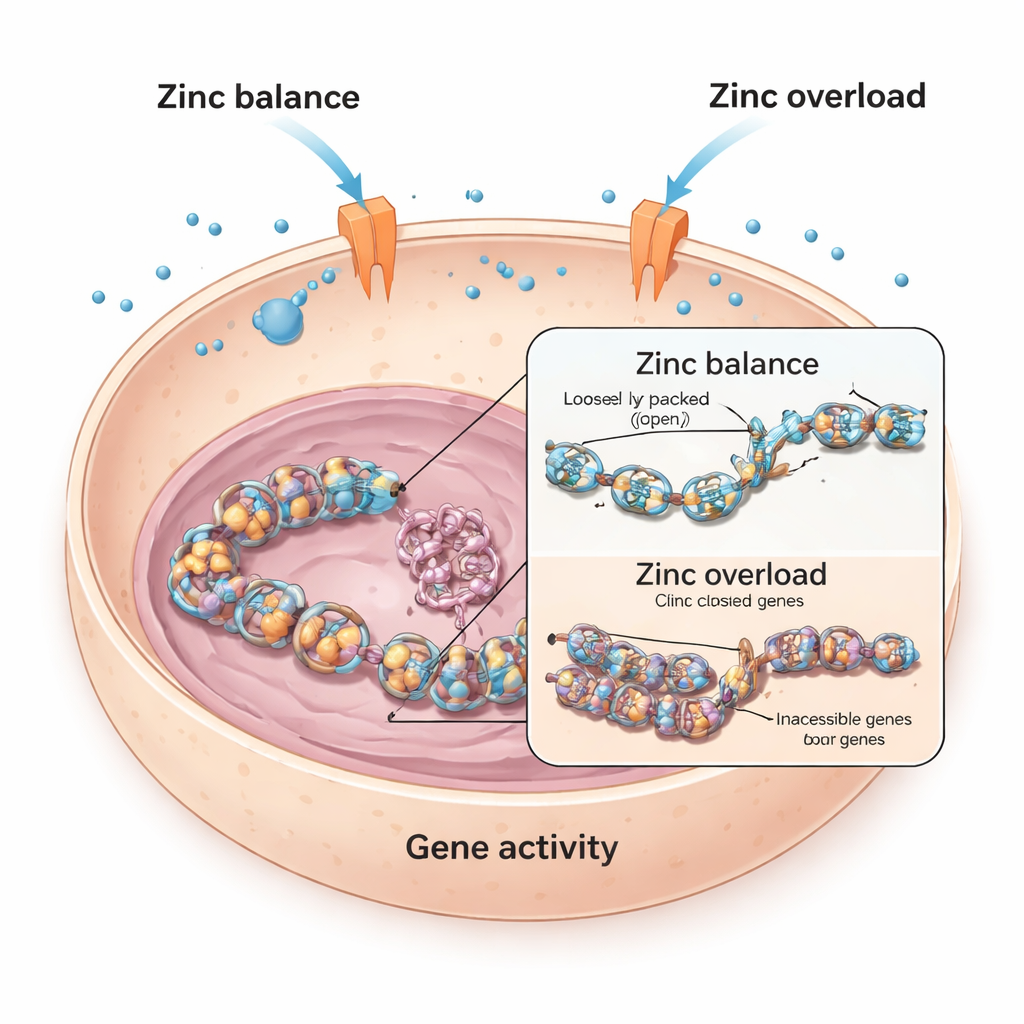
Att balansera zink inne i levande celler
Varje cell är beroende av zink, som hjälper tusentals proteiner att utföra sina funktioner. För att undvika både brist och överbelastning använder celler särskilda "grindar" i sina membran, kallade zinktransporterare, för att flytta zink in och ut. Forskarna började med hjärtmuskelceller från möss och människor och frågade vad som händer när dessa celler utsätts för extra zink. De fann att i mössens hjärtmuskelceller minskade höga zinknivåer starkt aktiviteten hos en nyckelgen relaterad till hjärtat, kallad Bmp4, som hjälper till att styra hjärtutveckling och funktion. I kontrast påverkades humana hjärtceller mycket mindre, vilket antyder att olika celler försvarar sig mot zinköverskott på olika sätt.
Hur zink förtätar DNA-förpackningen
För att ta reda på hur zink tystar gener som Bmp4 tittade teamet på histoner, de spolformade proteiner kring vilka DNA lindas. När små kemiska märken som acetylgrupper läggs till histoner blir DNA lösare och lättare att läsa; när dessa märken tas bort packas DNA hårdare och gener blir svårare att slå på. Studien visade att överskott av zink i mössens hjärtceller ledde till en nedgång i histonacetylering vid en specifik plats (känd som H3K9), vilket följde den sjunkande aktiviteten hos Bmp4. Läkemedel som blockerar histondeacetylaser kunde reversera zinkens effekt och återställa Bmp4, vilket tyder på att zink förskjöt balansen i detta kemiska märkningssystem.
För mycket zink inne, inte bara utanför
Det avgörande steget visade sig vara zink inne i cellens vattenrika cytoplasma, inte bara i den omgivande vätskan. Med en fluorescerande sond som lyser i närvaro av fritt zink såg forskarna en våg av zink inne i mössens hjärtceller efter behandling. När de använde ett zinktransportmolekyl för att tvinga zink direkt in i celler observerade de samma minskning i histonacetylering och genaktivitet, även vid mycket lägre zink i det yttre mediet. I humana hjärtceller justerade däremot membranets transportörer snabbt: vissa zinkimportörer stängde ner och exportörer ökade, vilket förhindrade en stor ökning av internt zink och skyddade histonacetyleringen. Mössens hjärtceller visade en mer "felkopplad" transportörsrespons, vilket tillät mer zink att strömma in och störa genregleringen.
Från genreglering till självstädning i normala och tumörceller
Forskarna frågade sedan om denna zinkdrivna förtätning av DNA-förpackningen är unik för hjärtceller. De testade flera normala humana celltyper och cancercellinjer från magsäck, livmoder och äggstock. När zink tilläts byggas upp inuti med hjälp av en transportör visade nästan alla dessa celler en tydlig minskning av histonacetylering. I vissa tumörceller, såsom magsäckscancerceller, skedde detta vid särskilt låga zinkdoser, vilket antyder att vissa cancrar är ovanligt känsliga för zinkobalans. Teamet kopplade också reducerad acetylering till autofagi, en process där celler återvinner utslitna delar. Måttliga interna zinkökningar ökade autofagi, men mycket höga zinknivåer försvagade den så småningom, vilket tyder på ett smalt fönster där zink skulle kunna användas för att finjustera denna självstädande väg.
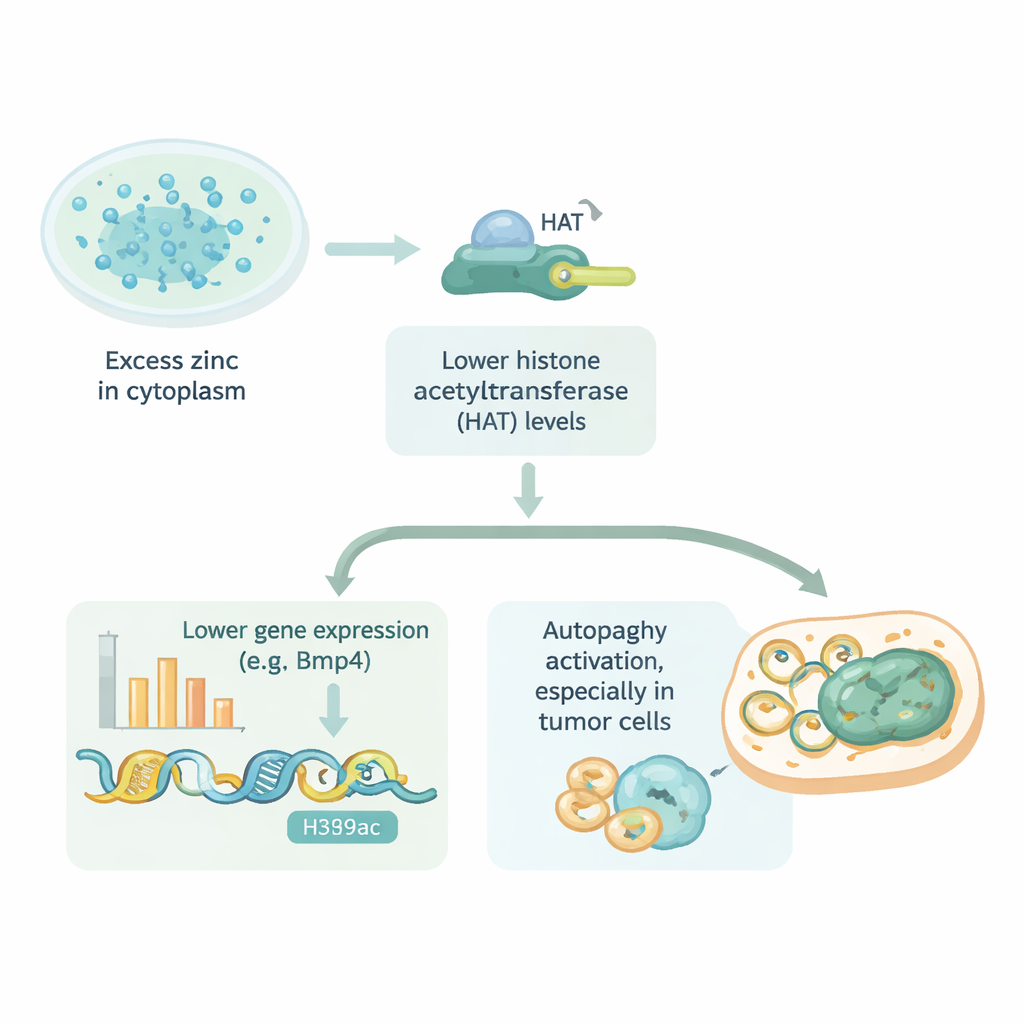
Vad detta betyder för hälsa och behandling
Enkelt uttryckt visar detta arbete att för mycket zink inne i celler kan sänka geners aktivitet genom att göra DNA svårare att nå, och att denna samma väg kan påverka hur aktivt celler rensar upp sig själva. Effekten är inte begränsad till hjärtceller; den förekommer i olika normala och cancerogena celler, även om vissa är bättre på att försvara sig mot zinköverskott än andra. Dessa insikter tyder på att de små zinktransport"grindarna" i cellmembran kan vara lovande läkemedelsmål — antingen för att skydda frisk vävnad från zinkrelaterad skada eller för att driva sårbara tumörceller mot död. Trots att fynden kommer från cellkulturstudier ger de ett nytt perspektiv på hur ett vardagligt näringsämne kan forma genaktivitet och sjukdom när dess känsliga balans rubbas.
Citering: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Nyckelord: zinkhomeostas, genreglering, histonacetylering, autofagi, cancerceller