Clear Sky Science · sv
Metaboliska omprogrammeringar förbättrar motståndskraft mot oxidativ stress i differentierande kardiomyocyter
Varför hjärtcellernas kamp med syre spelar roll
Varje hjärtslag är beroende av specialiserade muskelceller som kallas kardiomyocyter. När vi växer möter dessa celler en dramatisk livsförändring: de går från en syrefattig, sockerdriven miljö i livmodern till en syretrik värld efter födseln. Syre är nödvändigt, men det skapar också skadliga biprodukter som kan skada DNA och döda celler. Denna studie undersöker hur mognande hjärceller omkopplar sin metabolism så att de kan hantera mer syre, generera mer energi och samtidigt skydda sig mot oxidativ skada — insikter som kan informera framtida behandlingar för hjärtsjukdomar och regenerering.
Från enkla byggare till energifyllda atleter
Omogna hjärceller, kända som kardiomyoblaster, är små, delande celler som till stor del förlitar sig på nedbrytning av glukos för energi. När de differentierar till mogna kardiomyocyter slutar de dela sig och växer istället, ofta genom att bli polynukleära, förlängda celler bättre lämpade för kraftfull kontraktion. Med högupplöst mikroskopi följde forskarna denna omvandling under tio dagar i en laboratoriemodell. Markörer för cellproliferation minskade, samtidigt som cellerna sträcktes ut och omorganiserades till fibrösa, hjärtlika strukturer, vilket bekräftade att de hade gått in i ett mer vuxet, kontraktilt tillstånd. 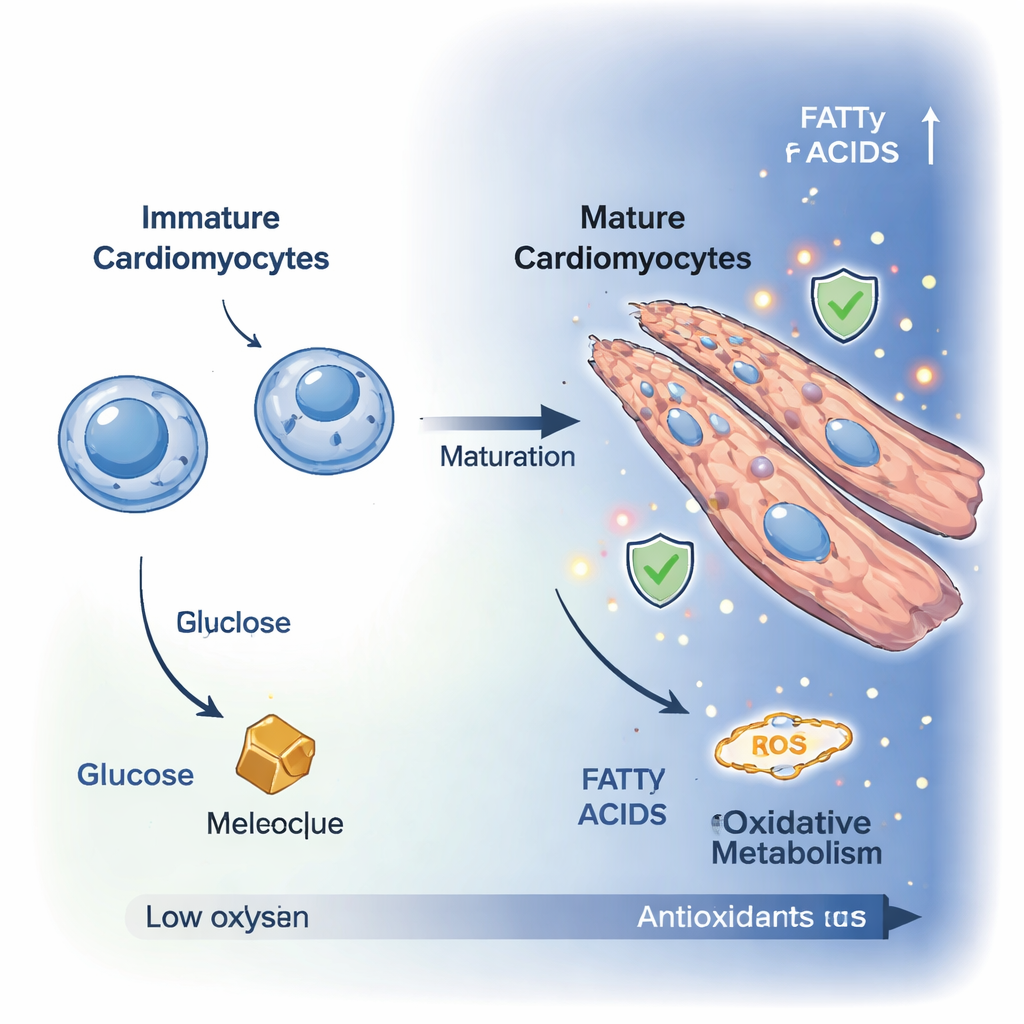
Byte av bränslekällor och nya energivägar
För att förstå vad som händer under huven mätte teamet hundratals småmolekyler i cellerna och använde avancerad avbildning av cellernas naturliga fluorescens för att spåra energianvändning i realtid. Tillsammans visade dessa tekniker ett tydligt skifte från ett glykolytiskt tillstånd, där cellerna huvudsakligen förbränner glukos, till ett oxiderande tillstånd dominerat av mitokondriell respiration. Halterna av glukos och fruktos sjönk, medan intermediärer i trikarboxylsyracykeln (TCA), såsom citronsyra, malat och oxoglutarat, ökade. Väganalys visade starkare aktivitet i rutter som matar bränsle in i mitokondrierna, inklusive malat–aspartat-shutteln och nedbrytning av aminosyror, vilket indikerar att mogna kardiomyocyter breddar sina bränsleval och effektivare kanaliserar energi till sina kraftstationer.
Att leva med mer syre — och mer stress
Effektivare förbränning i mitokondrierna har en kostnad: ökad produktion av reaktiva syreföreningar (ROS), kemiskt aggressiva molekyler som kan skada lipider, proteiner och DNA. Forskarna fann att när kardiomyocyterna mognade blev deras mitokondrier större och mer förlängda, och markörer för oxidativ stress ökade. Fluorescensbaserad avbildning visade fler lipofuscinliknande granuler, ett kännetecken för oxiderade lipider, och en nukleär probe visade högre ROS-nivåer i differentierade celler. Metabolomik pekade på förändringar i glutathionmetabolism, ett centralt antioxidativt system som använder molekylen glutathion — uppbyggd av aminosyror som glutamat och glycin — för att neutralisera ROS. Dessa fynd tyder på att när hjärceller ökar sin oxidativa metabolism finjusterar de samtidigt sina antioxiderande vägar för att hålla skador i schack. 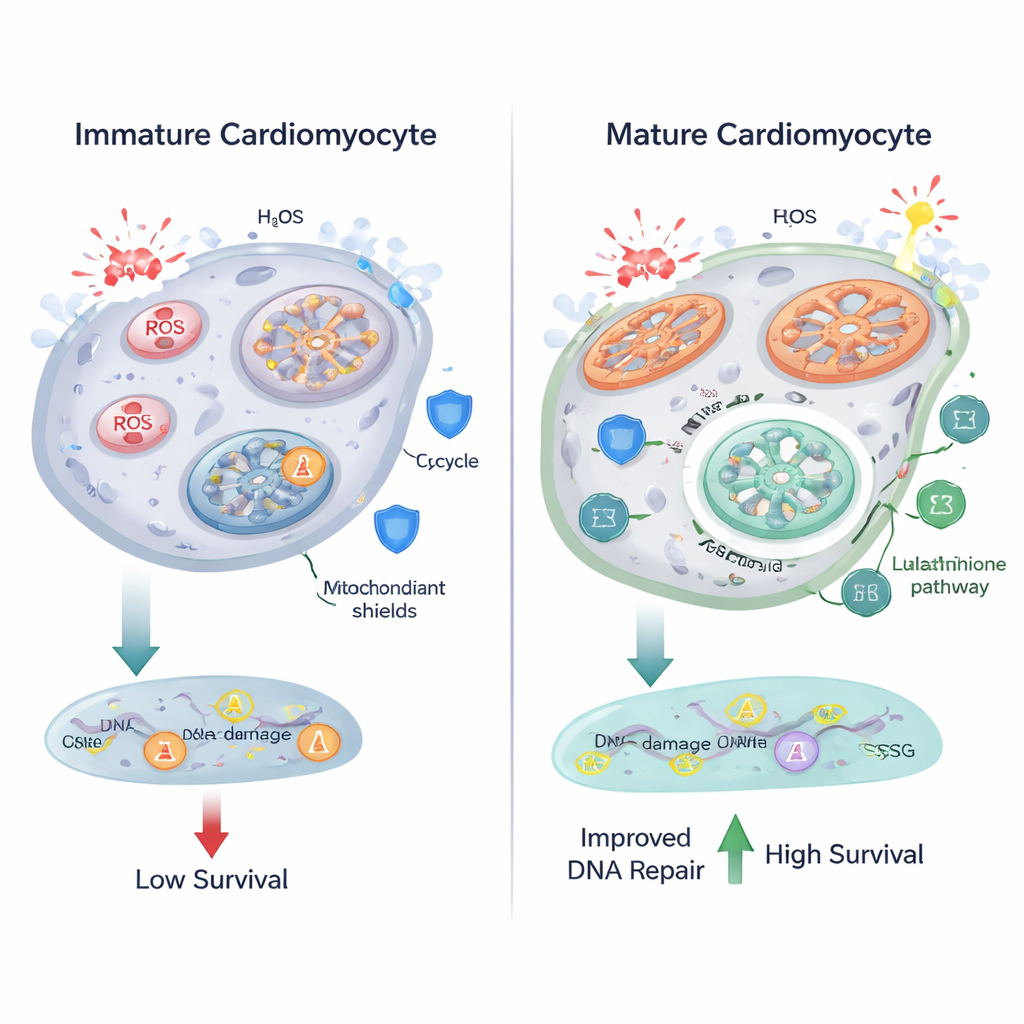
Skador begränsade, försvar stärkta
Överraskande nog visade differentierade kardiomyocyter inte fler DNA‑brott än sina omogna motsvarigheter när man mätte γ‑H2AX‑foci, en känslig markör för DNA‑skada, trots högre ROS. När teamet utsatte cellerna för väteperoxid, ett starkt oxiderande ämne, samlade både omogna och mogna celler på sig ROS och DNA‑brott — men de mogna cellerna klarade sig bättre. De visade proportionellt färre DNA‑lesioner i relation till sina högre ROS‑nivåer, var mindre benägna att aktivera celldödssignaler som PUMA, och uppvisade markant högre överlevnadsgrad. Dessa resultat tyder på att mognande kardiomyocyter inte bara justerar sin metabolism utan också uppgraderar sina reparations- och överlevnadssystem, vilket gör dem bättre rustade att tåla hårdare oxidativa förhållanden.
Vad detta betyder för att skydda hjärtat
Enkelt uttryckt visar denna studie att när hjärceller blir vuxna lär de sig att arbeta hårdare utan att bränna ut sig. De går från en sockerfokuserad, syrefattig livsstil till ett syreintensivt, mitokondriedrivet läge och bygger samtidigt bättre sköldar och reparationslag för att hantera oxidativ stress. Att förstå denna fint avvägda balans mellan energiproduktion och självskydd kan hjälpa forskare att utforma strategier för att göra skadat vuxet hjärtvävnad mer motståndskraftigt, eller att styra stamceller mot säkrare, mer hållbara kardiomyocyter för regenerativa terapier.
Citering: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Nyckelord: kardiomyocytdifferentiering, oxidativ stress, mitokondrier, cellmetabolism, hjärtsjukdom