Clear Sky Science · sv
Deglycosylering framkallar en ny distal konformation i mannossensorn CD206
Varför sockerlager på immunsensorer spelar roll
Våra immunceller förlitar sig på molekylära ”antenner” för att upptäcka hot som mikrober och cancerceller. En av dessa antenner, kallad mannossensorn CD206, hjälper immunceller att fånga sockerdekorerade molekyler och kan till och med rikta in sig mot tumörer. Liksom många proteiner är CD206 täckt av korta socker-kedjor. Denna studie ställer en till synes enkel fråga med stora följder: vad händer med CD206:s form och funktion när dessa sockerbistrar avlägsnas?
En flexibel arm som läser av söta signaler
CD206 sitter på ytan av vissa immunceller, särskilt makrofager som patrullerar vävnader och tumörer. Den har en lång, ledad struktur som sträcker sig ut från cellmembranet och slutar i flera ”lektin”-segment som känner igen socker på passerande molekyler. CD206 kan också lossna och cirkulera i blodet, där dess nivåer korrelerar med inflammatoriska och fibrotiska sjukdomar, vilket gör den till en potentiell markör för sjukdom. Proteinet är starkt dekorerat med N-kopplade socker-kedjor, vilket tidigare arbete visat kan påverka hur väl olika segment av receptorn känner igen socker. Många av dessa sockerställen ligger långt från huvudbindningsfickorna, vilket antyder att de kan fungera mer som avlägsna brytare än som enkla blockeringar.
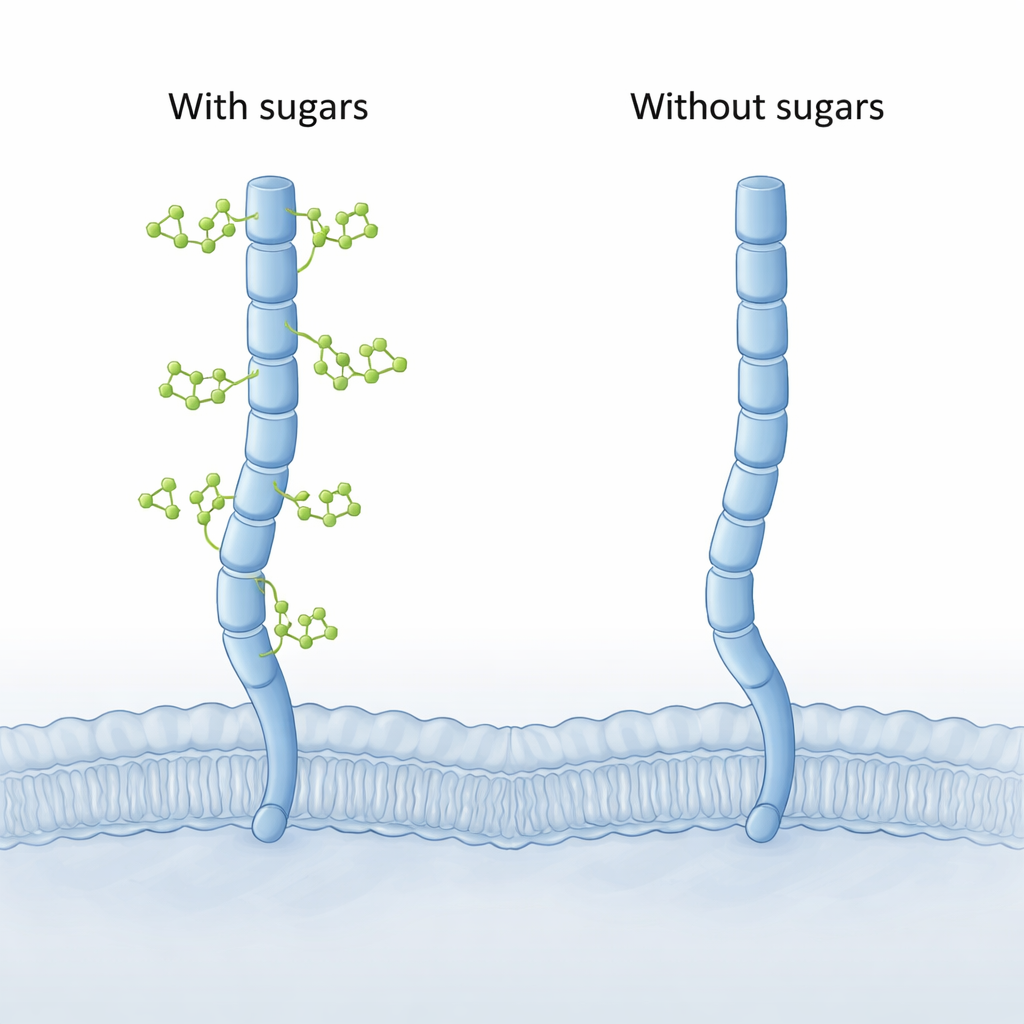
Dator-modeller avslöjar en dold böjning
Eftersom den fullständiga 3D-strukturen av CD206 ännu inte fångats experimentellt, vände sig författarna till moderna beräkningsverktyg. De använde först AlphaFold för att bygga fullängdsmodeller av receptorn och körde sedan långa, detaljerade molekyldynamiksimuleringar av CD206 med och utan dess bundna socker. Båda versionerna uppträdde som en utdragen molekylär arm, men den ”sockerfria” formen visade en påtaglig ny rörelse i sitt yttersta parti. De två sista lektinsegmenten (kallade CTLD7 och CTLD8) kunde svänga inåt och bilda en konkav, inåtböjd spets — en form som aldrig sågs i den sockerdekorerade versionen, som förblev mer utåtböjd, eller konvex.
Hur en liten förändring omformar rörelsen
För att förstå denna skillnad analyserade teamet de dominerande rörelsemönstren i sina simuleringar. De fann att den huvudsakliga rörelsen som skiljde de två formerna åt var denna böjning av det distala tippen, och att den bara uppträdde när socker saknades. Avlägsnande av socker gjorde i allmänhet receptorn mer flexibel, särskilt i de distala lektinsegmenten och i viss mån nära N-terminalen. Korrelationskartor över hur olika delar av proteinet rör sig tillsammans visade att de sista två lektinsegmenten, utan socker, rör sig mer samordnat och är mer tätt kopplade till andra regioner. I praktiken sitter inte sockren bara på ytan; de hjälper till att stämma in hur hela armen böjer sig och kommunicerar längs sin längd.
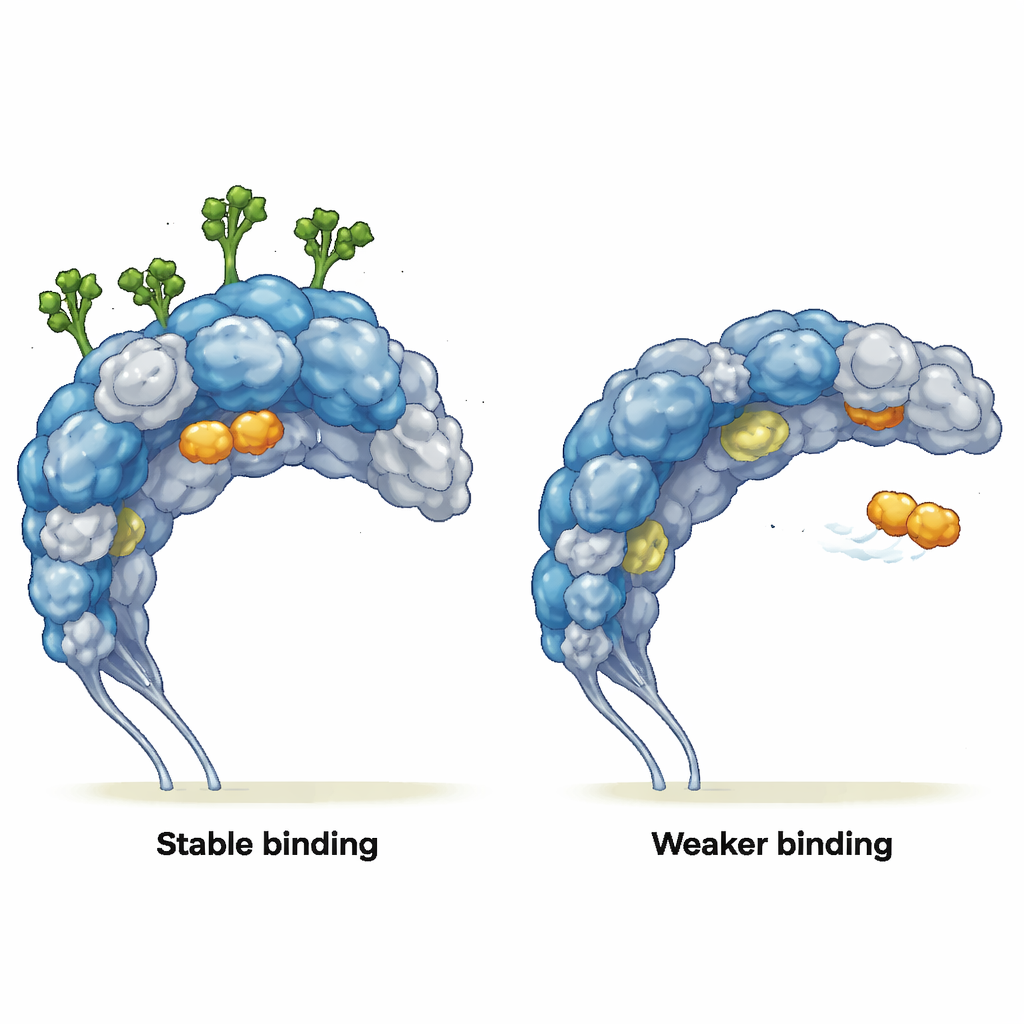
Förändrar hur partner binder
Författarna undersökte därefter hur denna förändrade rörelse påverkar verkliga bindningspartner. De simulerade interaktioner med två ligander: ett enkelt mannosliknande socker (MMA), som passar i en väldefinierad ficka, och en tumör-homing peptid kallad mUNO, som riktar sig mot CD206-positiva tumörassocierade makrofager. När socker var närvarande stannade MMA tryggt i sin bindningsficka under hela simuleringen och bibehöll viktiga kontakter, även om den närliggande proteinstrukturen knappt förändrades. Utan socker undkom MMA fickan, gled över proteinytan och bildade endast kortvariga, ytliga kontakter. För mUNO visade den glykosylerade receptorn flera stabila bindningsposer med frekventa, långvariga kontakter. I den deglykosylerade receptorn var mUNO:s bindning svagare och mer spridd, och den började också utforska regioner som normalt blockeras av socker-kedjor, vilket blottlade nya, tidigare dolda interaktionsytor.
Vad detta betyder för sjukdom och terapi
Tillsammans visar resultaten att de socker som är bundna till CD206 fungerar som avlägsna regulatorer av dess form och klibbighet. Genom att begränsa vissa böjningar och organisera hur dess segment rör sig tillsammans hjälper glykosylering receptorn att hålla fast vid vissa ligander hårdare och styra andra mot föredragna dockningsställen, samtidigt som delar av dess yta skyddas. I sjukdomar som cancer, där de övergripande socker-mönstren på proteiner ofta är förändrade, kan CD206 anta andra former och bindningsbeteenden och därigenom förändra hur immunceller uppfattar sin omgivning. Att förstå denna sockerberoende ”konformationella omkopplare” klargör inte bara hur CD206 fungerar, utan antyder också nya sätt att utforma läkemedel eller avbildningsagenter som utnyttjar dess föränderlig yta i tumörer och andra patologiska tillstånd.
Citering: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Nyckelord: mannossensor, proteinglykosylering, immunigenkänning, tumörassocierade makrofager, molekylär dynamik