Clear Sky Science · sv
Förlust av Snhg5 stör cellcykelreglering utan att ändra cystogenes i en musmodell för polycystisk njursjukdom
Varför en njurgen med ett märkligt namn spelar roll
Polycystisk njursjukdom (PKD) är en vanlig ärftlig sjukdom där otaliga vätskefyllda blåsor långsamt tar över njurarna och ofta leder till njursvikt. Forskare vet att fel i två gener, PKD1 och PKD2, driver sjukdomen, men många andra genetiska aktörer kan påverka hur snabbt den utvecklas. Denna studie fokuserar på en ovanlig typ av gen kallad ett långt icke-kodande RNA, med namnet Snhg5, och ställer en enkel men viktig fråga: påverkar detta molekyl betydligt hur PKD utvecklas, eller är det mest en åskådare?
En närmare titt på en obskyr genetisk budbärare
Till skillnad från typiska gener som ger ritningar för proteiner fungerar långa icke-kodande RNA mer som molekylära organisatörer eller strömbrytare inne i cellerna. Tidigare arbete visade att Snhg5 är starkt uppreglerat i musmodeller för PKD och har kopplats till flera cancerformer och njurskador, vilket antyder att det kan driva skadlig tillväxt. Forskarna kartlade först var och när Snhg5 är aktivt i normala möss. De fann att det är påslaget i många organ, med särskilt höga nivåer i tarmarna, och att dess aktivitet i njuren sjunker kraftigt efter födseln när organet skiftar från snabb tillväxt till ett mer stabilt, moget tillstånd. Inom njurceller finns nästan alla Snhg5-molekyler i kärnan, kommandocentralen som rymmer DNA, vilket tyder på att Snhg5 hjälper till att styra genaktivitet snarare än att bygga proteiner direkt.
Mönster i sjuka njurar berättar inte hela historien
Teamet jämförde sedan Snhg5-nivåer i en rad musmodeller för PKD. I snabbframskridande modeller, där cystor bildas snabbt, var Snhg5 två- till trefaldigt uppreglerat i sjuka njurar, och avbildning på enkelcellnivå visade starka nukleära signaler i cystbeklädnadsceller och intilliggande vävnad. Förvånande nog ökade inte Snhg5 i en långsammare, mildare musmodell som bättre efterliknar det långdragna förloppet hos mänsklig PKD. Än mer anmärkningsvärt var att i njurvävnad från människor med avancerad autosomalt dominant PKD var den mänskliga motsvarigheten, kallad SNHG5, faktiskt reducerad med mer än 90 procent. Tillsammans tyder dessa resultat på att förändringar i detta RNA följer cystbildning, men att riktningen och tidpunkten för förändringen skiljer sig mellan arter och sjukdomsstadier, vilket väcker tvivel om att Snhg5 ensamt är en enkel drivkraft för cysttillväxt.
Vad händer när genen tas bort
För att gå bortom korrelation använde forskarna CRISPR-genredigering för att helt ta bort Snhg5-genen i möss och skapade en global ”knockout”-linje. Tvärtemot oro för att borttagning av en så starkt förändrad molekyl skulle vara skadlig föddes möss utan Snhg5 i normala proportioner, levde normala livslängder och hade njurar som såg ut och fungerade likt sina friska kullsyskon. Mikroskopisk undersökning visade normal njurstruktur utan ärrbildning eller inflammation, och blodprov visade inga tecken på nedsatt njurfiltrering. På molekylär nivå framträdde dock mer subtila förändringar: både musnjurar och odlade njurtubuliceller utan Snhg5 visade konsekventa skift i aktiviteten hos gener kopplade till celldelning och DNA-kopiering. I cellkultur fastnade fler celler i sena faser av cellcykeln och i ett skadat sub-G1-tillstånd. Ett protein i synnerhet, ARPC5, en del av ett komplex som hjälper celler att dela sig genom att omarrangera deras interna skelett, var reducerat när Snhg5 saknades, vilket antyder en möjlig orsakskedja.
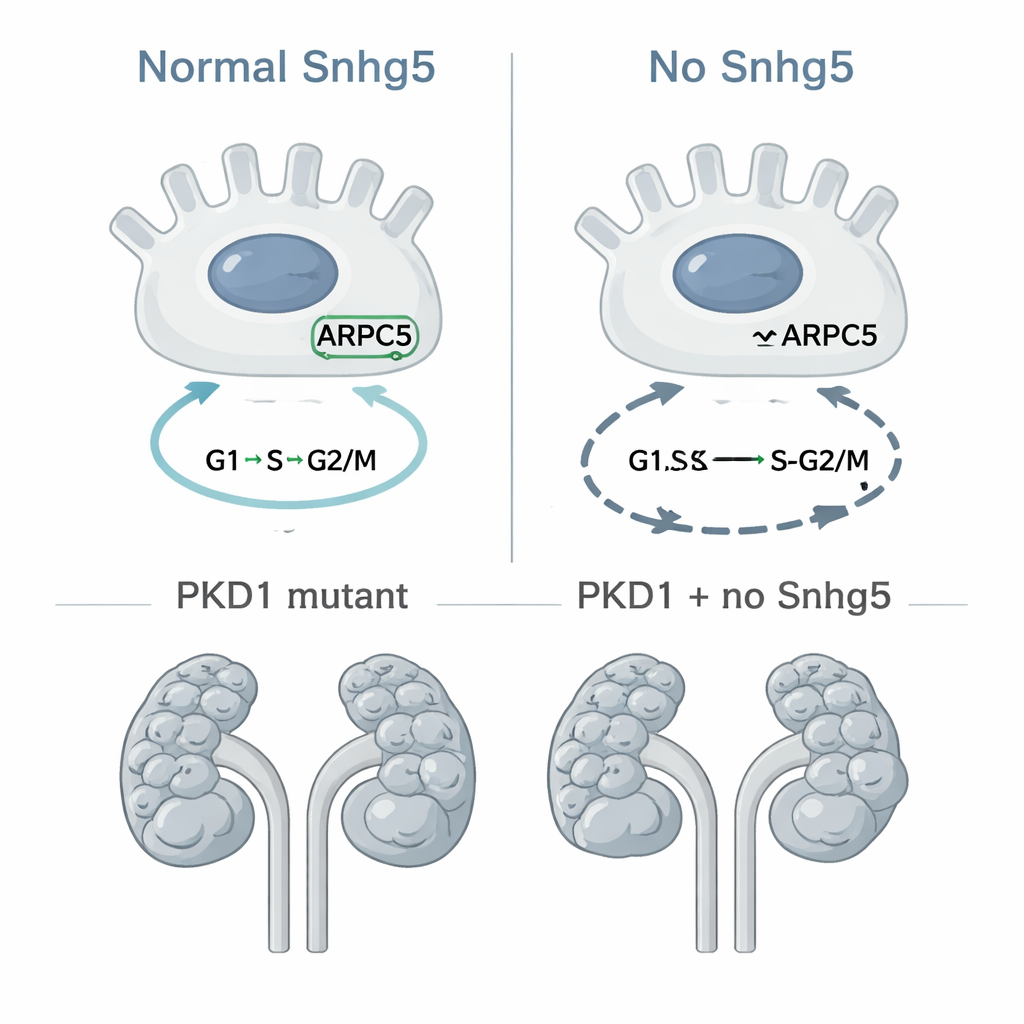
Att testa dess roll i cysttillväxt direkt
Eftersom okontrollerad celldelning är ett kärnfenomen i PKD frågade teamet nästa om borttagning av Snhg5 skulle bromsa cystbildning i en väletablerad musmodell där PKD1-genen är avstängd specifikt i samlingsgångens celler, källan till många cystor. De korsade möss så att vissa bara bar PKD1-mutanten, medan andra saknade både PKD1 och Snhg5. När de undersökte djuren vid 10 dagars ålder visade båda grupperna gravt cystiska njurar, och noggranna mätningar av njurstorlek, cystarea och cystantal visade inget meningsfullt skydd av att ta bort Snhg5. I bästa fall tenderade dubbelmutanterna att ha något större cystbörda, även om skillnaden var liten och inte statistiskt övertygande. Med andra ord, även om Snhg5 påverkar cellcykelgener i njurceller så förändrar dess frånvaro inte märkbart hur snabbt cystor uppträder eller växer i denna specifika PKD-modell.
Vad detta betyder för framtida behandlingar
För patienter och läkemedelsutvecklare är huvudslutsatsen att Snhg5, trots att det är en av de mest kraftigt förändrade genetiska signalerna i mus-PKD, inte är en nav för cystbildning—åtminstone inte i det tidiga, snabbväxande stadiet av samlingsgångsderiverad sjukdom. Genen verkar justera hur njurceller rör sig genom delningscykeln, sannolikt via påverkan på faktorer som ARPC5, men denna påverkan är så subtil att dess fullständiga förlust lämnar njurutveckling och tidig PKD-framsteg i stort sett opåverkade. Dessa fynd understryker en bredare lärdom: inte varje iögonfallande molekylär förändring i sjuk vävnad är ett lovande terapeutiskt mål. Att reda ut orsak från verkan kräver att man testar långa icke-kodande RNA som Snhg5 i flera sjukdomsmodeller och tidpunkter innan de säkert kan drivas som läkemedelskandidater.
Citering: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Nyckelord: polycystisk njursjukdom, lång icke-kodande RNA, Snhg5, cellcykel, njurcystor