Clear Sky Science · sv
Artificiell intelligens för klassificering av rektal neoplasi genom endoskopisk analys av fluorescensperfusion
Varför detta är viktigt för patienter och läkare
För personer med stora rektala polyper är en av de största frågorna om förändringen är ofarlig eller redan håller på att bli cancer. I dag kan läkare ofta inte vara säkra förrän efter att de tagit bort hela lesionen, vilket kan innebära större operationer än nödvändigt eller fördröjd behandling. Denna studie undersöker om en smart bildteknik, kombinerad med artificiell intelligens, kan upptäcka dold cancer under själva proceduren genom att observera hur blodet flödar genom vävnaden.
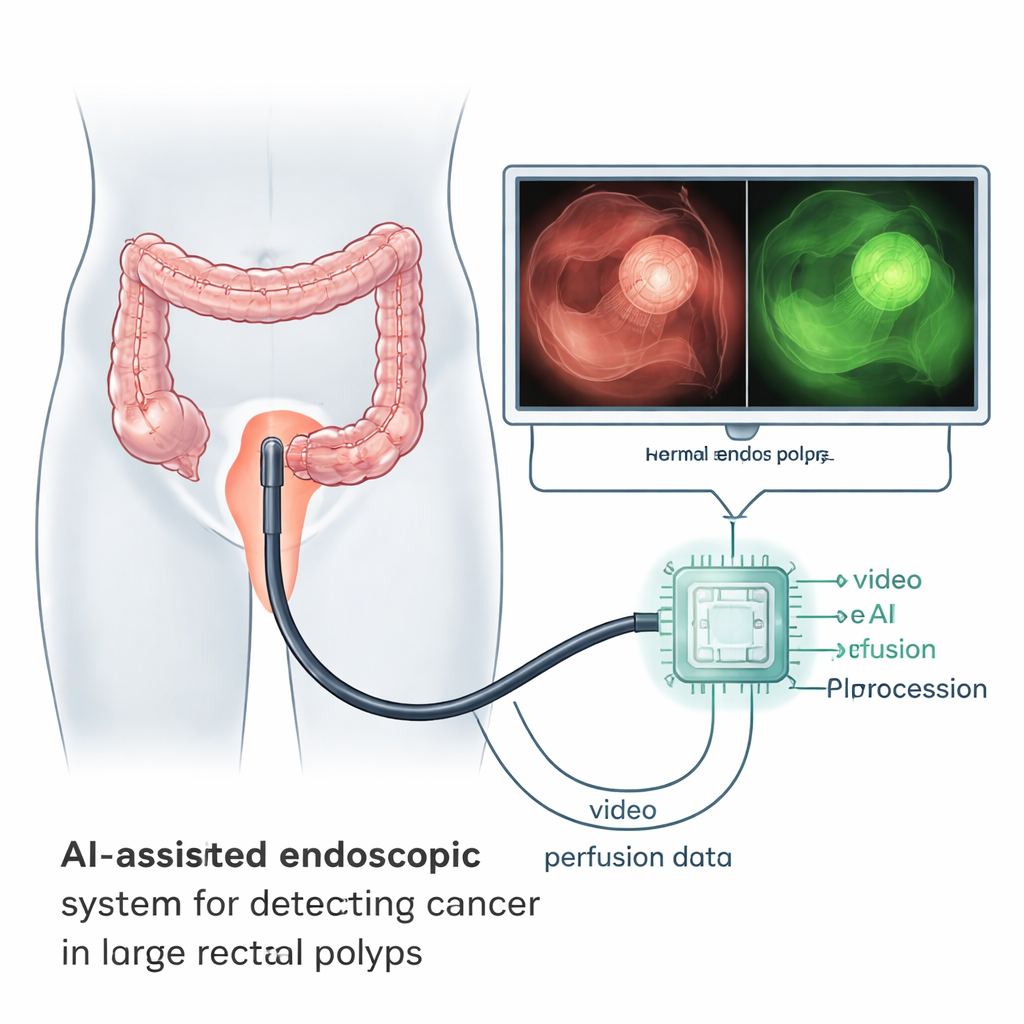
Lyssna på hur en tumör försörjs
Cancer växer inte som normal vävnad. Den stimulerar bildandet av nya, onormala blodkärl som läcker och förgrenar sig på ett oordnat sätt. Dessa förändringar skapar karaktäristiska mönster i hur blod och injicerade färgämnen sköljer in och ut ur en tumör. Forskarna använde ett färgämne kallat indocyaningrönt, som lyser under nära‑infrarött ljus, och spelade in korta videor under endoskopisk kirurgi hos patienter med stora rektala polyper och tidiga rektalcancerformer. Genom att följa ljusstyrkan i glödet över flera minuter kunde de fånga ett slags ”perfusions‑fingeravtryck” för både suspekta och friska områden inom samma patient.
Att omvandla glödmönster till data
Varje video analyserades av skräddarsydd programvara som delade in den synliga delen av tarmväggen i ett rutnät av små rutor och följde dem över tid, även när kamera och vävnad rörde sig. För varje ruta mätte programmet hur stark fluorescensen blev, hur snabbt den nådde sin topp och hur snabbt den avklingade. Därefter rengjordes och normaliserades dessa kurvor så att de kunde jämföras direkt. Från dessa tidsprofiler extraherade teamet enkla numeriska egenskaper, såsom maximal signal och signalminskning vid specifika tider efter toppen. De undersökte också hur ojämna dessa värden var över det avvikande området, med hjälp av en statistisk måttstock som fångar variation inom tumören jämfört med närliggande frisk vävnad.
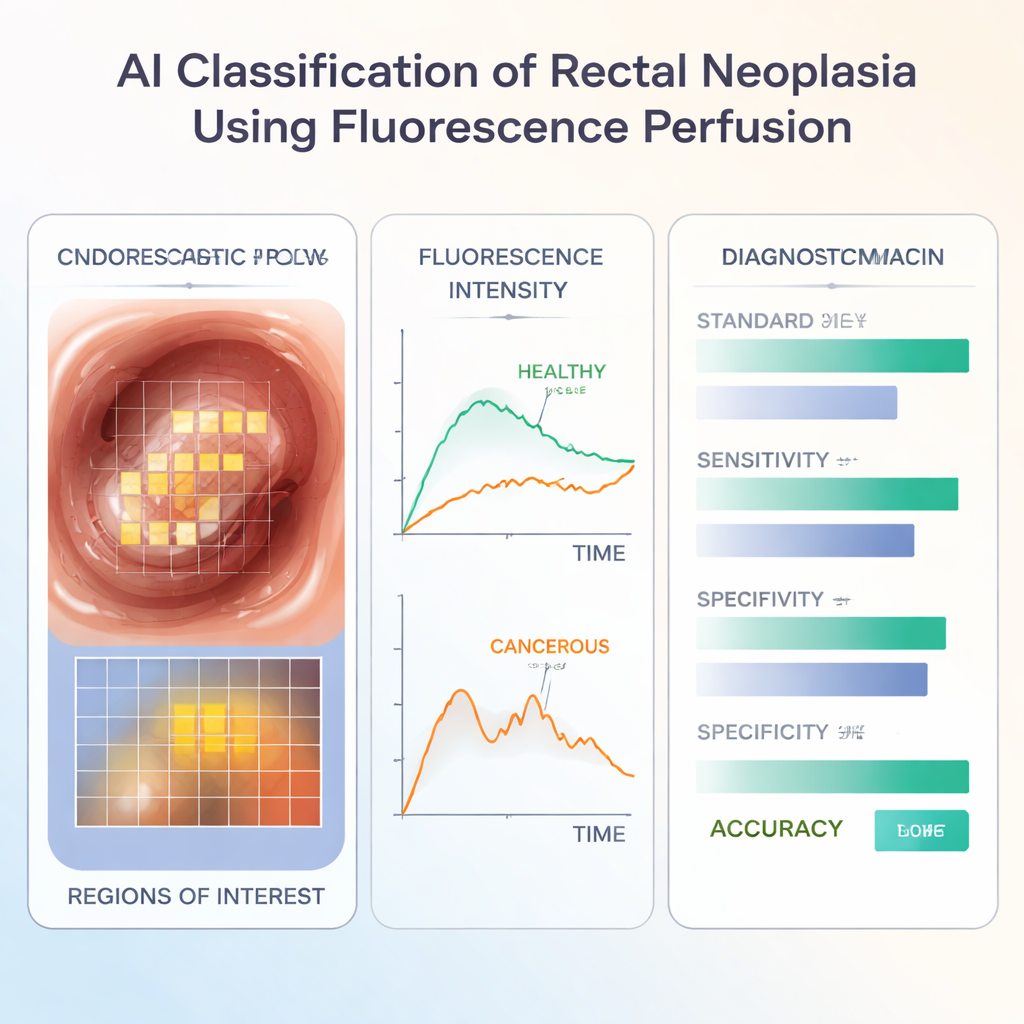
Träning av artificiell intelligens
Gruppen studerade 190 videor från 182 patienter som behandlats vid sex sjukhus i fyra länder; ungefär tre av fem patienter fick slutligen cancer bekräftad i mikroskopet. De tränade en maskininlärningsmodell (en XGBoost‑klassificerare) att lära sig skillnaden mellan godartade och cancerösa lesioner baserat endast på färgämnesflödets egenskaper, utan att titta på de vanliga färgbilderna. När modellen användes på nya fall identifierade den korrekt cancer i en stor majoritet av patienterna och presterade i nivå med eller något bättre än många standardverktyg som används i klinisk praxis, såsom endoskopiska biopsier, preoperativa MR‑undersökningar och den erfarne kirurgens visuella bedömning.
Att lägga till kliniska ledtrådar från verkliga världen
I verkligheten förlitar sig läkare sällan på ett enda test. Forskarna kombinerade därför AI:ns resultat med information som redan fanns tillgänglig: MR‑rapporter och den opererande kirurgens bedömning. När dessa matades in i samma datorflöde förbättrades förmågan att upptäcka cancer, särskilt när det gällde att korrekt utesluta sjukdom i godartade lesioner. I det bästa scenariot upptäckte det kombinerade systemet cirka 86 % av cancerfallen samtidigt som det undvek falska larm i ungefär 71 % av icke‑cancerfall. Metoden fungerade också relativt väl i undergrupper av patienter som var mer typiska för tidig, lokalt avlägsningsbar sjukdom.
Vad detta kan innebära för framtida vård
Studien visar att cancer i stora rektala polyper lämnar ett detekterbart signatur i hur blod och färgämne flödar genom dem, och att denna signatur kan plockas upp automatiskt av AI. Även om arbetet hittills har gjorts på inspelade videor och fortfarande måste bevisas i realtidskliniska prövningar, pekar det mot en framtid där en koloskopist kan varnas under proceduren att en till synes ofarlig polyp sannolikt döljer en invasiv cancer. Den informationen skulle kunna vägleda var man ska ta biopsi, om lesionen ska avlägsnas lokalt eller om patienten bör remitteras för mer omfattande kirurgi, vilket minskar både missade cancerfall och onödiga större operationer.
Citering: Boland, P.A., MacAonghusa, P., Singaravelu, A. et al. Artificial intelligence classification of rectal neoplasia by endoscopic fluorescence perfusion analysis. Sci Rep 16, 4761 (2026). https://doi.org/10.1038/s41598-026-35233-x
Nyckelord: rektalcancer, endoskopisk bildgivning, fluorescensperfusion, artificiell intelligens, maskininlärning